चमकदार लाल, एक बंद प्रणाली में लगातार घूम रहा है रक्त वाहिकाएं. एक वयस्क मानव शरीर में लगभग 5 लीटर रक्त होता है। रक्त का हिस्सा (लगभग 40%) रक्त वाहिकाओं के माध्यम से प्रसारित नहीं होता है, लेकिन "डिपो" (केशिकाएं, यकृत, प्लीहा, फेफड़े, त्वचा) में स्थित होता है। यह एक रिजर्व है जो खून की कमी, मांसपेशियों के काम या ऑक्सीजन की कमी के मामले में खून में प्रवेश करता है। रक्त में थोड़ी क्षारीय प्रतिक्रिया होती है।
खून
कोशिकाएं (46%) - गठित तत्व: एरिथ्रोसाइट्स, ल्यूकोसाइट्स, प्लेटलेट्स;
प्लाज्मा (54%) - तरल अंतरकोशिकीय पदार्थ = पानी + शुष्क पदार्थ (8-10%): कार्बनिक पदार्थ (78%) - प्रोटीन (फाइब्रिनोजेन, एल्ब्यूमिन, ग्लोब्युलिन), कार्बोहाइड्रेट, वसा; अकार्बनिक पदार्थ (0.9%) - आयनों के रूप में खनिज लवण (K+, Na+, Ca2+)
प्लाज्मा एक हल्का पीला तरल है, जिसमें पानी (90%) और उसमें घुले हुए पदार्थ (10%) शामिल हैं; रक्त कोशिकाओं (गठित तत्वों) से शुद्ध रक्त का प्रतिनिधित्व करता है।
पानी के अलावा, प्लाज्मा में प्रोटीन पर आधारित विभिन्न पदार्थ शामिल हैं: सीरम एल्ब्यूमिन, जो कैल्शियम, सीरम ग्लोब्युलिन को बांधता है, जो पदार्थों के परिवहन और प्रतिरक्षा प्रतिक्रियाओं को लागू करने का कार्य करता है; प्रोथ्रोम्बिन और फाइब्रिनोजेन चयापचय प्रक्रियाओं में शामिल हैं। इसके अलावा, प्लाज्मा में बड़ी मात्रा में आयन, विटामिन, हार्मोन, पाचन के घुलनशील उत्पाद और चयापचय प्रतिक्रियाओं के दौरान बनने वाले पदार्थ होते हैं। इसके अलावा, सीरम को प्लाज्मा से अलग किया जा सकता है। सीरम रचना में लगभग प्लाज्मा के समान है, लेकिन इसमें फाइब्रिनोजेन की कमी होती है। सीरम तब बनता है जब खून का थक्का शरीर से अलग होने के बाद शरीर के बाहर जम जाता है।
रक्त के गठित तत्व हैं:
लाल रक्त कोशिकाओं- एक उभयलिंगी आकार की छोटी गैर-परमाणु कोशिकाएँ। वे एक प्रोटीन - हीमोग्लोबिन की उपस्थिति के कारण लाल रंग के होते हैं, जिसमें दो भाग होते हैं: प्रोटीन - ग्लोबिन और आयरन - हीम। लाल रक्त कोशिकाएं लाल अस्थि मज्जा में बनती हैं और सभी कोशिकाओं तक ऑक्सीजन ले जाती हैं। लाल रक्त कोशिकाओं की खोज 1673 में ल्यूवेनहोक ने की थी। एक वयस्क के रक्त में लाल रक्त कोशिकाओं की संख्या 4.5-5 मिलियन प्रति 1 घन मिमी होती है। एरिथ्रोसाइट्स की संरचना में पानी (60%) और सूखा अवशेष (40%) शामिल हैं। ऑक्सीजन के परिवहन के अलावा, एरिथ्रोसाइट्स रक्त प्लाज्मा में विभिन्न आयनों की मात्रा को नियंत्रित करते हैं, ग्लाइकोलाइसिस में भाग लेते हैं, रक्त प्लाज्मा से विषाक्त पदार्थों और कुछ औषधीय पदार्थों को निकालते हैं, कुछ वायरस को ठीक करते हैं।
स्वस्थ महिलाओं में 100 ग्राम रक्त में औसत हीमोग्लोबिन सामग्री 13.5 ग्राम है, और पुरुषों में यह 15 ग्राम है। यदि शरीर से अलग किए गए रक्त को एक तरल पदार्थ से अलग किया जाता है जो थक्के को रोकता है, तो एक कांच की केशिका में रखा जाता है, लाल रक्त कोशिकाएं शुरू हो जाएंगी एक साथ रहना और तल पर बसना। इसे आमतौर पर एरिथ्रोसाइट अवसादन दर (ईएसआर) के रूप में जाना जाता है। सामान्य ईएसआर 4-11 मिमी/घंटा है। ईएसआर दवा में एक महत्वपूर्ण निदान कारक है।

ल्यूकोसाइट्सरंगहीन न्यूक्लियेटेड मानव रक्त कोशिकाएं हैं। आराम से, उनके पास गोलाकार आकार होता है, सक्रिय रूप से स्थानांतरित करने में सक्षम होता है, और रक्त वाहिकाओं की दीवारों में प्रवेश कर सकता है। मुख्य कार्य सुरक्षात्मक है, स्यूडोपोड्स की मदद से वे विभिन्न सूक्ष्मजीवों को अवशोषित और नष्ट कर देते हैं। ल्यूकोसाइट्स की खोज भी 1673 में लीउवेनहोक द्वारा की गई थी और 1946 में आर विरचो द्वारा वर्गीकृत की गई थी। विभिन्न ल्यूकोसाइट्स के साइटोप्लाज्म में दाने होते हैं, या वे नहीं होते हैं, लेकिन एरिथ्रोसाइट्स के विपरीत, उनके पास एक नाभिक होता है।
ग्रैन्यूलोसाइट्स। लाल अस्थि मज्जा में उत्पादित। उनके पास ब्लेड में विभाजित एक कोर है। अमीबीय संचलन में सक्षम। में विभाजित: न्यूट्रोफिल, ईोसिनोफिल, बेसोफिल।
न्यूट्रोफिल. या फागोसाइट्स। वे सभी ल्यूकोसाइट्स का लगभग 70% हिस्सा हैं। वे कोशिकाओं के बीच के रिक्त स्थान से गुजरते हैं जो वाहिकाओं की दीवारों का निर्माण करते हैं, और शरीर के उन हिस्सों में जाते हैं जहां बाहरी संक्रमण का ध्यान केंद्रित होता है। न्यूट्रोफिल रोगजनक बैक्टीरिया के सक्रिय अवशोषक होते हैं, जो परिणामी लाइसोसोम के अंदर पच जाते हैं।
प्लेटलेट्ससबसे छोटी रक्त कोशिकाएं हैं। उन्हें कभी-कभी प्लेटलेट्स कहा जाता है और वे गैर-परमाणु होते हैं। मुख्य कार्य रक्त जमावट में भागीदारी है। प्लेटलेट्स को प्लेटलेट्स कहते हैं। मूल रूप से, वे कोशिकाएँ नहीं हैं। वे लाल अस्थि मज्जा में निहित बड़ी कोशिकाओं के टुकड़े हैं - मेगाकारियोसाइट्स। 1 मिमी3 वयस्क रक्त में 230-250 हजार प्लेटलेट्स होते हैं।
रक्त कार्य:
परिवहन - रक्त ऑक्सीजन, पोषक तत्वों को वहन करता है, कार्बन डाइऑक्साइड, चयापचय उत्पादों को हटाता है, गर्मी वितरित करता है;
सुरक्षात्मक - ल्यूकोसाइट्स, एंटीबॉडी विदेशी निकायों और पदार्थों से रक्षा करते हैं;
नियामक - हार्मोन (पदार्थ जो महत्वपूर्ण प्रक्रियाओं को नियंत्रित करते हैं) रक्त के माध्यम से फैलते हैं;
थर्मोरेगुलेटरी - रक्त में गर्मी होती है;
यांत्रिक - रक्त प्रवाह के कारण अंगों को लोच देता है।
प्रतिरक्षा शरीर की रोगजनक रोगाणुओं और विदेशी निकायों और पदार्थों से खुद को बचाने की क्षमता है।
रोग प्रतिरोधक क्षमताऐसा होता है:
प्राकृतिक - जन्मजात, अधिग्रहित
कृत्रिम - सक्रिय (टीकाकरण), निष्क्रिय (चिकित्सीय सीरम का प्रशासन)
संक्रमण के खिलाफ शरीर की रक्षा न केवल कोशिकाओं - फागोसाइट्स द्वारा की जाती है, बल्कि विशेष प्रोटीन पदार्थों द्वारा भी की जाती है -। प्रतिरक्षा का शारीरिक सार लिम्फोसाइटों के दो समूहों द्वारा निर्धारित किया जाता है: बी- और टी-लिम्फोसाइट्स। प्राकृतिक सहज प्रतिरक्षा को मजबूत करना महत्वपूर्ण है। मनुष्यों में दो प्रकार की प्रतिरक्षा होती है: सेलुलर और विनोदी। सेलुलर प्रतिरक्षा टी-लिम्फोसाइटों के शरीर में उपस्थिति से जुड़ा हुआ है, जो विदेशी कणों के प्रतिजनों को बांधने और उनके विनाश का कारण बनने में सक्षम हैं।
त्रिदोषन प्रतिरोधक क्षमताटी बी-लिम्फोसाइट्स की उपस्थिति से जुड़ा हुआ है। ये कोशिकाएं एंटीबॉडी नामक रसायन का स्राव करती हैं। एंटीबॉडीज, एंटीजन से जुड़ते हैं, फागोसाइट्स द्वारा उनके कब्जे में तेजी लाते हैं, या एंटीजन के रासायनिक विनाश या ग्लूइंग और वर्षा की ओर ले जाते हैं।
प्राकृतिक सहज प्रतिरक्षा. इस मामले में, तैयार एंटीबॉडी स्वाभाविक रूप से एक जीव से दूसरे जीव में जाते हैं। उदाहरण: मातृ प्रतिपिंडों का शरीर में प्रवेश। इस प्रकार की प्रतिरक्षा केवल अल्पकालिक सुरक्षा प्रदान कर सकती है (इन एंटीबॉडी के अस्तित्व की अवधि के लिए)।
प्राकृतिक प्रतिरक्षा प्राप्त की. एंटीजन के स्वाभाविक रूप से शरीर में प्रवेश करने (एक बीमारी के परिणामस्वरूप) के परिणामस्वरूप एंटीबॉडी का निर्माण होता है। इस मामले में गठित "स्मृति कोशिकाएं" एक विशेष प्रतिजन के बारे में जानकारी को काफी समय तक बनाए रखने में सक्षम हैं।
कृत्रिम सक्रिय प्रतिरक्षा. यह तब होता है जब टीके के रूप में कृत्रिम रूप से शरीर में थोड़ी मात्रा में एंटीजन पेश किया जाता है।
कृत्रिम निष्क्रिय. तब होता है जब किसी व्यक्ति को बाहर से तैयार एंटीबॉडी का इंजेक्शन लगाया जाता है। उदाहरण के लिए, टेटनस के खिलाफ तैयार एंटीबॉडी की शुरूआत के साथ। ऐसी प्रतिरक्षा का प्रभाव अल्पकालिक होता है। प्रतिरक्षा के सिद्धांत के विकास में विशेष गुण लुई पाश्चर, एडवर्ड जेनर, आई। आई। मेचनिकोव के हैं।
शरीर का आंतरिक वातावरण बनता है रक्त, लसीका और ऊतक द्रव।
कोशिकाओं, लसीका और रक्त के बीच पदार्थों का आदान-प्रदान किसके द्वारा होता है ऊतकों का द्रवजो ब्लड प्लाज्मा से बनता है। शरीर का आंतरिक वातावरण अंगों के बीच एक विनोदी संबंध प्रदान करता है। वह अपेक्षाकृत स्थिर है। शरीर के आंतरिक वातावरण की स्थिरता कहलाती है समस्थिति.
खून- आंतरिक वातावरण का सबसे महत्वपूर्ण घटक। यह एक तरल संयोजी ऊतक है, जिसमें समान तत्व और प्लाज्मा होते हैं।
रक्त कार्य:
– परिवहन- पूरे शरीर में रसायनों का परिवहन और वितरण करता है;
– रक्षात्मक- इसमें एंटीबॉडी होते हैं, बैक्टीरिया के फागोसाइटोसिस होते हैं;
– थर्मोरेगुलेटरी- चयापचय की प्रक्रिया में उत्पन्न गर्मी का वितरण और बाहरी वातावरण में इसकी रिहाई सुनिश्चित करता है;
– श्वसन- ऊतकों, कोशिकाओं और आंतरिक वातावरण के बीच गैस विनिमय प्रदान करता है।
एक वयस्क मानव शरीर में लगभग 5 लीटर रक्त होता है। भाग वाहिकाओं के माध्यम से प्रसारित होता है, और भाग रक्त डिपो में होता है।
रक्त के सामान्य कामकाज के लिए शर्तें:
– रक्त की मात्रा 7% से कम नहीं होनी चाहिए;
- रक्त प्रवाह दर - 5 एल प्रति मिनट;
- सामान्य संवहनी स्वर बनाए रखना।
रक्त की संरचना :
प्लाज्मारक्त की मात्रा का 55% हिस्सा बनाता है, जिसमें से 90-92% पानी और 8-10% अकार्बनिक और कार्बनिक पदार्थ होते हैं। रक्त प्लाज्मा की संरचना में शामिल हैं: प्रोटीन - एल्ब्यूमिन, ग्लोब्युलिन, फाइब्रिनोजेन, प्रोथ्रोम्बिन। फाइब्रिन रहित प्लाज्मा कहलाता है सीरम. प्लाज्मा पीएच = 7.3-7.4।
आकार के तत्वखून।
एरिथ्रोसाइट्स- लाल रक्त कोशिकाओं। 1 मिमी 3 4-5 मिलियन में।
परिपक्व एरिथ्रोसाइट्स- गैर-केंद्रीकृत, उभयलिंगी कोशिकाएं। मुख्य भाग आयरन युक्त प्रोटीन है हीमोग्लोबिन. यह आणविक ऑक्सीजन का परिवहन करता है, एक नाजुक यौगिक - ऑक्सीहीमोग्लोबिन में बदल जाता है। लाल रक्त कोशिकाएं ऊतकों से कार्बन डाइऑक्साइड का परिवहन करती हैं। इस मामले में, हीमोग्लोबिन कार्बोहेमोग्लोबिन में परिवर्तित हो जाता है। कार्बन मोनोऑक्साइड विषाक्तता में, एक स्थिर हीमोग्लोबिन यौगिक बनता है - कार्बोक्सीहेमोग्लोबिन, ऑक्सीजन को बाँधने में असमर्थ।
लाल रक्त कोशिकाओंन्यूक्लियर, स्टेम सेल से चपटी हड्डियों के लाल अस्थिमज्जा में बनते हैं। परिपक्व एरिथ्रोसाइट्स 100-120 दिनों के लिए रक्त में प्रसारित होते हैं, जिसके बाद वे प्लीहा, यकृत और अस्थि मज्जा में नष्ट हो जाते हैं। लाल रक्त कोशिकाएं अन्य ऊतकों में भी नष्ट हो सकती हैं (खरोंच गायब हो जाती है)।
ल्यूकोसाइट्स- सफेद रक्त कोशिकाएं, व्यास में 8-10 माइक्रोमीटर। 1 मिमी 3 5-8 हजार में।
ल्यूकोसाइट्स- रंगहीन परमाणु कोशिकाएं जिनमें हीमोग्लोबिन नहीं होता है। शरीर की कार्यात्मक स्थिति के आधार पर दिन के दौरान ल्यूकोसाइट्स की संख्या में उतार-चढ़ाव हो सकता है। ल्यूकोसाइट्स एक फागोसाइटिक फ़ंक्शन करते हैं।
लिम्फोसाइटों, एक प्रकार का ल्यूकोसाइट, लिम्फ नोड्स, टॉन्सिल, अपेंडिक्स, प्लीहा, थाइमस, अस्थि मज्जा में बनता है। एंटीबॉडी और एंटीटॉक्सिन का उत्पादन करें। एंटीबॉडी शरीर को विदेशी प्रोटीन - एंटीजन से बचाते हैं।
प्लेटलेट्स- गैर-परमाणु कोशिकाएं (प्लेटलेट्स)। व्यास में 5 माइक्रोमीटर। 1 मिमी 3 - 200-400 हजार में।
प्लेटलेट्स- सपाट, गैर-परमाणु, अनियमित आकार की कोशिकाएं जो रक्त जमावट की प्रक्रिया में भाग लेती हैं और रक्त वाहिकाओं की चिकनी मांसपेशियों के संकुचन में योगदान करती हैं। लाल अस्थि मज्जा में उत्पादित। ये 5-10 दिनों तक रक्त में घूमते रहते हैं, फिर यकृत, फेफड़े और प्लीहा में नष्ट हो जाते हैं।
रक्त आधान . बड़े रक्त की हानि और कुछ बीमारियों के साथ, एक व्यक्ति से रक्त आधान किया जाता है जो एक भाग (लगभग 200 सेमी) देता है 3 ) उसका रक्त - दाता - उस व्यक्ति को जो इसे प्राप्त करता है - प्राप्तकर्ता। इस मामले में, रक्त समूहों की अनुकूलता को ध्यान में रखा जाता है। एरिथ्रोसाइट्स में एक प्रोटीन प्रकृति के पदार्थ होते हैं - एग्लूटीनोजेन्स (सरेस से जोड़ा हुआ), और रक्त प्लाज्मा में - एग्लूटीनिन (ग्लूइंग)। एग्लूटिनिन बी एग्लूटीनोजेन बी, एग्लूटीनिन ά - एरिथ्रोसाइट्स एग्लूटीनोजेन ए के साथ एरिथ्रोसाइट्स से चिपक जाता है। इन पदार्थों की उपस्थिति ने सभी लोगों के रक्त को 4 समूहों में विभाजित करने के आधार के रूप में कार्य किया। रक्त प्रकार (एबीओ सिस्टम) विरासत में मिला है और जीवन भर नहीं बदलता है।
कभी-कभी एक व्यक्ति का रक्त सीरम दूसरे के एरिथ्रोसाइट्स से चिपक जाता है, इसलिए रक्त आधान के बुनियादी नियम का पालन करना आवश्यक है: रक्त आधान के दौरान, प्राप्तकर्ता के प्लाज्मा प्रोटीन को एक ही नाम के दाता के एरिथ्रोसाइट प्रोटीन से चिपकना नहीं चाहिए। योजना के अनुसार विभिन्न समूहों का रक्ताधान संभव है।
रक्त आधान दाता रक्त के चयन और प्राप्तकर्ता को इसके आधान में शामिल है।
रक्त आधान करते समय, की उपस्थिति को ध्यान में रखना आवश्यक है आरएच कारक.
आकार के तत्वों का जीवन कालरक्त सीमित है।
सापेक्ष स्थिरताशरीर में रक्त की मात्रा और संरचना इसके द्वारा प्रदान की जाती है:
रक्त वाहिकाएं,
हेमेटोपोएटिक अंग(लाल अस्थि मज्जा, लिम्फ नोड्स, प्लीहा, यकृत कोशिकाएं जो प्लाज्मा प्रोटीन को संश्लेषित करती हैं)
रक्तस्राव के अंग(यकृत, प्लीहा)।
आरएच कारकएक प्रोटीन है जो अधिकांश लोगों के रक्त प्लाज्मा में मौजूद होता है। ऐसे लोगों को ब्लड ग्रुप के लिए Rh पॉजिटिव कहा जाता है। Rh-negative लोगों में यह प्रोटीन नहीं होता है। रक्त आधान करते समय, आरएच कारक के साथ इसकी अनुकूलता को ध्यान में रखना आवश्यक है। यदि Rh-नकारात्मक व्यक्ति को Rh-पॉजिटिव रक्त चढ़ाया जाता है, तो एरिथ्रोसाइट्स आपस में चिपक जाएंगे, जिससे प्राप्तकर्ता की मृत्यु हो सकती है।
रक्त के थक्के (हेमोस्टेसिस) . जब कोई रक्त वाहिका क्षतिग्रस्त हो जाती है, तो उसमें से बहने वाला रक्त 3-4 मिनट के भीतर जम जाता है, जिससे एक लाल थक्का बन जाता है जो वाहिका के लुमेन को बंद कर देता है और आगे रक्त की हानि को रोकता है। रक्त के थक्के की उपस्थिति के लिए मुख्य प्रतिक्रिया प्लाज्मा में घुले फाइब्रिनोजेन प्रोटीन से अघुलनशील फाइब्रिन प्रोटीन फिलामेंट्स का निर्माण है। फाइब्रिनोजेन और रक्त जमावट में शामिल अन्य पदार्थ (15 से अधिक कारक) रक्त के स्थायी घटक हैं। हालांकि, स्वस्थ लोगों में जमावट की प्रक्रिया जहाजों की चोट और उनसे रक्त के निकलने के बाद ही होती है। यह इस तथ्य के कारण है कि रक्त जमावट की प्रक्रिया पोत की दीवारों की क्षतिग्रस्त कोशिकाओं के क्षय उत्पादों और प्लेटलेट्स की मृत्यु से शुरू होती है। रक्त के थक्के जमने वाले किसी भी कारक की अनुपस्थिति रक्त के थक्के जमने की क्षमता को कम या पूरी तरह से कम कर सकती है, जो हीमोफिलिया जैसी गंभीर बीमारियों का कारण है।
रक्ताल्पता - रक्त में एरिथ्रोसाइट्स और हीमोग्लोबिन (एरिथ्रोसाइट्स का एक प्रोटीन पदार्थ जिसमें लोहा होता है और ऑक्सीजन और कार्बन डाइऑक्साइड के साथ संयोजन करने की क्षमता होती है) की कमी होती है, जिसके परिणामस्वरूप ऊतकों को ऑक्सीजन वितरण बाधित होता है, ऑक्सीजन की कमी विकसित होता है। मरीजों में कमजोरी, थकान, चक्कर आना, चिड़चिड़ापन, सांस की तकलीफ और धड़कन, सिरदर्द, आंखों के सामने "मक्खियों" की झिलमिलाहट, त्वचा का पीलापन और श्लेष्मा झिल्ली होती है। अच्छा पोषण, शरीर की लोहे, विटामिन, ताजी हवा की जरूरतों को पूरा करने से रक्त में लाल रक्त कोशिकाओं और हीमोग्लोबिन की सामान्य सामग्री को बहाल करने में मदद मिलती है।
ऊतकों का द्रव उन कोशिकाओं को स्नान करता है जो पोषक तत्वों और ऑक्सीजन को अवशोषित करती हैं और उसमें कार्बन डाइऑक्साइड और अन्य अपशिष्ट उत्पादों को छोड़ती हैं। केशिकाओं (सबसे छोटी रक्त वाहिकाओं) की दीवारों के माध्यम से ऊतक द्रव और प्लाज्मा (रक्त का तरल भाग) के बीच, प्रसार द्वारा पदार्थों का आदान-प्रदान लगातार किया जाता है। रक्त कोशिकाओं द्वारा आवश्यक पदार्थों को ऊतक द्रव में देता है और उन पदार्थों को अवशोषित करता है जो वे स्रावित करते हैं।
लसीका यह लसीका केशिकाओं में प्रवेश करने वाले ऊतक द्रव से बनता है, जो ऊतक कोशिकाओं के बीच उत्पन्न होता है और लसीका वाहिकाओं में गुजरता है जो छाती की बड़ी नसों में प्रवाहित होता है। लसीका प्रणाली को ऊतकों और रक्त के बीच जल निकासी प्रणाली माना जाता है।
लसीका तंत्र हृदय प्रणाली का हिस्सा है और शिरापरक तंत्र का पूरक है, चयापचय में भाग लेता है, कोशिकाओं और ऊतकों को साफ करता है। इसमें लसीका मार्ग होते हैं जो परिवहन कार्य करते हैं, और प्रतिरक्षा प्रणाली के अंग जो प्रतिरक्षा और जैविक सुरक्षा के कार्य करते हैं।
लसीका प्रणाली की सबसे छोटी संरचनात्मक इकाई लसीका केशिकाएं हैं, जो रक्त केशिकाओं के विपरीत, आँख बंद करके शुरू होती हैं। लसीका केशिकाएं विभिन्न आकृतियों और व्यास की एंडोथेलियल ट्यूब होती हैं जिनमें एक तहखाने की झिल्ली नहीं होती है और एक दूसरे से जुड़कर लसीका जाल बनाती हैं। लसीका पोस्टकेशिकाएं वाल्व युक्त बड़ी संरचनाएं हैं। वे लसीका वाहिकाओं में गुजरते हैं, जो इंट्राऑर्गेनिक और एक्स्ट्राऑर्गेनिक में विभाजित होते हैं और बड़ी संख्या में युग्मित सेमिलुनर वाल्व होते हैं जो लसीका के पीछे के प्रवाह को रोकते हैं।
नसों और धमनियों के साथ स्थित सबसे बड़ी लसीका वाहिकाओं को संग्राहक कहा जाता है। वे शरीर के बड़े हिस्सों से लसीका एकत्र करते हैं: अंग, आंतरिक अंग। लसीका वाहिकाओं को स्थानीयकरण के स्थान के अनुसार गहरे में वर्गीकृत किया जाता है, मुख्य रूप से रक्त वाहिकाओं के साथ स्थित होता है, और सतही, चमड़े के नीचे के ऊतक में स्थित होता है, साथ ही प्रवाह और बहिर्वाह में, लिम्फ के संबंध में आंदोलन के आधार पर लिम्फ नोड्स। क्षेत्रीय लिम्फ नोड्स से लसीका के पारित होने के बाद, कलेक्टर लसीका चड्डी बनाते हैं, और वे लसीका नलिकाओं में संयुक्त होते हैं, जो तब नसों में प्रवाहित होते हैं।
बाएं आधे अंगों और छाती की दीवारों से लसीका बाएं ब्रोंकोमेडिस्टिनल ट्रंक द्वारा, सिर और गर्दन के बाईं ओर से - बाएं गले के ट्रंक से, और बाएं हाथ से - बाएं सबक्लेवियन ट्रंक द्वारा एकत्र किया जाता है। ये सभी वक्ष वाहिनी के ग्रीवा भाग में प्रवाहित होते हैं। वे एक ही नाम के तीन दाहिने चड्डी के अनुरूप हैं, छाती के दाहिने आधे हिस्से के अंगों और दीवारों से लसीका इकट्ठा करते हैं, सिर और गर्दन के दाहिने हिस्से और दाहिने हाथ। दाहिनी लसीका चड्डी दाहिनी लसीका वाहिनी में प्रवाहित होती है, जो बदले में दाहिने शिरापरक कोण में बहती है। सही लसीका वाहिनी की लंबाई 1-1.5 सेमी से अधिक नहीं है।
रोग प्रतिरोधक तंत्र
प्रतिरक्षा के अंग:
केंद्रीय:
1 - थाइमस ग्रंथि (थाइमस) - टी-कोशिकाएं परिपक्व होती हैं;
2 - अस्थि मज्जा (टी- और बी-कोशिकाओं के अग्रदूत होते हैं);
परिधीय:
1 - लिम्फ नोड्स;
2 - प्लीहा;
3 - पाचन तंत्र के लिम्फोइड ऊतक
रोग प्रतिरोधक तंत्रप्रतिरक्षा प्रणाली के सेलुलर तत्वों, जो लिम्फोसाइट्स और प्लास्मोसाइट्स हैं, के कारण शरीर की प्रतिरक्षा सुरक्षा प्रदान करता है।
प्रतिरक्षा तंत्रलिम्फ नोड्स, प्लीहा, अस्थि मज्जा, थाइमस, या थाइमस, साथ ही श्वसन और पाचन तंत्र की दीवारों के लिम्फोइड ऊतक बनाते हैं, जिसमें टॉन्सिल, परिशिष्ट के समूह लिम्फोइड नोड्यूल, समूह और एकल लिम्फोइड नोड्यूल शामिल हैं। इलियम।
लिम्फ नोड्सप्रतिरक्षा प्रणाली के सबसे असंख्य अंग हैं। मानव शरीर में, उनकी संख्या 500 तक पहुँच जाती है। वे सभी लसीका प्रवाह के मार्ग पर स्थित हैं और घटते हुए, इसके आगे बढ़ने में योगदान करते हैं। उनका मुख्य कार्य बाधा-निस्पंदन है, अर्थात्, लसीका प्रवाह के मार्ग के साथ बैक्टीरिया और अन्य विदेशी कणों का प्रतिधारण। इसके अलावा, लिम्फ नोड्स एक हेमटोपोइएटिक फ़ंक्शन करते हैं, लिम्फोसाइटों के निर्माण में भाग लेते हैं, और एक इम्युनोसाइटोपोएटिक फ़ंक्शन, प्लाज्मा कोशिकाओं का निर्माण करते हैं जो एंटीबॉडी का उत्पादन करते हैं।
लिम्फ नोड्स का आकार बहुत विविध हो सकता है: गोल, अंडाकार, लम्बी या सेम के आकार का। आकार 25 से 50 मिमी तक भिन्न होता है।
लिम्फ नोड में एक उत्तल पक्ष होता है, जिसमें 4-6 लसीका वाहिकाएं होती हैं जो लिम्फ लाती हैं, लिम्फ नोड्स को लिम्फ की आपूर्ति करती हैं, और एक अवतल पक्ष, जिसे नोड का द्वार कहा जाता है, दृष्टिकोण। गेट के माध्यम से, इसे खिलाने वाली धमनियां और तंत्रिकाएं नोड में प्रवेश करती हैं। अपवाही लसीका वाहिकाएं, जो नोड और शिरा से लसीका को हटाती हैं, उनमें से भी निकलती हैं। लिम्फ नोड एक संयोजी ऊतक कैप्सूल द्वारा कवर किया गया है।
तिल्लीप्रतिरक्षा प्रणाली का सबसे बड़ा अंग है, जिसकी लंबाई 12 सेमी तक पहुंचती है, और वजन 150-200 ग्राम है। यह बाएं हाइपोकॉन्ड्रिअम में स्थित है, इसमें एक विशेषता भूरा-लाल रंग, एक चपटा लम्बी आकार और एक नरम बनावट है . डायाफ्रामिक-स्प्लेनिक और गैस्ट्रो-स्प्लेनिक लिगामेंट्स की मदद से प्लीहा एक निश्चित स्थिति में तय हो जाती है। ऊपर से यह एक रेशेदार झिल्ली से ढका होता है, जो सीरस झिल्ली (पेरिटोनियम) से जुड़ा होता है।
प्लीहा की उत्तल बाहरी सतह को डायाफ्रामिक कहा जाता है, क्योंकि यह डायाफ्राम के संपर्क में है, और अवतल आंतरिक सतह, जिसे स्प्लेनचेनिक कहा जाता है, पेट का सामना करती है, बृहदान्त्र के प्लीहा के लचीलेपन, अग्न्याशय की पूंछ, बाईं ओर गुर्दे और बाईं अधिवृक्क ग्रंथि। आंत की सतह के खंडों का नाम उनसे सटे अंगों के नाम पर रखा गया है। इसके अलावा, प्लीहा के द्वार उस पर स्थित होते हैं, जिसके माध्यम से वाहिकाएं और तंत्रिकाएं पैरेन्काइमा में प्रवेश करती हैं।
अस्थि मज्जारक्त निर्माण का मुख्य अंग है। नवजात शिशुओं में, यह सभी अस्थि मज्जा गुहाओं को भरता है और इसका रंग लाल होता है। ट्यूबलर हड्डियों के डायफिसिस में 4-5 साल तक पहुंचने पर, लाल अस्थि मज्जा को वसा ऊतक द्वारा बदल दिया जाता है और एक पीले रंग का टिंट प्राप्त होता है। एक वयस्क में, लाल अस्थि मज्जा लंबी हड्डियों, छोटी और सपाट हड्डियों के एपिफेसिस में जमा होता है। इसका द्रव्यमान 1.5 किग्रा तक पहुँच जाता है।
लाल अस्थि मज्जामायलोइड ऊतक द्वारा गठित, जिसमें हेमटोपोइएटिक स्टेम सेल होते हैं। ये कोशिकाएं सभी रक्त कोशिकाओं के पूर्वज हैं और इसके प्रवाह के साथ प्रतिरक्षा प्रणाली के अंगों में प्रवेश करती हैं, जहां उन्हें विभेदित किया जाता है। स्टेम कोशिकाओं का एक हिस्सा थाइमस ग्रंथि में प्रवेश करता है, जहां वे टी-लिम्फोसाइट्स, यानी थाइमस-आश्रित के रूप में अंतर करते हैं। भविष्य में, वे कुछ क्षेत्रों में बस जाते हैं, जिन्हें लिम्फ नोड्स और प्लीहा के थाइमस-आश्रित क्षेत्र कहा जाता है। टी-लिम्फोसाइट्स अप्रचलित या घातक कोशिकाओं को नष्ट करते हैं, साथ ही विदेशी कोशिकाओं को नष्ट करते हैं, सेलुलर और ऊतक प्रतिरक्षा प्रदान करते हैं।
शेष स्टेम कोशिकाएं प्रतिरक्षा प्रणाली के अन्य अंगों में प्रवेश करती हैं, जहां वे उन कोशिकाओं के रूप में अंतर करती हैं जो प्रतिरक्षा प्रणाली, यानी बी-लिम्फोसाइट्स, या बर्सा-आश्रित की मानवीय प्रतिक्रियाओं में भाग लेती हैं। इन कोशिकाओं का नाम पक्षियों में मौजूद फैब्रिकियस के बैग (बर्सा) के नाम से आता है, जो क्लोका की दीवार में लसीका ऊतक का संचय होता है। यह माना जाता है कि मनुष्यों में ऐसा थैला या तो अस्थि मज्जा में स्थित हो सकता है, या यह इलियम और परिशिष्ट के समूह लिम्फोइड नोड्यूल्स द्वारा दर्शाया जाता है। बी-लिम्फोसाइट्स कोशिकाओं के पूर्वज हैं जो एंटीबॉडी, या इम्युनोग्लोबुलिन का उत्पादन करते हैं, और प्रतिरक्षा प्रणाली के परिधीय अंगों के बर्सा-आश्रित क्षेत्रों में बस जाते हैं।
थाइमस ग्रंथि (थाइमस)एक प्रतिरक्षात्मक कार्य करता है, हेमटोपोइजिस का कार्य करता है और अंतःस्रावी गतिविधि करता है। बाद वाला तथ्य हमें इसे न केवल प्रतिरक्षा प्रणाली के अंगों के बीच, बल्कि आंतरिक स्राव के अंगों के बीच भी रैंक करने की अनुमति देता है। थाइमस में, लाल अस्थि मज्जा की स्टेम कोशिकाओं का विभेदन किया जाता है। इसलिए, यह टी-लिम्फोसाइट्स का एक स्रोत है, यानी, प्रतिरक्षा प्रणाली का केंद्रीय अंग। इसके संबंध में, लिम्फ नोड्स और प्लीहा परिधीय अंग हैं।
रोग प्रतिरोधक क्षमता
प्रतिरक्षा के आधुनिक सिद्धांत के केंद्र में - संक्रामक और अन्य विदेशी उच्च-आणविक कार्बनिक एजेंटों की कार्रवाई के लिए शरीर की प्रतिरक्षा जो इसमें प्रवेश कर चुके हैं - आई.आई. की खोज और विचार हैं। मेचनिकोव। वह सबसे पहले यह स्थापित करने वाले थे कि ल्यूकोसाइट्स शरीर को संक्रामक, संक्रामक रोगों से बचाने, उनके रोगजनकों, रोगजनक रोगाणुओं को नष्ट करने, फागोसाइटोसिस द्वारा निर्णायक भूमिका निभाते हैं। उन्हें पचाने या नष्ट करने से ल्यूकोसाइट्स मर जाते हैं। संक्रामक रोगों की रोकथाम में निवारक और चिकित्सीय टीकाकरण की भूमिका महान है - टीकों और सीरा की मदद से टीकाकरण, जो शरीर में कृत्रिम सक्रिय और निष्क्रिय प्रतिरक्षा पैदा करते हैं।
प्रतिरक्षा के प्रकार।
सहज (प्रजाति) और अधिग्रहित (व्यक्तिगत) प्रतिरक्षा के बीच भेद। सहज मुक्तिइस पशु प्रजाति का एक वंशानुगत गुण है। उदाहरण के लिए, खरगोश और कुत्ते पोलियोमाइलाइटिस (शिशु पक्षाघात) के प्रति प्रतिरक्षित हैं, और मनुष्य रिंडरपेस्ट आदि के प्रेरक एजेंट के प्रति प्रतिरक्षित हैं। अधिग्रहीतप्रतिरक्षा में बांटा गया है प्राकृतिकऔर कृत्रिम, और उनमें से प्रत्येक में बांटा गया है सक्रियऔर निष्क्रिय.
प्राकृतिक सक्रिय प्रतिरक्षाएक संक्रामक बीमारी से पीड़ित होने के बाद एक व्यक्ति में उत्पन्न होता है। इसलिए, जिन लोगों को बचपन में खसरा या काली खांसी हुई है, वे अब दोबारा बीमार नहीं पड़ते, क्योंकि उन्होंने अपने रक्त में सुरक्षात्मक पदार्थ बना लिए हैं - एंटीबॉडी (प्रोटीन पदार्थ जो सूक्ष्मजीवों को गोंद या नष्ट कर सकते हैं)। प्राकृतिक निष्क्रिय प्रतिरक्षामाँ के रक्त से सुरक्षात्मक एंटीबॉडी के संक्रमण के कारण, जिसके शरीर में वे बनते हैं, नाल के माध्यम से भ्रूण के रक्त में। बच्चों को खसरा, स्कार्लेट ज्वर, डिप्थीरिया आदि के खिलाफ निष्क्रिय प्रतिरक्षा प्राप्त होती है। 1-2 वर्षों के बाद, जब माँ से प्राप्त एंटीबॉडी नष्ट हो जाते हैं और बच्चे के शरीर से आंशिक रूप से उत्सर्जित हो जाते हैं, तो इन संक्रमणों के प्रति उसकी संवेदनशीलता नाटकीय रूप से बढ़ जाती है।
कृत्रिम सक्रिय प्रतिरक्षामारे गए या कमजोर रोगजनक रोगाणुओं या वायरस, कमजोर माइक्रोबियल जहर - विषाक्त पदार्थों (एनाटॉक्सिन) की संस्कृतियों के साथ स्वस्थ लोगों और जानवरों के टीकाकरण द्वारा प्राप्त किया जाता है। शरीर में इन दवाओं (टीकों) की शुरूआत एक हल्की बीमारी की नकल करती है और शरीर की सुरक्षा को सक्रिय करती है, जिससे उसमें उपयुक्त एंटीबॉडी का निर्माण होता है। बच्चों को खसरा, काली खांसी, डिप्थीरिया, पोलियोमाइलाइटिस, तपेदिक, चेचक, टेटनस के खिलाफ टीका लगाया जाता है, जिससे इन गंभीर बीमारियों के मामलों की संख्या में उल्लेखनीय कमी आई है। कृत्रिम निष्क्रिय प्रतिरक्षारोगाणुओं और उनके जहर - विषाक्त पदार्थों के खिलाफ एक व्यक्ति को एंटीबॉडी और एंटीटॉक्सिन (सूक्ष्मजीवों के अपशिष्ट उत्पादों को बेअसर करने वाले पदार्थ जो मनुष्यों के लिए हानिकारक हैं) युक्त सीरम का प्रशासन करके बनाया जाता है। सेरा उन जानवरों से प्राप्त किया जाता है जिन्हें उपयुक्त विष से प्रतिरक्षित किया जाता है। निष्क्रिय रूप से अधिग्रहीत प्रतिरक्षा आमतौर पर एक महीने से अधिक नहीं रहती है, लेकिन यह चिकित्सीय सीरम की शुरूआत के लगभग तुरंत बाद ही प्रकट होती है। तैयार एंटीबॉडी युक्त समय पर प्रशासित चिकित्सीय सीरम अक्सर एक गंभीर संक्रमण (उदाहरण के लिए, डिप्थीरिया) के खिलाफ एक सफल लड़ाई प्रदान करता है, जो इतनी जल्दी विकसित होता है कि शरीर के पास पर्याप्त एंटीबॉडी का उत्पादन करने का समय नहीं होता है और रोगी की मृत्यु हो सकती है। कुछ संक्रामक रोगों के बाद, प्रतिरक्षा विकसित नहीं होती है, उदाहरण के लिए, गले में खराश, जो कई बार बीमार हो सकती है।
विषयगत कार्य
ए 1। शरीर का आंतरिक वातावरण है
1) रक्त प्लाज्मा, लसीका, अंतरकोशिकीय पदार्थ
2) रक्त और लसीका
3) रक्त और अंतरकोशिकीय पदार्थ
4) रक्त, लसीका, ऊतक द्रव
ए2. रक्त बना होता है
1) प्लाज्मा और गठित तत्व
2) अंतरकोशिकीय द्रव और कोशिकाएं
3) लसीका और आकार के तत्व
4) आकार के तत्व
ए3. एक मकई एक क्लस्टर है
1) रक्त कोशिकाएं
ए 4। एरिथ्रोसाइट्स कार्य करते हैं
1) ऑक्सीजन परिवहन
3) रक्त का थक्का जमना
2) संक्रमण से बचाव
4) फागोसाइटोसिस
ए 5। रक्त के थक्के संक्रमण के साथ जुड़ा हुआ है
1) हीमोग्लोबिन से ऑक्सीहीमोग्लोबिन
2) थ्रोम्बिन से प्रोथ्रोम्बिन
3) फाइब्रिनोजेन से फाइब्रिन
4) फाइब्रिन से फाइब्रिनोजेन
ए 6। दाता से प्राप्तकर्ता को गलत तरीके से रक्त चढ़ाना
1) प्राप्तकर्ता के रक्त को थक्का जमने से रोकता है
2) शरीर के कार्यों को प्रभावित नहीं करता
3) प्राप्तकर्ता के रक्त को पतला करता है
4) प्राप्तकर्ता की रक्त कोशिकाओं को नष्ट कर देता है
ए 7। आरएच नकारात्मक लोग
3) सार्वभौमिक प्राप्तकर्ता हैं
4) सार्वभौम दाता हैं
ए 8। एनीमिया के कारणों में से एक हो सकता है
1) भोजन में आयरन की कमी
2) रक्त में एरिथ्रोसाइट्स की बढ़ी हुई सामग्री
3) पहाड़ों में जीवन
4) खाने में चीनी की कमी
ए9. एरिथ्रोसाइट्स और प्लेटलेट्स का उत्पादन होता है
1) पीली अस्थि मज्जा
2) लाल अस्थि मज्जा
4) तिल्ली
ए10। एक संक्रामक रोग का एक लक्षण रक्त के स्तर में वृद्धि हो सकता है
1) एरिथ्रोसाइट्स
2) प्लेटलेट्स
3) ल्यूकोसाइट्स
4) ग्लूकोज
ए11। के खिलाफ दीर्घकालिक प्रतिरक्षा विकसित नहीं होती है
2) चिकनपॉक्स
4) स्कार्लेट ज्वर
ए12. पागल कुत्ते के काटने पर मरीज को इंजेक्शन लगाया जाता है
1) तैयार एंटीबॉडी
2) एंटीबायोटिक्स
3) कमजोर रेबीज रोगजनकों
4) दर्द की दवाएं
ए 13। एचआईवी का खतरा यह है कि यह
1)सर्दी का कारण बनता है
2) रोग प्रतिरोधक क्षमता कम हो जाती है
3) एलर्जी का कारण बनता है
4) विरासत में मिला है
ए14. टीका प्रशासन
1) रोग की ओर ले जाता है
2) रोग के हल्के रूप का कारण बन सकता है
3) बीमारी का इलाज
4) कभी भी दिखाई देने वाली स्वास्थ्य समस्याएं नहीं होती हैं
ए15. शरीर की प्रतिरक्षा सुरक्षा प्रदान की जाती है
1) एलर्जी
2) एंटीजन
3) एंटीबॉडी
4) एंटीबायोटिक्स
ए16. प्रशासन के बाद निष्क्रिय प्रतिरक्षा होती है
1) सीरम
2) टीके
3) एंटीबायोटिक
4) रक्तदाता
ए17. सक्रिय अधिग्रहीत प्रतिरक्षा के बाद होता है
1) पुरानी बीमारी
3) वैक्सीन की शुरूआत
2) सीरम इंजेक्शन
4) बच्चे का जन्म
ए18. विदेशी अंगों का जुड़ाव विशिष्टता से बाधित है
1) कार्बोहाइड्रेट
2) लिपिड
4) अमीनो एसिड
ए 19. प्लेटलेट्स की मुख्य भूमिका होती है
1) शरीर की प्रतिरक्षा रक्षा
2) गैसों का परिवहन
3) ठोस कणों का फागोसाइटोसिस
4) रक्त का थक्का जमना
ए20. प्रतिरक्षा के फागोसाइटिक सिद्धांत का निर्माण किया
1) एल पाश्चर
2) ई. जेनर
3) आई मेचनिकोव
4) आई। पावलोव
पहले में। कोशिकाओं और रक्त पदार्थों का चयन करें जो इसके सुरक्षात्मक कार्य प्रदान करते हैं
1) एरिथ्रोसाइट्स
2) लिम्फोसाइट्स
3) प्लेटलेट्स
5) हीमोग्लोबिन
योजना
1 परिचय
2. प्रतिरक्षा के रूप:
ए) प्राकृतिक प्रतिरक्षा;
बी) अधिग्रहित प्रतिरक्षा।
3. प्रतिरक्षा के तंत्र
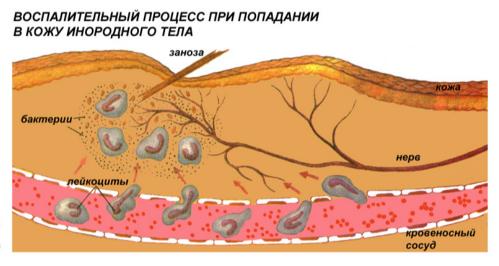
4. सूजन और फागोसाइटोसिस
5. प्रतिरक्षा का नियमन
6. प्रतिरक्षा का बैरियर कार्य
7. इम्यूनोलॉजिकल रिएक्टिविटी
8. प्रतिरक्षा की विकृति
ए) इम्युनोडेफिशिएंसी वायरस की उत्पत्ति;
ख) आपको एड्स कैसे हो सकता है?
c) एड्स किसके द्वारा नहीं हो सकता...
10. साहित्य
परिचय
रोग प्रतिरोधक क्षमता- संक्रामक शुरुआत या किसी बाहरी पदार्थ के लिए जीव की प्रतिरक्षा।
प्रतिरक्षा उन सभी आनुवंशिक रूप से प्राप्त और शरीर द्वारा व्यक्तिगत रूप से प्राप्त अनुकूलन की समग्रता के कारण है जो रोगाणुओं, वायरस और अन्य रोगजनक एजेंटों के प्रवेश और प्रजनन को रोकते हैं और उनके द्वारा स्रावित उत्पादों की क्रिया को रोकते हैं। इम्यूनोलॉजिकल सुरक्षा को न केवल रोगजनक एजेंटों और उनके द्वारा जारी उत्पादों के लिए निर्देशित किया जा सकता है। कोई भी पदार्थ जो एक प्रतिजन है, उदाहरण के लिए, शरीर के लिए एक विदेशी प्रोटीन, प्रतिरक्षात्मक प्रतिक्रियाओं का कारण बनता है, जिसकी मदद से यह पदार्थ शरीर से एक या दूसरे तरीके से हटा दिया जाता है।
विकास ने लगभग 500 मिलियन वर्ष पहले प्रतिरक्षा प्रणाली का गठन किया। प्रकृति की यह उत्कृष्ट कृति हमें सद्भाव और समीचीनता की सुंदरता से प्रसन्न करती है। विभिन्न विशिष्टताओं के वैज्ञानिकों की लगातार जिज्ञासा ने हमें इसके कामकाज के पैटर्न का खुलासा किया और पिछले 110 वर्षों में "मेडिकल इम्यूनोलॉजी" का विज्ञान बनाया।
चिकित्सा के इस तेजी से विकसित हो रहे क्षेत्र में हर साल नई खोजें होती हैं।
एंटीजन -पदार्थ जो शरीर द्वारा विदेशी के रूप में माना जाता है और एक विशिष्ट प्रतिरक्षा प्रतिक्रिया का कारण बनता है। प्रतिरक्षा प्रणाली और एंटीबॉडी की कोशिकाओं के साथ बातचीत करने में सक्षम एंटीजन के शरीर में प्रवेश से प्रतिरक्षा, प्रतिरक्षात्मक सहिष्णुता या एलर्जी का गठन हो सकता है। प्रोटीन और अन्य मैक्रोमोलेक्यूल्स में एंटीजन के गुण होते हैं। "एंटीजन" शब्द का उपयोग बैक्टीरिया, वायरस, पूरे अंगों (प्रत्यारोपण में) के संबंध में भी किया जाता है जिसमें एंटीजन होता है। एंटीजन की प्रकृति का निर्धारण संक्रामक रोगों, रक्त आधान, अंग और ऊतक प्रत्यारोपण के निदान में किया जाता है। टीके और सेरा बनाने के लिए भी एंटीजन का इस्तेमाल किया जाता है।
एंटीबॉडीज -मनुष्यों और गर्म रक्त वाले जानवरों के रक्त प्लाज्मा के प्रोटीन (इम्युनोग्लोबुलिन), जो तब बनते हैं जब विभिन्न एंटीजन शरीर में प्रवेश करते हैं और विशेष रूप से इन एंटीजन से जुड़ने में सक्षम होते हैं। वे शरीर को संक्रामक रोगों से बचाते हैं: सूक्ष्मजीवों के साथ बातचीत करते हुए, वे उनके प्रजनन को रोकते हैं या उत्सर्जित इमिटॉक्सिन को बेअसर करते हैं।
एंटीजेनिक प्रकृति के सभी रोगजनक एजेंट और पदार्थ शरीर के आंतरिक वातावरण की स्थिरता का उल्लंघन करते हैं। इस गड़बड़ी को संतुलित करते समय, जीव आंतरिक वातावरण की स्थिरता को बनाए रखने के उद्देश्य से अपने तंत्र के पूरे परिसर का उपयोग करता है। इम्यूनोलॉजिकल तंत्र इस परिसर का हिस्सा हैं। प्रतिरक्षा जीव वह हो जाता है जिसका तंत्र या तो अपने आंतरिक वातावरण की स्थिरता को परेशान करने की अनुमति नहीं देता है या इस उल्लंघन को जल्दी से समाप्त करना संभव बनाता है। इस प्रकार, प्रतिरक्षा रोगक्षमता की एक स्थिति है, शरीर के आंतरिक वातावरण की स्थिरता को बहाल करने के उद्देश्य से प्रक्रियाओं के एक सेट के कारण, रोगजनक एजेंटों और एंटीजेनिक पदार्थों से परेशान।
संक्रमण के लिए शरीर की प्रतिरक्षा न केवल इसकी प्रतिरक्षात्मक प्रतिक्रिया के कारण हो सकती है, बल्कि अन्य तंत्रों के कारण भी हो सकती है। उदाहरण के लिए, जठर रस की अम्लता मुंह द्वारा कुछ जीवाणुओं के संक्रमण से रक्षा कर सकती है, और जठर रस की उच्च अम्लता वाला जीव कम अम्लता वाले जीव की तुलना में उनसे अधिक सुरक्षित होता है। ऐसे मामलों में जहां प्रतिरक्षा तंत्र के कारण सुरक्षा नहीं होती है, वे जीव के प्रतिरोध के बारे में कहते हैं। प्रतिरक्षा और प्रतिरोध के बीच एक स्पष्ट रेखा खींचना हमेशा संभव नहीं होता है। उदाहरण के लिए, शरीर के संक्रमण के प्रतिरोध में परिवर्तन, जो थकान या ठंडक के परिणामस्वरूप होता है, प्रतिरक्षात्मक सुरक्षा के कारकों की तुलना में जीव के शारीरिक स्थिरांक में परिवर्तन के कारण अधिक होता है। अधिग्रहित प्रतिरक्षा की घटना में यह रेखा अधिक विशिष्ट है, जो उच्च विशिष्टता की विशेषता है, जो प्रतिरोध की घटना में अनुपस्थित है।
प्रतिरक्षा के रूप
प्रतिरक्षा अपने मूल, अभिव्यक्ति, तंत्र और कई अन्य विशेषताओं में विविध है, यही कारण है कि प्रतिरक्षा के कुछ रूपों के रूप में विभिन्न प्रतिरक्षात्मक घटनाओं का वर्गीकरण होता है। मूल
प्राकृतिक प्रतिरक्षा, सहज प्रतिरक्षा और उपार्जित प्रतिरक्षा के बीच अंतर।
प्राकृतिक प्रतिरक्षा- पशु या व्यक्ति की किसी प्रजाति में निहित जन्मजात जैविक विशेषताओं के कारण प्रतिरक्षा। यह एक प्रजाति विशेषता है जो किसी प्रजाति के किसी अन्य रूपात्मक या जैविक लक्षण की तरह विरासत में मिली है। केनाइन डिस्टेंपर या खसरे के लिए कई जानवरों की मानव प्रतिरक्षा प्रतिरक्षा के इस रूप के उदाहरण हैं। यह एक ही जानवर में कई संक्रामक एजेंटों के लिए देखा जाता है, उदाहरण के लिए, मवेशियों से कैनाइन डिस्टेंपर, एवियन डिस्टेंपर, इन्फ्लूएंजा, और अलग-अलग जानवरों में एक ही संक्रामक एजेंट (उदाहरण के लिए, सभी जानवर गोनोक्कू के प्रति प्रतिरक्षित हैं)।
नेचुरल इम्युनिटी का टेंशन बहुत ज्यादा होता है। आमतौर पर इसे निरपेक्ष माना जाता है, क्योंकि अधिकांश मामलों में पूरी तरह से विषाक्त सामग्री की भारी मात्रा के साथ भी संक्रमण से प्राकृतिक प्रतिरक्षा का उल्लंघन नहीं किया जा सकता है। हालांकि, ऐसे कई अपवाद हैं जो प्राकृतिक प्रतिरक्षा की सापेक्षता की गवाही देते हैं। तो, एक चिकन एंथ्रेक्स से संक्रमित हो सकता है यदि उसके शरीर का तापमान कृत्रिम रूप से कम किया जाता है (सामान्य रूप से 41-420) एक ऐसे तापमान पर जो एंथ्रेक्स माइक्रोब (370) के विकास के लिए इष्टतम है। कृत्रिम रूप से अपने शरीर का तापमान बढ़ाकर टेटनस के साथ एक स्वाभाविक रूप से प्रतिरक्षा मेंढक को संक्रमित करना भी संभव है। कुछ मामलों में प्राकृतिक प्रतिरक्षा को आयनकारी विकिरण की क्रिया और प्रतिरक्षात्मक सहिष्णुता के निर्माण से कम किया जा सकता है। कुछ मामलों में, बीमारी की अनुपस्थिति का मतलब यह नहीं है कि कोई संक्रमण नहीं है। अव्यक्त संक्रमण का सिद्धांत एक रोग प्रतिरोधक क्षमता और एक सूक्ष्म जीव की प्रतिरक्षा के बीच अंतर करना संभव बनाता है। कुछ मामलों में, रोग इस तथ्य के कारण नहीं होता है कि शरीर में प्रवेश करने वाले सूक्ष्म जीव इसमें गुणा नहीं करते हैं और मर जाते हैं, अन्य मामलों में रोग उत्पन्न नहीं होता है, इस तथ्य के बावजूद कि सूक्ष्म जीव या वायरस शरीर में प्रवेश कर चुका है। शरीर उसमें गुणा करता है। ये बाद के मामले, स्वाभाविक रूप से प्रतिरक्षा जीवों के अव्यक्त संक्रमणों में होते हैं,
प्राकृतिक प्रतिरक्षा की सापेक्षता की भी गवाही देते हैं। प्राकृतिक प्रतिरक्षा न केवल निहित है
प्रतिरोधी जीव। अतिसंवेदनशील जीवों में भी कुछ, यद्यपि हल्की, प्रतिरक्षा होती है, जैसा कि इस तथ्य से प्रमाणित होता है कि अतिसंवेदनशील जीव रोगाणुओं की संक्रामक खुराक के संपर्क में ही बीमार हो जाता है। यदि एक छोटी खुराक शरीर में प्रवेश करती है, तो ये रोगाणु मर जाते हैं और रोग नहीं होता है। नतीजतन, अतिसंवेदनशील जीव में कुछ हद तक प्राकृतिक प्रतिरक्षा भी होती है। यह "प्राकृतिक प्रतिरक्षा-अतिसंवेदनशील" बहुत व्यावहारिक महत्व का है। रोगाणुओं की एक खुराक जो संक्रामक से कम है, रोग पैदा किए बिना, अधिग्रहित प्रतिरक्षा की उपस्थिति का कारण बन सकती है, जिसका एक संकेतक एंटीबॉडी का गठन है। इसी तरह, कुछ संक्रमणों के लिए आबादी का क्रमिक आयु-विशिष्ट टीकाकरण होता है। डिप्थीरिया में इन प्रक्रियाओं का अच्छी तरह से अध्ययन किया जाता है।
नकारात्मक स्किक प्रतिक्रियाओं की संख्या उम्र के साथ तेजी से बढ़ती है, जो डिप्थीरिया माइक्रोब के साथ आबादी के संपर्क के कारण होती है। डिप्थीरिया बहुत कम मामलों में होता है, और वृद्ध लोगों (60 से 70 वर्ष की उम्र के) के केवल एक छोटे से अनुपात में जिनके रक्त में एंटीटॉक्सिन होता है, उन्हें कभी भी डिप्थीरिया होता है। छोटे बच्चों में डिप्थीरिया के लिए एक निश्चित डिग्री की प्रतिरक्षा के बिना, डिप्थीरिया बैक्टीरिया की कोई भी खुराक उनमें बीमारी का कारण बनेगी, और आबादी के बीच उम्र से संबंधित अस्पष्ट टीकाकरण नहीं होगा। खसरे के साथ भी ऐसी ही स्थिति है, जो लगभग 100% लोगों को प्रभावित करती है। पोलियोमाइलाइटिस के साथ, दूसरी दिशा में एक बदलाव होता है: बहुत कम संख्या में बच्चे बीमार होते हैं, लेकिन 20-25 वर्ष की आयु तक लगभग सभी लोगों में रोगज़नक़ के प्रति एंटीबॉडी होते हैं और इसलिए, इसके साथ संपर्क होता है। इस प्रकार, संवेदनशीलता की अवधारणा, जो प्रतिरक्षा की अनुपस्थिति का पर्याय है, सापेक्ष है। हम केवल संक्रमण की कुछ खुराक के प्रति संवेदनशीलता के बारे में बात कर सकते हैं। इसी समय, यह अवधारणा विशुद्ध रूप से शारीरिक है, क्योंकि संवेदनशीलता शारीरिक तंत्र द्वारा सटीक रूप से निर्धारित की जाती है
विकासवादी प्रक्रिया से उत्पन्न जीव।
प्राप्त प्रतिरक्षाशरीर द्वारा अपने व्यक्तिगत जीवन के दौरान उत्पादित, या तो संबंधित बीमारी (स्वाभाविक रूप से प्राप्त प्रतिरक्षा) या टीकाकरण (कृत्रिम रूप से प्राप्त प्रतिरक्षा) को स्थानांतरित करके। सक्रिय और निष्क्रिय अधिग्रहित प्रतिरक्षा भी हैं। सक्रिय रूप से अधिग्रहीत प्रतिरक्षा या तो स्वाभाविक रूप से होती है, जब कोई संक्रमण फैलता है, या कृत्रिम रूप से, जब जीवित या मृत रोगाणुओं या उनके उत्पादों के साथ टीका लगाया जाता है। दोनों ही मामलों में, प्रतिरक्षा प्राप्त करने वाला जीव स्वयं इसके निर्माण में भाग लेता है और कई सुरक्षात्मक कारकों को विकसित करता है जिन्हें काउंटरबॉडी कहा जाता है। उदाहरण के लिए, जब कोई व्यक्ति हैजा से बीमार हो जाता है, तो उसका सीरम हैजे के रोगाणुओं को मारने की क्षमता प्राप्त कर लेता है; जब एक घोड़े को डिप्थीरिया विष से प्रतिरक्षित किया जाता है, तो उसका सीरम घोड़े के शरीर में एंटीटॉक्सिन के निर्माण के कारण इस विष को बेअसर करने की क्षमता प्राप्त कर लेता है। यदि पहले से बना हुआ एंटीटॉक्सिन युक्त सीरम किसी ऐसे जानवर या व्यक्ति को दिया जाता है जिसे पहले विष नहीं मिला है, तो इस तरह एक एंटीटॉक्सिन के कारण निष्क्रिय प्रतिरक्षा को पुन: उत्पन्न करना संभव है जो उस जीव द्वारा सक्रिय रूप से उत्पादित नहीं किया गया था जिसने सीरम प्राप्त किया था, लेकिन इंजेक्शन वाले सीरम के साथ इसे निष्क्रिय रूप से प्राप्त किया गया था।
सक्रिय रूप से अधिग्रहित प्रतिरक्षा, विशेष रूप से स्वाभाविक रूप से अधिग्रहित, बीमारी या टीकाकरण के हफ्तों के बाद स्थापित की जा रही है, ज्यादातर मामलों में लंबे समय तक रहती है - वर्षों और दशकों तक; कभी-कभी यह जीवन भर बना रहता है (उदाहरण के लिए, खसरे के प्रति प्रतिरोधकता)। हालाँकि, यह विरासत में नहीं मिला है। अधिग्रहित प्रतिरक्षा के वंशानुगत संचरण को स्थापित करने वाले कई अध्ययनों की पुष्टि नहीं हुई है। साथ ही, सक्रिय प्रतिरक्षा विकसित करने की क्षमता निस्संदेह जीव में निहित एक प्रजाति विशेषता है, जैसे संवेदनशीलता या प्राकृतिक प्रतिरक्षा। निष्क्रिय रूप से अधिग्रहीत प्रतिरक्षा बहुत जल्दी स्थापित हो जाती है, आमतौर पर प्रतिरक्षा सीरम की शुरुआत के कुछ घंटों के भीतर, लेकिन बहुत लंबे समय तक नहीं रहती है और गायब हो जाती है क्योंकि शरीर में पेश किए गए एंटीबॉडी गायब हो जाते हैं। यह
आमतौर पर कुछ हफ्तों के भीतर होता है। अपने सभी रूपों में एक्वायर्ड इम्युनिटी अक्सर सापेक्ष होती है और, काफी तनाव के बावजूद, कुछ मामलों में इसे संक्रामक सामग्री की बड़ी खुराक से दूर किया जा सकता है, हालांकि संक्रमण का कोर्स आसान होगा। इम्युनिटी या तो रोगाणुओं के खिलाफ या उत्पादों के खिलाफ निर्देशित की जा सकती है। उनके द्वारा गठित, विशेष रूप से विषाक्त पदार्थों में; इसलिए, वे रोगाणुरोधी प्रतिरक्षा के बीच अंतर करते हैं, जिसमें सूक्ष्म जीव शरीर में विकसित होने के अवसर से वंचित होता है, जो इसे अपने सुरक्षात्मक कारकों और एंटीटॉक्सिक प्रतिरक्षा के साथ मारता है, जिसमें सूक्ष्म जीव शरीर में मौजूद हो सकता है, लेकिन रोग नहीं होता है होता है, क्योंकि प्रतिरक्षा जीव सूक्ष्म जीव के विषाक्त पदार्थों को बेअसर कर देता है।
अधिग्रहीत प्रतिरक्षा का एक विशेष रूप तथाकथित संक्रामक प्रतिरक्षा है। प्रतिरक्षा का यह रूप संक्रमण को स्थानांतरित करने के कारण नहीं होता है, बल्कि शरीर में इसकी उपस्थिति के कारण होता है और जब तक शरीर संक्रमित होता है तब तक मौजूद रहता है। मॉर्गनरोथ (1920), जिन्होंने स्ट्रेप्टोकोकी से संक्रमित चूहों में एक समान रूप देखा, इसे अवसादग्रस्तता प्रतिरक्षा कहा। स्ट्रेप्टोकोकस की छोटी खुराक से संक्रमित चूहे मर नहीं गए, लेकिन एक पुराने संक्रमण से बीमार हो गए; हालांकि, वे स्ट्रेप्टोकोकस की एक घातक खुराक के साथ अतिरिक्त संक्रमण के लिए प्रतिरोधी थे, जिससे स्वस्थ नियंत्रण चूहों की मृत्यु हो गई। उसी प्रकृति की प्रतिरक्षा तपेदिक और कुछ अन्य संक्रमणों के साथ विकसित होती है। संक्रामक प्रतिरक्षा को गैर-बाँझ भी कहा जाता है, अर्थात यह नहीं करता है शरीर को संक्रमण से मुक्त करना, प्रतिरक्षा के अन्य तथाकथित बाँझ रूपों के विपरीत, जिसमें शरीर को संक्रामक शुरुआत से मुक्त किया जाता है। हालांकि, इस तरह की नसबंदी हमेशा नहीं होती है, क्योंकि अधिग्रहित प्रतिरक्षा के मामलों में भी, शरीर लंबे समय तक एक सूक्ष्म जीव या वायरस का वाहक हो सकता है और इसलिए, स्थानांतरित संक्रमण के संबंध में "बाँझ" नहीं हो सकता है।
शरीर के अलग-अलग ऊतकों और अंगों की अलग-अलग प्रतिरक्षात्मक प्रतिक्रिया और प्रतिरक्षा की उपस्थिति और एंटीबॉडी की उपस्थिति के बीच कई मामलों में विसंगति स्थानीय प्रतिरक्षा के सिद्धांत के निर्माण के आधार के रूप में कार्य करती है। ए। एम। बेज़्रेडकी
(1925) इस सिद्धांत के अनुसार, स्थानीय प्रतिरक्षा सामान्य प्रतिरक्षा से स्वतंत्र रूप से उत्पन्न होती है और एंटीबॉडी से जुड़ी नहीं होती है। केवल कुछ ऊतक संक्रमण के लिए अतिसंवेदनशील होते हैं (उदाहरण के लिए, केवल त्वचा एंथ्रेक्स के प्रति संवेदनशील होती है), और इसलिए उनके प्रतिरक्षण से शरीर की सामान्य प्रतिरक्षा हो जाती है। इसलिए प्रस्ताव है कि त्वचा को त्वचा के संक्रमण से, आंतों को आंतों के संक्रमण से प्रतिरक्षित किया जाए। इस मुद्दे के अध्ययन में प्राप्त प्रायोगिक सामग्री की एक बड़ी मात्रा से पता चला है कि स्थानीय प्रतिरक्षा, पूरे जीव पर निर्भर घटना के रूप में मौजूद नहीं है और यह कि सभी मामलों में स्थानीय प्रतिरक्षण एंटीबॉडी के गठन के साथ सामान्य प्रतिरक्षा के उद्भव के साथ होता है। . हालांकि, यह पाया गया कि कुछ ऊतकों की प्रतिरक्षात्मक प्रतिक्रिया की ख़ासियत के कारण कुछ मामलों में स्थानीय टीकाकरण उपयुक्त हो सकता है।
प्रतिरक्षा के तंत्र
प्रतिरक्षा के तंत्र को योजनाबद्ध रूप से निम्नलिखित समूहों में विभाजित किया जा सकता है: त्वचा और श्लेष्मा अवरोध; सूजन, फागोसाइटोसिस, रेटिकुलोएन्डोथेलियल सिस्टम; लसीका ऊतक का बाधा कार्य; विनोदी कारक; सेल प्रतिक्रियाशीलता।
त्वचा और श्लैष्मिक बाधाएँ।त्वचा अधिकांश जीवाणुओं के लिए अभेद्य है।त्वचा की पारगम्यता को बढ़ाने वाले सभी प्रभाव संक्रमण के प्रति इसके प्रतिरोध को कम करते हैं, और इसके पारगम्यता को कम करने वाले सभी प्रभाव विपरीत दिशा में कार्य करते हैं। हालांकि, त्वचा न केवल रोगाणुओं के लिए एक यांत्रिक बाधा है। इसमें स्टरलाइज़िंग गुण भी होते हैं, और त्वचा पर लगने वाले कीटाणु जल्दी मर जाते हैं। अर्नोल्ड (1930) और अन्य वैज्ञानिकों ने देखा कि स्वस्थ मानव त्वचा पर लगाई गई एक चमत्कारी छड़ी इतनी जल्दी गायब हो जाती है कि 10 मिनट के बाद केवल 10% का पता लगाया जा सकता है, और 20 मिनट के बाद - त्वचा पर रखे गए बैक्टीरिया की कुल संख्या का 1%; 30 मिनट के बाद चमत्कारी छड़ी का कोई पता नहीं चला। Escherichia और टाइफाइड बेसिली 10 मिनट के बाद गायब हो गए। यह स्थापित किया गया है कि त्वचा का जीवाणुनाशक प्रभाव इसकी शुद्धता की डिग्री से संबंधित है। त्वचा का स्टरलाइज़िंग प्रभाव केवल उन प्रकार के रोगाणुओं के संबंध में पाया जाता है जो इसके साथ अपेक्षाकृत कम ही संपर्क में आते हैं या इसके साथ बिल्कुल नहीं मिलते हैं। यह रोगाणुओं के संबंध में नगण्य है जो त्वचा के लगातार निवासी हैं, जैसे कि स्टैफिलोकोकस ऑरियस। यह मानने का कारण है कि त्वचा के जीवाणुनाशक गुण मुख्य रूप से पसीने और वसामय ग्रंथियों में लैक्टिक और फैटी एसिड की सामग्री के कारण होते हैं। यह दिखाया गया है कि फैटी एसिड और साबुन युक्त आवश्यक मादक त्वचा के अर्क में स्ट्रेप्टोकोकस, डिप्थीरिया बेसिली और आंतों के बैक्टीरिया के खिलाफ एक ध्यान देने योग्य जीवाणुनाशक प्रभाव होता है, जबकि नमक वाले इस गुण से रहित या लगभग रहित होते हैं।
श्लेष्म झिल्ली भी रोगाणुओं के खिलाफ शरीर की एक सुरक्षात्मक बाधा है, और यह सुरक्षा न केवल यांत्रिक कार्यों के कारण है। गैस्ट्रिक जूस की उच्च अम्लता, साथ ही इसमें लार की उपस्थिति, जिसमें जीवाणुनाशक गुण होते हैं, बैक्टीरिया को गुणा करने से रोकता है। . आंतों के म्यूकोसा, जिसमें बड़ी संख्या में बैक्टीरिया होते हैं, ने जीवाणुनाशक गुणों का उच्चारण किया है। डिस्चार्ज किए गए श्लेष्मा झिल्ली की जीवाणुनाशक क्रिया भी इस डिस्चार्ज में एक विशेष पदार्थ की उपस्थिति से जुड़ी होती है - लाइसोजाइम। लाइसोजाइम आँसू, थूक, लार, प्लाज्मा और रक्त सीरम, ल्यूकोसाइट्स, चिकन प्रोटीन और मछली की मछली में पाया जाता है। आंसू और उपास्थि में लाइसोजाइम की उच्चतम सांद्रता पाई जाती है। मस्तिष्कमेरु द्रव, मस्तिष्क, मल और पसीने में लाइसोजाइम नहीं पाया गया। लाइसोजाइम न केवल जीवित, बल्कि मृत रोगाणुओं को भी घोल देता है। सैप्रोफाइट्स के अलावा, यह कुछ रोगजनक रोगाणुओं (गोनोकोकस, एंथ्रेक्स बैसिलस) पर भी कार्य करता है, कुछ हद तक उनके विकास को रोकता है और आंशिक विघटन का कारण बनता है। इस संबंध में अध्ययन किए गए विषाणुओं पर लाइसोजाइम का कोई प्रभाव नहीं पड़ता है। सबसे अधिक खुलासा कॉर्निया की प्रतिरक्षा प्रणाली के साथ-साथ मुंह, ग्रसनी और नाक की गुहाओं में लाइसोजाइम की भूमिका है। कॉर्निया एक ऐसा ऊतक है जो संक्रमण के प्रति बेहद संवेदनशील होता है, यह सीधे बड़ी मात्रा में वायु रोगाणुओं के संपर्क में आता है, जिसमें वे भी शामिल हैं जो इसके अंदर पपड़ी पैदा कर सकते हैं (स्टैफिलोकोसी, न्यूमोकोकी)। हालांकि, कॉर्निया के ये रोग अपेक्षाकृत दुर्लभ हैं, जिन्हें आँसू की उच्च जीवाणुनाशक गतिविधि द्वारा समझाया जा सकता है जो कॉर्निया को लगातार धोते हैं और उनमें लाइसोजाइम की सामग्री होती है। लार में लाइसोजाइम की उच्च सामग्री के कारण मुंह में कोई भी घाव असामान्य रूप से जल्दी ठीक हो जाता है। यदि ऐसी गड़गड़ाहट की सतह, जो होती है, उदाहरण के लिए, दांत निकालने के दौरान, शरीर के किसी अन्य क्षेत्र में होती है, तो संक्रमण अपरिहार्य होगा। हालाँकि, वोर्टू, इसमें भारी मात्रा में रोगाणुओं की उपस्थिति के बावजूद, ऐसा नहीं होता है। लार की जीवाणुनाशक प्रकृति सभी जानवरों में जीभ चाटने की प्रवृत्ति को समझने योग्य बनाती है। इस तरह की चाट से न केवल संक्रमण का यांत्रिक निष्कासन होता है, बल्कि घाव में एक जीवाणुनाशक एजेंट की शुरूआत भी होती है। इसी समय, जानवर बाहरी संक्रमण की तुलना में मौखिक गुहा से घाव में पेश किए गए रोगाणुओं के प्रति कम संवेदनशील होते हैं। लाइसोजाइम का शारीरिक कार्य अभी भी अस्पष्टीकृत है।
त्वचा या श्लेष्म झिल्ली के माध्यम से संक्रमित अतिसंवेदनशील जानवरों की तुलनात्मक घातकता का अध्ययन करके और इस बाधा को दरकिनार करके त्वचा और श्लेष्मा झिल्ली की सुरक्षात्मक भूमिका का पता चलता है। लाइसोजाइम के अलावा, अन्य जीवाणुनाशक पदार्थ भी ऊतकों और तरल पदार्थों में पाए गए हैं।
विल्सन और रोसेनब्लम (1952) द्वारा दूध के जीवाणुनाशक गुणों का विस्तार से अध्ययन किया गया है। लैक्टेनिन नामक एक विशिष्ट कारक, जो हेमोलिटिक स्ट्रेप्टोकोकस के खिलाफ जीवाणुनाशक है, मनुष्यों, गायों और भेड़ों के दूध में पाया गया है। पाश्चुरीकरण के दौरान लैक्टेनाइन संरक्षित होता है, लेकिन t0 800 और उससे अधिक पर नष्ट हो जाता है।
ये सभी अल्प-अध्ययन किए गए पदार्थ (लैक्टेनिन, पॉलीपेप्टाइड, आदि) शब्द के सही अर्थों में जीवाणुनाशक नहीं हैं, वे एक जीवाणु कोशिका को उसके प्रोटोप्लाज्म को नष्ट करके मार देते हैं। वे रोगाणुओं के प्रजनन को रोकते हैं, जाहिरा तौर पर एंटीबायोटिक दवाओं के समान, उनके चयापचय को प्रभावित करके।
कुछ मामलों में, चयापचय की प्रक्रिया में बनने वाले कुछ तत्वों के ऊतकों में उपस्थिति कुछ सूक्ष्म जीवों के प्रजनन को रोक सकती है या इसमें योगदान दे सकती है। उदाहरण के लिए, यह ज्ञात है कि लोहे की कम सांद्रता डिप्थीरिया रोगाणुओं के कुछ उपभेदों द्वारा विष के उत्पादन के लिए इष्टतम स्थिति बनाती है, और यह कि मानव डिप्थीरिया फिल्मों में लौह सामग्री इस इष्टतम से काफी कम हो सकती है। इसलिए, केवल कुछ उपभेद उचित लौह सांद्रता की उपस्थिति में मनुष्यों में गंभीर बीमारी का कारण बन सकते हैं।
सूजन और फागोसाइटोसिस।
फैगोसाइटोसिस -एककोशिकीय जीवों या विशेष कोशिकाओं - फागोसाइट्स द्वारा जीवित कोशिकाओं या किसी भी छोटे कणों का सक्रिय कब्जा और अवशोषण। फागोसाइटोसिस मुख्य रूप से सूजन में शरीर की सुरक्षात्मक प्रतिक्रियाओं में से एक है। 1882 में आई.आई. मेचनिकोव द्वारा खोजा गया।
सूक्ष्म जीव के एक महत्वपूर्ण विषाणु के साथ और पर्याप्त संक्रामक खुराक पर, त्वचा और म्यूकोसल अवरोध पूरी तरह से अपर्याप्त हो सकते हैं, और सूक्ष्म जीव त्वचा, श्लेष्मा झिल्ली, या चमड़े के नीचे या सबम्यूकोसल परत में प्रवेश करता है। महत्वपूर्ण संख्या में मामलों में, एक भड़काऊ प्रक्रिया विकसित होती है। शरीर को रोगाणुओं से बचाने में इस प्रक्रिया की भूमिका का अध्ययन I.I के नाम से जुड़ा है। मेचनिकोव।
मेचनिकोव ने रोगाणु परतों के कार्यों का अध्ययन किया, विशेष रूप से मध्य रोगाणु परत - अकशेरूकीय भ्रूण में मेसोडर्म; स्पंज के शरीर में किसी भी विदेशी शरीर (ग्लास केशिका) को पेश करते हुए, उन्होंने देखा कि यह मेसोडर्म के मोबाइल अमीबॉइड कोशिकाओं से घिरा हुआ था, जो विभिन्न निष्क्रिय कणों को निगलने में सक्षम था। इसी तरह की प्रक्रिया - ल्यूकोसाइट्स की आकांक्षा, पर्यावरण और उनके द्वारा एक विदेशी शरीर का अवशोषण जो एक भड़काऊ प्रक्रिया का कारण बनता है - अन्य जानवरों की प्रजातियों में भी देखा गया था, दोनों एक संचार प्रणाली के साथ और इसके बिना। रोगाणुओं की कोशिकाओं और I.I के अन्य कोरपसकुलर तत्वों द्वारा अवशोषण की यह प्रक्रिया। मेचनिकोव ने फागोसाइटोसिस कहा। विभिन्न रोगाणुओं के साथ किए गए कई अध्ययनों ने मेचनिकोव को यह निष्कर्ष निकालने की अनुमति दी कि फागोसाइटोसिस भड़काऊ प्रक्रियाओं में और सूजन प्रक्रिया के सुरक्षात्मक कार्य के बारे में प्रमुख है। भड़काऊ प्रतिक्रिया में फागोसाइटोसिस वास्तव में जूलॉजिकल सीढ़ी के सभी चरणों में आवश्यक रक्षा तंत्रों में से एक है। हालांकि, भड़काऊ प्रतिक्रिया का सुरक्षात्मक तंत्र जितना सोचा जा सकता है उससे कहीं अधिक जटिल निकला, और फागोसाइटोसिस सुरक्षा की सभी संभावनाओं को समाप्त नहीं करता है जो भड़काऊ प्रक्रिया अपने साथ लाती है। हिस्टामाइन और सेरोटोनिन, मुख्य रूप से मस्तूल कोशिकाओं से जारी होते हैं, सूजन तंत्र में महत्वपूर्ण भूमिका निभाते हैं। वे केशिका दीवारों की पारगम्यता और संयोजी ऊतक के मुख्य पदार्थ को प्रभावित करते हैं और एंडोथेलियम और मेसेनचाइम की फागोसाइटिक गतिविधि को बढ़ाते हैं। ग्लोबुलिन पारगम्यता कारक और इसके अवरोधक, साथ ही एंजाइम जैसे कई अन्य पदार्थ, जो भड़काऊ प्रक्रिया के विभिन्न चरणों में बदलते हैं, का महत्वपूर्ण महत्व है।
सूजन वाले ऊतक प्रोटीन और अक्रिय कणों को ठीक करने में भी सक्षम होते हैं।त्वचा या पेट की गुहा में सूजन के क्षेत्र में पेश किया गया एक विदेशी प्रोटीन सामान्य ऊतकों की तुलना में लंबी अवधि के लिए बनाए रखा जाता है, और त्वचा में अवधारण होता है उदर गुहा की तुलना में लंबा। सूजन के फोकस में इसी तरह की देरी तब देखी गई जब रंगों को उदर गुहा में इंजेक्ट किया गया। इसलिए, भड़काऊ प्रक्रिया, चाहे वह प्रतिरक्षा या गैर-प्रतिरक्षा जीव में होती है, रोगाणुओं के प्रसार को रोकती है। यह सूक्ष्म जीवों की शुरूआत के तुरंत बाद नहीं होता है, यहां तक कि उन मामलों में भी जहां सूक्ष्मजीव, जैसे स्टेफिलोकोकस, में सबसे गंभीर सूजन पैदा करने की क्षमता होती है। यदि रोगाणुओं में उच्च आक्रामक क्षमता होती है, तो उनमें से कुछ भड़काऊ प्रतिक्रिया होने से पहले शरीर में प्रवेश कर जाते हैं और इतने तीव्र हो जाते हैं कि यह रोगज़नक़ों के प्रसार को रोक सकते हैं। एक तीव्र भड़काऊ प्रतिक्रिया की घटना की दर उत्तेजना की प्रकृति पर निर्भर करती है। भड़काऊ प्रक्रिया का चरण भी आवश्यक है। भड़काऊ प्रतिक्रिया के पहले चरण सक्रिय हाइपरिमिया और त्वरित रक्त और लसीका प्रवाह के साथ होते हैं। इस अवधि के दौरान, बैक्टीरिया को इंजेक्शन साइट से जल्दी से दूर किया जा सकता है, जो संक्रामक प्रक्रिया के विकास में योगदान दे सकता है। हालांकि, यह चरण बहुत छोटा है, और जल्द ही आने वाले संवहनी विकार और ल्यूकोसाइट्स का प्रवाह संक्रमण के प्रसार को रोकता है। इस प्रकार, भड़काऊ प्रतिक्रिया एक रक्षा तंत्र है जो रोगाणुओं के प्रसार को रोकता है, लेकिन शरीर में रोगाणुओं की शुरूआत के तुरंत बाद प्रभाव में नहीं आता है, लेकिन कई घंटों के बाद। भड़काऊ प्रक्रिया के अंतिम चरण में, जब बड़ी मात्रा में ल्यूकोसाइट्स सूजन क्षेत्र में जमा होते हैं, तो फागोसाइटोसिस के कारण शेष रोगाणुओं का गहन विनाश भी होता है।
सूजन के क्षेत्र में रोगाणुओं और विदेशी पदार्थों के निर्धारण और संचय का तंत्र जटिल है। लसीका नाकाबंदी, जो लिम्फ के ठहराव और जमावट के कारण भड़काऊ क्षेत्र में होती है, भड़काऊ फोकस से रोगाणुओं के प्रसार को रोकने वाले मुख्य कारकों में से एक है। यह नाकाबंदी जमा हुआ प्लाज्मा से युक्त एक यांत्रिक अवरोध बनाती है और रोगाणुओं के पारित होने के लिए एक महत्वपूर्ण बाधा है। एक तीव्र भड़काऊ प्रक्रिया में, मंदी नहीं होती है, लेकिन सूजन क्षेत्र के माध्यम से लसीका प्रवाह का त्वरण होता है, और बैक्टीरिया और अन्य विदेशी कण इस क्षेत्र में विभिन्न भौतिक-रासायनिक कारकों की कार्रवाई के कारण तय होते हैं।
भड़काऊ फोकस में रोगाणुओं के निर्धारण और विनाश में एक महत्वपूर्ण भूमिका फागोसाइटोसिस और एंटीबॉडी द्वारा निभाई जाती है।
ल्यूकोसाइट्स, जो सूजन के क्षेत्र में बहुतायत में जमा होते हैं, एक प्रकार का शाफ्ट बनाते हैं जो जीवों के प्रसार को रोकता है। इसके साथ ही, ल्यूकोसाइट शाफ्ट के सेलुलर तत्व सक्रिय रूप से रोगज़नक़ को नष्ट कर देते हैं।केशिका दबाव में वृद्धि और केशिका पारगम्यता में वृद्धि जो सूजन के दौरान होती है, केशिका एंडोथेलियम के माध्यम से द्रव की मात्रा में वृद्धि का कारण बनती है। भड़काऊ क्षेत्र रक्त में निहित पदार्थों से समृद्ध होता है, जिसमें एंटीबॉडी (सामान्य और प्रतिरक्षा) शामिल हैं। बैक्टीरिया पर कार्य करने वाले एंटीबॉडी, उन्हें सेलुलर रक्षा कारकों के लिए अधिक सुलभ बनाते हैं और उन्हें सूजन के क्षेत्र में रखते हैं। यह संभव है कि सूजन के क्षेत्र में ध्यान केंद्रित करने वाले एलेक्सिन, बीटालिसिन और अन्य गैर-विशिष्ट सुरक्षात्मक कारक, भड़काऊ प्रतिक्रिया के कारण जटिल रक्षा तंत्र में भूमिका निभाते हैं।
जैसा कि ज्ञात है, फागोसाइट्स की मुख्य संपत्ति इंट्रासेल्युलर रूप से पचाने की उनकी क्षमता है। हालांकि, यह क्षमता हमेशा नहीं होती है और सभी रोगाणुओं के संबंध में उचित डिग्री के लिए व्यक्त नहीं होती है। कभी-कभी फागोसाइट्स द्वारा पकड़े गए रोगाणुओं को न केवल उनके द्वारा पचाया नहीं जाता है, बल्कि उनमें संग्रहीत और गुणा किया जाता है (अपूर्ण फागोसाइटोसिस)। इस मामले में, फागोसाइटोसिस जीव की सुरक्षात्मक प्रतिक्रिया नहीं है, बल्कि, इसके विपरीत, रोगाणुओं को जीव के जीवाणुनाशक गुणों से बचाता है। हालाँकि, यह घटना दुर्लभ है। फागोसाइट्स की एक अन्य विशेषता रोगाणुओं और उनके उत्पादों के प्रति उनका सकारात्मक रसायन है। सकारात्मक केमोटैक्सिस भी उनके प्रवेश के स्थल पर जमा होने वाले ल्यूकोसाइट्स द्वारा शरीर में घुसने वाले रोगाणुओं के विनाश की संभावना को निर्धारित करता है। हालांकि, रोगाणुओं या विषाक्त पदार्थों की बड़ी खुराक नकारात्मक केमोटॉक्सिस का कारण बन सकती है, और फिर फागोसाइटिक प्रतिक्रिया को महसूस नहीं किया जा सकता है। एक भड़काऊ प्रतिक्रिया के साथ, ल्यूकोसाइट्स का एक महत्वपूर्ण संचय होता है जो केमोटॉक्सिक आकर्षण के कारण जहाजों की दीवारों से गुजरते हैं। भड़काऊ प्रक्रियाओं के दौरान जमा होने वाला मवाद ये संचय है।
लेकिन सूजन की अनुपस्थिति में भी, फागोसाइटोसिस की सुरक्षात्मक भूमिका को काफी प्रदर्शनकारी रूप से प्रकट किया जा सकता है। जब रोगाणुओं को एक प्रतिरक्षा जानवर में पेश किया जाता है, तो बाद वाले तुरंत फागोसाइट्स द्वारा कब्जा कर लिए जाते हैं; इसलिए, उदाहरण के लिए, एक मेंढक को एंथ्रेक्स की खेती शुरू करने पर, यह देखा जा सकता है कि थोड़ी देर के बाद सभी सूक्ष्म जीवों को फैगोसाइटोज किया जाता है, और संक्रमण विकसित नहीं होता है। किसी भी जानवर को विभिन्न प्रकार के गैर-रोगजनक रोगाणुओं को पेश करते समय भी यही देखा जा सकता है। अतिसंवेदनशील जीव में, फैगोसाइटोसिस या तो बिल्कुल भी नहीं देखा जाता है, या केवल कुछ हद तक ही देखा जाता है। फागोसाइट्स जीवित रोगाणुओं को पकड़ने में सक्षम हैं। यदि आप ल्यूकोसाइट्स युक्त एक एक्सयूडेट लेते हैं, जिसने एंथ्रेक्स बेसिली की संस्कृति प्राप्त करने वाले मेंढक से सभी बेसिली को पूरी तरह से पकड़ लिया है, और इसे गिनी पिग से मिलाते हैं, तो बाद वाला एंथ्रेक्स से मर जाएगा, क्योंकि मेंढक के ल्यूकोसाइट्स अनुपयुक्त हो गए हैं एक गिनी पिग के शरीर में वातावरण, मर जाते हैं और इस प्रकार उनमें कैद लोगों को मुक्त कर देते हैं जो काफी विषाणुजनित सूक्ष्म जीव होते हैं। जीव के सुरक्षात्मक तंत्र के रूप में फागोसाइटोसिस के निस्संदेह महत्व का प्रमाण यह भी है कि फागोसाइट का दमन या इसके लिए बाधाओं का निर्माण जीव के प्रतिरोध को कम करता है। यदि टेटनस के बीजाणुओं को विष से अच्छी तरह से धोया जाता है और पशु शरीर में पेश किया जाता है, तो वे जल्दी से फागोसाइटोज हो जाते हैं, और टेटनस रोग नहीं होगा। हालाँकि, यदि आप इन बीजाणुओं को एक कपास झाड़ू में पेश करते हैं, जब ल्यूकोसाइट्स उन्हें अवशोषित नहीं कर सकते हैं या इसे बहुत देरी से करते हैं, तो बीजाणुओं को अंकुरित होने का समय मिलता है और बीमारी और मृत्यु होती है। यदि रोगाणुओं की संस्कृति को लैक्टिक एसिड के साथ पेश किया जाता है, जिसका ल्यूकोसाइट्स पर नकारात्मक केमोटॉक्सिक प्रभाव होता है, तो संस्कृति की ऐसी खुराक से मृत्यु होगी जो बिना एसिड के जानवरों द्वारा आसानी से सहन की जाती है। दूसरी ओर, ल्यूकोसाइट्स की संख्या में वृद्धि, विशेष रूप से संक्रमण के स्थल पर, निस्संदेह शरीर की प्रतिरोधक क्षमता को बढ़ाती है। यह गैर-विशिष्ट एजेंटों के कारण भी हो सकता है। इसमें कोई संदेह नहीं है कि ल्यूकोसाइटोसिस निरर्थक प्रतिरक्षा के कारकों में से एक है, जिसे तथाकथित प्रोटीन थेरेपी में पुन: पेश किया जाता है।
डिप्थीरिया और टेटनस विष दोनों के संबंध में ल्यूकोसाइट्स द्वारा विषाक्त पदार्थों के बंधन (सोखना) को अलग-अलग लेखकों द्वारा बार-बार वर्णित किया गया है, हालांकि प्राप्त परिणाम बल्कि विरोधाभासी थे।
फैगोसाइटोसिस प्रतिक्रिया का सभी संक्रामक रोगों में एक सुरक्षात्मक कार्य नहीं होता है। उदाहरण के लिए, इन्फ्लूएंजा बेसिलस के कारण होने वाले मेनिन्जाइटिस के साथ, बाद वाला अवशोषित हो जाता है, लेकिन फागोसाइट्स द्वारा नष्ट नहीं होता है जो इसे एंटीबॉडी की कार्रवाई से बचाता है। लेकिन बैक्टीरियल संक्रमणों के भारी बहुमत में, फागोसाइटोसिस एक तरह से या किसी अन्य में सुरक्षात्मक कार्य करता है। वायरल संक्रमण में फागोसाइटोसिस का एक अलग अर्थ है। फैगोसाइटिक प्रतिक्रिया सभी संक्रामक प्रक्रियाओं में समान नहीं है। यह पूरी तरह से I.I के विचारों से मेल खाता है। मेचनिकोव, जिन्होंने विभिन्न जानवरों और विभिन्न रोगाणुओं में फागोसाइटिक प्रतिक्रियाओं का अध्ययन करते हुए, अपने विकासवादी विकास में इस प्रतिक्रिया के विभिन्न रूपों की स्थापना की। स्टैफिलोकोकस को ल्यूकोसाइट्स द्वारा कब्जा कर लिया जाता है और मार दिया जाता है, गोनोकोकस उनके द्वारा फागोसाइटोज किया जाता है लेकिन ल्यूकोसाइट्स के अंदर जीवित रहता है, और अंत में, कुछ वायरस ल्यूकोसाइट्स द्वारा फागोसाइटोज नहीं होते हैं। यह संभव है कि ये तीन उदाहरण विकासवादी विकास में तीन अलग-अलग चरणों का प्रतिनिधित्व करते हैं। फागोसाइटिक प्रतिक्रिया।
प्रतिरक्षा का विनियमन।
प्रतिरक्षा प्रतिक्रिया की तीव्रता काफी हद तक तंत्रिका और अंतःस्रावी तंत्र की स्थिति से निर्धारित होती है। यह स्थापित किया गया है कि विभिन्न सबकोर्टिकल संरचनाओं (थैलेमस, हाइपोथैलेमस, ग्रे ट्यूबरकल) की जलन एंटीजन की शुरूआत के लिए प्रतिरक्षा प्रतिक्रिया में वृद्धि और कमी दोनों के साथ हो सकती है। यह दिखाया गया है कि स्वायत्त (वानस्पतिक) तंत्रिका तंत्र के सहानुभूति विभाजन की उत्तेजना, साथ ही एड्रेनालाईन का प्रशासन, फागोसाइटोसिस और प्रतिरक्षा प्रतिक्रिया की तीव्रता को बढ़ाता है। स्वायत्त तंत्रिका तंत्र के पैरासिम्पेथेटिक डिवीजन के स्वर में वृद्धि से विपरीत प्रतिक्रियाएं होती हैं।
तनाव और अवसाद प्रतिरक्षा प्रणाली को दबाते हैं, जो न केवल विभिन्न रोगों के लिए संवेदनशीलता में वृद्धि के साथ है, बल्कि घातक नवोप्लाज्म के विकास के लिए अनुकूल परिस्थितियों का निर्माण भी करता है।
हाल के वर्षों में, यह स्थापित किया गया है कि पिट्यूटरी और पीनियल ग्रंथियां "साइटोमेडिन्स" नामक विशेष पेप्टाइड बायोरेगुलेटर की मदद से थाइमस की गतिविधि को नियंत्रित करती हैं।
प्रतिरक्षा नियामक प्रणाली।
हाल ही में, यह सुझाव दिया गया है कि दो नियामक प्रणालियां (नर्वस और ह्यूमरल) नहीं हैं, लेकिन तीन (नर्वस, ह्यूमरल और इम्यून) हैं। इम्यूनोकम्पेटेंट कोशिकाएं मॉर्फोजेनेसिस में हस्तक्षेप करने में सक्षम हैं, साथ ही साथ शारीरिक कार्यों के पाठ्यक्रम को नियंत्रित करती हैं। शारीरिक कार्यों के नियमन में एक विशेष रूप से महत्वपूर्ण भूमिका इंटरल्यूकिन्स की है, जो "सभी अवसरों के लिए अणुओं का परिवार" हैं, क्योंकि शरीर में होने वाली शारीरिक प्रक्रिया बिल्कुल हस्तक्षेप करती है।
प्रतिरक्षा प्रणाली होमियोस्टैसिस का नियामक है। यह कार्य सक्रिय एंजाइमों, रक्त जमावट कारकों और अतिरिक्त हार्मोन को बांधने वाले स्वप्रतिपिंडों के उत्पादन के कारण किया जाता है।
इम्यूनोलॉजिकल प्रतिक्रिया, एक ओर, हास्य का एक अभिन्न अंग है, क्योंकि अधिकांश शारीरिक और जैव रासायनिक प्रक्रियाएं हास्य मध्यस्थों की प्रत्यक्ष भागीदारी के साथ की जाती हैं। हालांकि, अक्सर प्रतिरक्षात्मक प्रतिक्रिया को लक्षित किया जाता है, इस प्रकार एक नर्वस जैसा दिखता है। लिम्फोसाइट्स और मोनोसाइट्स, साथ ही प्रतिरक्षा प्रतिक्रिया में शामिल अन्य कोशिकाएं, हास्य मध्यस्थ को सीधे लक्ष्य अंग में दान करती हैं। इसलिए इम्यूनोलॉजिकल रेगुलेशन को सेल्युलर-ह्यूमरल कहने का प्रस्ताव।
प्रतिरक्षा प्रणाली के विनियामक कार्यों को ध्यान में रखते हुए विभिन्न विशिष्टताओं के डॉक्टरों को नैदानिक चिकित्सा की कई समस्याओं को हल करने के लिए एक नया दृष्टिकोण अपनाने की अनुमति मिलती है।
लसीका ऊतक का बैरियर कार्य।एक सूक्ष्म जीव जो त्वचा और श्लेष्मा अवरोधों में प्रवेश कर गया है। अधिकांश मामलों में, यह लिम्फ नोड्स में प्रवेश करता है। हेमोलाइटिक स्ट्रेप्टोकोकस, लसीका वाहिका में लसीका नोड की ओर जाता है, इस नोड में एक महत्वपूर्ण मात्रा में रहता है और लगभग बाहर जाने वाले पोत में नहीं पाया जाता है। इसी तरह के परिणाम कई अन्य रोगाणुओं के साथ प्रयोगों में प्राप्त किए गए थे जब उन्हें त्वचा के नीचे पेश किया गया था, फेफड़ों में और आंतों में। लेकिन जब बैक्टीरिया को पेरिटोनियल कैविटी में पेश किया गया, तो वे बहुत जल्दी रक्त प्रवाह में दिखाई दिए। त्वचा के नीचे पेश किए गए शरीर में बैक्टीरिया के फैलाव पर अवलोकन से पता चलता है कि लिम्फ नोड्स एक बाधा है जो शरीर में बैक्टीरिया के प्रवेश को रोकता है। टीकाकरण के दौरान लिम्फ नोड्स का बाधा कार्य बढ़ जाता है। इस मुद्दे का विस्तार से वीएम बर्मन (1948) और अन्य शोधकर्ताओं द्वारा अध्ययन किया गया था। उन्होंने पाया कि जब प्रायोगिक जानवर टाइफाइड बुखार, पेचिश, तपेदिक, ब्रुसेलोसिस और हैजा से संक्रमित होते हैं, तो लिम्फ नोड्स , संवहनी एंडोथेलियम और रेटिकुलो कोशिकाएं - शरीर में बैक्टीरिया के प्रवेश को रोकने के लिए एंडोथेलियल सिस्टम में प्रतिरक्षा शरीर में एक स्पष्ट क्षमता होती है। शरीर में रोगाणुओं के प्रवेश को रोकने के लिए लसीका ऊतक की क्षमता को बैरियर-फिक्सिंग फ़ंक्शन कहा जाता है। कुछ बैक्टीरिया जो लिम्फ नोड्स में रहते हैं उनमें गुणा हो जाते हैं। तो, एच.एच. प्लैनल्स (1950) की टिप्पणियों से पता चला है कि टाइफाइड के रोगाणु लिम्फ नोड्स में तेजी से गुणा करते हैं, लिम्फोसाइटों में प्रवेश करते हैं और उनके नाभिक में कॉलोनियां बनाते हैं। लिम्फ नोड्स का अवरोधक कार्य कुछ हद तक हमलावर बैक्टीरिया के कारण होने वाली भड़काऊ प्रक्रिया से जुड़ा होता है।
इम्यूनोलॉजिकल रिएक्टिविटी -विभिन्न कारकों के साथ-साथ उम्र के साथ-साथ एंटीजेनिक प्रजनन परिवर्तनों का जवाब देने की शरीर की क्षमता। नवजात जानवरों में तेजी से कम प्रतिरक्षात्मक प्रतिक्रिया होती है, जो कई संक्रमणों के लिए उनकी बढ़ती संवेदनशीलता की व्याख्या करती है। जीव की प्रतिक्रियाशीलता में परिवर्तन, जो एंटीबॉडी बनाने की क्षमता के संबंध में उम्र के साथ होता है, आई. आई. मेचनिकोव द्वारा नोट किया गया था।
1897 में, उन्होंने देखा कि वयस्क मगरमच्छ युवा लोगों की तुलना में बहुत अधिक मात्रा में टेटनिक एंटीटॉक्सिन का उत्पादन करते हैं। इसके बाद, कई लेखकों ने नवजात जानवरों में एंटीबॉडी की अनुपस्थिति या उनके गठन में तेज कमी और वयस्कों में इस क्षमता में वृद्धि देखी। इसलिए, उदाहरण के लिए, उम्र के साथ खरगोशों में, कई एंटीजन (घोड़े के सीरम, भेड़ एरिथ्रोसाइट्स, टाइफाइड वैक्सीन) के खिलाफ एंटीबॉडी के उत्पादन में वृद्धि होती है।
वयस्क जानवरों में टीकाकरण के लिए एक अधिक स्पष्ट क्षमता चूहों पर ट्रिपैनोसोम के साथ, एन्सेफेलोमाइलाइटिस और रेबीज वायरस वाले चूहों पर और इसी तरह के अन्य मामलों में भी दिखाई गई थी। इसी समय, यह देखा गया कि मध्यम आयु वर्ग के खरगोशों की तुलना में पुराने खरगोशों में एंटीबॉडी का उत्पादन करने की क्षमता कम स्पष्ट है। नवजात शिशुओं में फैगोसाइटोसिस की क्षमता भी तेजी से कम हो जाती है। जाहिर है, इन सभी मामलों में, नवजात कोशिकाओं की जैव रसायन से जुड़ी एक प्राथमिक कम प्रतिक्रियाशीलता है। भ्रूण के जीवन में एक और भी अधिक स्पष्ट घटी हुई प्रतिक्रियाशीलता होती है। एक विकासशील चिक भ्रूण में, एंटीबॉडी या तो बिल्कुल नहीं बनते हैं या एक छोटे अनुमापांक में बनते हैं। इसी समय, कई संक्रामक एजेंट भ्रूण में गुणा करते हैं, जिसके लिए वयस्क जानवर अतिसंवेदनशील नहीं होते हैं। यह गुणा इतना तीव्र है कि चिकन भ्रूण व्यापक रूप से वायरस संस्कृतियों के लिए उपयोग किया जाता है। चिकन भ्रूण में कई बैक्टीरिया भी गुणा करते हैं। हाल ही में, प्रायोगिक सामग्री जमा हुई है जो भ्रूण के जीवन में एक विशेष प्रतिरक्षात्मक प्रतिक्रिया की उपस्थिति का संकेत देती है।
प्रतिरक्षा प्रणाली की पैथोलॉजी।
लंबे समय तक यह स्थापित माना जाता था कि शरीर अपने प्रतिजनों के प्रति एंटीबॉडी के गठन के साथ प्रतिक्रिया नहीं करता है। एर्लिच ने इसे एक प्रकार का "आत्म-विषाक्तता का डर" माना।
हालाँकि, धीरे-धीरे तथ्य जमा हो रहे थे, यह दर्शाता है कि कुछ मामलों में शरीर अपने स्वयं के प्रतिजनों के लिए एंटीबॉडी का उत्पादन कर सकता है। इसी तरह की घटना तब होती है जब शरीर के अपने प्रतिजन किसी रोग प्रक्रिया द्वारा विकृत हो जाते हैं और इस तरह के परिवर्तित रूप में उन ऊतकों में प्रवेश करते हैं जो एंटीबॉडी का उत्पादन करते हैं, या यदि ये ऊतक ऐसे प्रतिजन प्राप्त करते हैं जो प्राकृतिक परिस्थितियों में कभी भी रक्तप्रवाह में प्रवेश नहीं करते हैं और उनकी प्रजाति विशिष्टता कम होती है (के लिए) उदाहरण के लिए, प्रोटीन लेंस)। इस तरह के स्वप्रतिरक्षी अपने स्वयं के जीव में एक स्वप्रतिरक्षी प्रक्रिया का कारण बनते हैं, जिससे उत्पन्न होने वाली स्वप्रतिपिंडों के बीच प्रतिक्रिया के कारण कई रोग स्थितियों का उदय होता है, कभी-कभी बहुत गंभीर।
इम्यूनोलॉजिकल प्रक्रियाएं आमतौर पर शरीर के आंतरिक वातावरण की सापेक्ष स्थिरता को बहाल करने के उद्देश्य से होती हैं, जिसके साथ उनका सुरक्षात्मक कार्य जुड़ा होता है। वर्णित मामलों में, इन प्रक्रियाओं से आंतरिक वातावरण की स्थिरता का उल्लंघन होता है, जो एक रोग संबंधी प्रकृति की कई नैदानिक घटनाओं द्वारा व्यक्त किया जाता है। इसलिए, इम्यूनोलॉजिकल प्रक्रियाओं के कारण होने वाले ऐसे सभी विकारों को सामान्य अवधारणा द्वारा एकजुट किया जा सकता है प्रतिरक्षा की पैथोलॉजी। वर्तमान में, कई बीमारियों का अध्ययन किया गया है, जिनमें से घटना एक ऑटोइम्यूनाइजेशन प्रक्रिया से जुड़ी या जुड़ी हुई है। इनमें शामिल हैं: अधिग्रहित हेमोलिटिक एनीमिया, शारीरिक पीलिया, आमवाती हृदय रोग और अन्य रोग। इनमें से कुछ बीमारियों से उत्पन्न होने वाली एंटीबॉडी का अपेक्षाकृत अच्छी तरह से अध्ययन किया गया है।
एड्स
आज की मानवता की सबसे महत्वपूर्ण और तीव्र समस्याओं में से एक सभ्यता के रोग (कैंसर, एड्स, सिफलिस, नशा और शराब, आदि) हैं। डॉक्टरों ने उनमें से कई को लंबे समय तक और जिद्दी रूप से लड़ा, लेकिन, दुर्भाग्य से, उन्हें अभी भी मारक नहीं मिला है। ऐसी ही एक बीमारी है एड्स: एक्वायर्ड इम्यून डेफिसिएंसी सिंड्रोम।
इसे हमारे युग का प्लेग कहा जाता है। यह ह्यूमन इम्युनोडेफिशिएंसी वायरस (एचआईवी) के कारण होता है, जो शरीर की रक्षा प्रणाली पर हमला करता है।
एड्स की महामारी लगभग 20 वर्षों से चली आ रही है: ऐसा माना जाता है कि एचआईवी संक्रमण के पहले सामूहिक मामले 1970 के दशक के अंत में सामने आए थे। हालांकि एचआईवी को तब से दुनिया के किसी भी वायरस से बेहतर समझा जा चुका है, लाखों लोग एड्स से मर रहे हैं और लाखों लोग एचआईवी संक्रमण का निदान कर रहे हैं। एड्स शीर्ष पांच घातक बीमारियों में से एक है जो हमारे ग्रह पर सबसे बड़ी संख्या में जीवन का दावा करती है। महामारी बढ़ती जा रही है, अधिक से अधिक क्षेत्रों को कवर कर रही है। समाजशास्त्रीय अध्ययनों से पता चला है कि 20 मिलियन से अधिक लोग वायरस से मर गए (20 वर्षों के शोध में), 40 मिलियन इस भयानक निदान के साथ रहते हैं।
हाल के वर्षों में, न केवल एचआईवी और एड्स के बारे में ज्ञान बदल गया है, बल्कि इस समस्या के प्रति समाज का दृष्टिकोण भी बदल गया है। इस बीमारी की अज्ञानता और अंधे डर से, मानवता वायरस पर विज्ञान की आंशिक जीत और सामान्य ज्ञान - नाडिस्टेरिया और स्पाइडोफोबिया पर आ गई है।
इम्युनोडेफिशिएंसी वायरस की उत्पत्ति
मानव शरीर में प्रतिरक्षा है - संक्रामक एजेंटों के खिलाफ निर्देशित कई सुरक्षात्मक प्रतिक्रियाएं। प्रतिरक्षा प्रणाली की मुख्य कोशिकाएं माइक्रोफेज (ग्रीक में "फेज" - खाने) और लिम्फोसाइट्स हैं। प्रतिरक्षा प्रणाली इस तरह काम करती है: यह शरीर से बाहर की हर चीज को पहचानती है और हटाती है - रोगाणु, वायरस, कवक और यहां तक कि अपनी खुद की कोशिकाएं और ऊतक, अगर वे पर्यावरणीय कारकों ("प्रतिरक्षा" - किसी भी चीज से मुक्त) के प्रभाव में विदेशी हो जाते हैं। . प्रतिरक्षा प्रणाली बहुत कुशल और संसाधनपूर्ण है। हालाँकि, यह सभी मामलों में शरीर की मदद नहीं कर सकता है। एक वायरस जिससे प्रतिरक्षा प्रणाली नहीं लड़ सकती, वह है ह्यूमन इम्युनोडेफिशिएंसी वायरस।
इससे पहले कि आप समझें कि एचआईवी वायरस कैसे काम करता है, आपको रक्त के बारे में थोड़ी बात करने की आवश्यकता है। रक्त एक तरल संयोजी ऊतक है जिसमें प्लाज्मा और अलग-अलग आकार के तत्व होते हैं: लाल रक्त कोशिकाएं, एरिथ्रोसाइट्स, सफेद रक्त कोशिकाएं, ल्यूकोसाइट्स और प्लेटलेट्स, प्लेटलेट्स। शरीर में, रक्त विभिन्न कार्य करता है: श्वसन, पोषण, उत्सर्जन, थर्मोरेगुलेटरी, सुरक्षात्मक, ह्यूमरल। तथाकथित सेलुलर प्रतिरक्षा टी-लिम्फोसाइटों द्वारा प्रदान की जाती है। उनकी विविधता - टी-हत्यारे ("हत्यारे") उन कोशिकाओं को नष्ट करने में सक्षम हैं जिनके खिलाफ एंटीबॉडी का उत्पादन किया गया था, या विदेशी कोशिकाओं को मार दिया गया था। प्रतिरक्षा की जटिल विविध प्रतिक्रियाओं को दो और किस्मों द्वारा नियंत्रित किया जाता है - टी-लिम्फोसाइट्स: टी-हेल्पर्स ("हेल्पर्स"), जिसे टी 4 और टी-सप्रेसर्स ("उत्पीड़क") भी कहा जाता है, अन्यथा टी 8 के रूप में जाना जाता है। पूर्व सेलुलर प्रतिरक्षा की प्रतिक्रियाओं को उत्तेजित करते हैं, बाद वाले उन्हें रोकते हैं।
तो एचआईवी एड्स का कारण है। हालांकि एचआईवी संक्रमण के कुछ पहलुओं को अभी तक पूरी तरह से समझा नहीं गया है, जैसे कि वायरस प्रतिरक्षा प्रणाली को कैसे नष्ट कर देता है, और क्यों एचआईवी वाले कुछ लोग लंबे समय तक पूरी तरह से स्वस्थ रहते हैं, फिर भी, एचआईवी मानव में सबसे गहराई से अध्ययन किए गए वायरस में से एक है। इतिहास। इम्युनोडेफिशिएंसी वायरस लेंटिवायरस ("धीमे वायरस") से संबंधित है, जो रेट्रोवायरस का एक उपसमूह है। इन वायरस को धीमा कहा जाता है क्योंकि ऊष्मायन अवधि महीनों और वर्षों में मापी जाती है, और क्योंकि बीमारी का एक लंबा कोर्स होता है।
एक बार शरीर में, एचआईवी कुछ रक्त कोशिकाओं पर हमला करता है: टी-लिम्फोसाइट्स "सहायक" होते हैं। इन लिम्फोसाइटों की सतह पर सीडी-4 अणु होते हैं, इसलिए उन्हें टी-4 लिम्फोसाइट्स और सीडी-4 लिम्फोसाइट्स (या सीडी-4 कोशिकाएं) भी कहा जाता है। ).
वायरस की संरचना आदिम है: फैटी अणुओं की एक दोहरी परत का एक खोल, ग्लाइकोप्रोटीन "मशरूम" इससे बाहर निकलता है, अंदर दो आरएनए श्रृंखलाएं होती हैं जिनमें वायरस के आनुवंशिक कार्यक्रम होते हैं, और प्रोटीन - रिवर्स ट्रांसक्रिपटेस, इंटीग्रेज और प्रोटीज . इस अल्प सामान के अलावा, वायरस को कुछ भी नहीं चाहिए: यह मेजबान सेल को पुनरुत्पादित करने के लिए उपयोग करता है।
अधिकांश स्वाभाविक रूप से होने वाली कोशिकाओं और वायरस की आनुवंशिक जानकारी डीएनए के रूप में एन्कोडेड होती है। एचआईवी में, यह आरएनए में एन्कोड किया गया है। वायरस को अपनी आनुवंशिक जानकारी को होस्ट सेल के लिए समझ में आने वाली भाषा में अनुवाद करने की आवश्यकता होती है, यानी अपने आरएनए को डीएनए में अनुवाद करना। ऐसा करने के लिए, वायरस रिवर्स ट्रांसक्रिपटेस नामक एंजाइम का उपयोग करता है, जो आरएनए को डीएनए में परिवर्तित करता है। इस तरह के परिवर्तन के बाद, मेजबान सेल वायरस के डीएनए को "देशी" के रूप में स्वीकार करता है। यह प्रक्रिया आमतौर पर संक्रमण के 12 घंटे के भीतर होती है।
वायरस को पनडुब्बी रोधी खदान के समान चित्रित किया गया है। इसकी सतह पर "मशरूम" ग्लाइकोप्रोटीन अणुओं से बने होते हैं। "टोपी" - तीन-चार GP120 अणु, और "पैर" - 3-4 GP41 अणु।
दुनिया में एचआईवी से संक्रमित लोगों की संख्या:
ऑस्ट्रेलिया 12,000 उत्तरी अमेरिका 920,000 दक्षिण अमेरिका 1.3 मिलियन यूरेशिया 7.4 मिलियन अफ्रीका 23.5 मिलियन कुल 33.6 मिलियन
आपको एड्स कैसे हो सकता है?
1. एक अंतःशिरा इंजेक्शन सुई के माध्यम से। उदाहरण के लिए, जब एक ही सुई का उपयोग कई लोगों द्वारा किया जाता है जो दवाओं का इंजेक्शन लगाते हैं। हर बार एक अंतःशिरा इंजेक्शन के बाद, सुई में थोड़ा सा रक्त होता है - इतना कम कि इसे हमेशा देखा नहीं जा सकता है, लेकिन बीमारी को अगले व्यक्ति तक पहुँचाने के लिए पर्याप्त है जो सुई को अपनी नस में इंजेक्ट करता है।
2. रक्त आधान के साथ। यह उन दुर्लभ मामलों में होता है जब इस उद्देश्य के लिए एचआईवी संक्रमित लोगों के अप्रयुक्त रक्त का उपयोग किया जाता है। रक्त में वायरस की उपस्थिति निर्धारित करने के लिए अब पर्याप्त विश्वसनीय परीक्षण हैं।
3. मां से बच्चे तक एक संक्रमित गर्भवती महिला अपने अजन्मे बच्चे को संक्रमित कर सकती है क्योंकि वे एक सामान्य संचार प्रणाली साझा करते हैं। हालाँकि, अब ऐसा बहुत कम ही होता है, क्योंकि सभी गर्भवती महिलाओं को एचआईवी के लिए परीक्षण करने की आवश्यकता होती है।
एड्स आप संक्रमित नहीं हो सकते द्वारा:
छूना और हाथ मिलाना;
चुंबन (यदि दोनों के मुंह में खुले घाव नहीं हैं);
मच्छर काटना; खांसने और छींकने पर;
टॉयलेट सीट, बर्तन और अन्य चीजें।
एचआईवी से संक्रमित होने पर, अधिकांश लोग किसी संवेदना का अनुभव नहीं करते हैं। कभी-कभी संक्रमण के कुछ सप्ताह बाद, फ्लू जैसी स्थिति विकसित हो जाती है (बुखार, त्वचा पर चकत्ते, लिम्फ नोड्स में सूजन, दस्त)।
एचआईवी संक्रमण के कुछ लक्षण: लगातार सूखी खांसी; लंबे समय तक, तीन महीने से अधिक, अज्ञात कारण का बुखार; रात में पसीना आना; नाटकीय वजन घटाने; लगातार सिरदर्द, कमजोरी, स्मृति हानि और कार्य क्षमता; मौखिक श्लेष्म की सूजन, सफेद पट्टिका, अल्सर; अस्पष्टीकृत घटी हुई दृष्टि और अंधापन।
हालांकि, अगर किसी व्यक्ति में यहां बताए गए लक्षणों में से कोई भी लक्षण है, तो इसका मतलब यह बिल्कुल नहीं है कि उसे एड्स है। ये लक्षण अन्य बीमारियों के कारण हो सकते हैं जो एचआईवी संक्रमण से संबंधित नहीं हैं, इसलिए आपको हमेशा परीक्षण करवाना चाहिए और बीमारी के कारण का पता लगाना चाहिए। किसी भी मामले में, डॉक्टर को देखना एक उचित निर्णय होगा।
अब तक, एड्स मानव जाति की सबसे खतरनाक बीमारियों में से एक है। क्या इस रोग को सबसे कपटी में से एक बनाता है? कि डॉक्टरों और वैज्ञानिकों को अभी तक कोई मारक नहीं मिला है। उनके अब तक के सभी प्रयास व्यर्थ गए हैं। लेकिन दुनिया के डॉक्टरों और वैज्ञानिकों के श्रमसाध्य काम के लिए धन्यवाद, ऐसी दवाएं सामने आई हैं जो एक संक्रमित व्यक्ति के जीवन को लम्बा करने में मदद करती हैं।
आज, लगभग किसी भी किताबों की दुकान में आप साहित्य खरीद सकते हैं, जहां एक साधारण भाषा में, न केवल इस बीमारी के अध्ययन में एक विशेषज्ञ के लिए समझ में आता है, बल्कि हर व्यक्ति को इस भयानक बीमारी के बारे में, इसके विकास और परिणामों के बारे में स्पष्टीकरण दिया जाता है। लेकिन ज्यादातर लोग या तो डॉक्टरों की सलाह नहीं मानते या मानते हैं कि उनके साथ ऐसा कभी नहीं होगा। शायद यह किसी के स्वास्थ्य के प्रति इतना तुच्छ रवैया है, प्राथमिक सावधानियों का पालन करने में विफलता ने इस तथ्य को जन्म दिया है कि एड्स खतरनाक रूप से ताकत हासिल कर रहा है और सबसे आम बीमारियों में से एक है जिसे मानव जाति ने कभी जाना है।
मुझे ऐसा लगता है कि एड्स को हराना संभव है, लेकिन इसके लिए एक और अधिक प्राचीन बीमारी पर काबू पाना आवश्यक है। हमारा अज्ञान।
साहित्य
1. बकुलेव ए.एन., ब्रूसिलोव्स्की एल.वाईए, टिमकोव वी.डी., शाबानोव ए.एन.
बिग मेडिकल एनसाइक्लोपीडिया एम।, 1959।
2. Khlyabich G., Zhdanov V. AIDS: जानने और लड़ने के लिए। "चिकित्सा
3. कुदरीवत्सेवा ई।, 1981 से एड्स ... "विज्ञान और जीवन" नंबर 10, 1987
4. वीएम पोक्रोव्स्की वीएम, कोरोटको जीएफ, ह्यूमन फिजियोलॉजी एम,
5. वेबसाइट www.mednovosti.ru का डेटा
951 0
शरीर की विभिन्न कोशिकाओं की साइटोटॉक्सिक क्षमता की संभावनाओं की चर्चा को समाप्त करते हुए एक और प्रकार की कोशिकाओं को नजरअंदाज नहीं किया जा सकता है।
हम प्लेटलेट्स - कोशिकाओं के बारे में बात कर रहे हैं, जो आम तौर पर स्वीकृत अवधारणाओं के अनुसार, आज प्रतिरक्षा प्रणाली की कोशिकाओं के रूप में नहीं मानी जाती हैं।
फिर भी, उनके पास विभिन्न ट्यूमर कोशिकाओं के खिलाफ साइटोटॉक्सिक गतिविधि है, लेकिन लक्ष्य कोशिकाओं को छांटने की उनकी क्षमता का सबसे कम अध्ययन किया गया है।
ट्यूमर प्रक्रिया में प्लेटलेट्स की भूमिका का अध्ययन करने में रुचि न केवल ट्यूमर लक्ष्यों के विश्लेषण में उनकी भागीदारी के कारण है, बल्कि कम से कम कई पहलुओं पर चर्चा की जा सकती है।
पहला विभिन्न ट्यूमर पर साइटोटॉक्सिक प्रभाव है, दूसरा प्रतिरक्षा प्रणाली की ऐसी कोशिकाओं के कार्यों के कार्यान्वयन में भागीदारी है प्राकृतिक हत्यारे (एनके), मोनोसाइट्स, कुछ टी-लिम्फोसाइट्स (प्रसार, प्रवासन, आसंजन, आदि), और तीसरा - ट्यूमर कोशिकाओं के साथ प्लेटलेट्स की बातचीत।
पहले से बने विचारों के दृष्टिकोण से, बाद वाला पहलू सीधे एंटीट्यूमर इम्यूनोलॉजिकल प्रोटेक्शन से संबंधित नहीं है, लेकिन यह माइक्रोएन्वायरमेंट की विशेषताओं को समझने के लिए महत्वपूर्ण है, और इसके परिणामस्वरूप, प्रतिरक्षा प्रणाली की कोशिकाओं के कार्यों के कार्यान्वयन के लिए।
प्लेटलेट्स के सामान्य और बल्कि जाने-माने गुणों पर ध्यान दिए बिना, उन बातों पर ध्यान देना उचित लगता है जो चर्चा के तहत मुद्दे के पहलू में महत्वपूर्ण हैं।
हाल ही में, प्लेटलेट्स द्वारा विभिन्न संरचनाओं की अभिव्यक्ति के बारे में बहुत सारी जानकारी सामने आई है, जो लगातार अधिक से अधिक होती जा रही हैं। ट्यूमर प्रक्रिया में प्लेटलेट्स की भूमिका को समझने के लिए, निम्नलिखित संरचनाओं की अभिव्यक्ति का विशेष महत्व है।
सबसे पहले, इस बात पर जोर दिया जाना चाहिए कि प्लेटलेट्स में कई अणु होते हैं जो उन्हें आसंजन के पर्याप्त अवसर प्रदान करते हैं। प्लेटलेट्स के चिपकने वाले गुणों में विभिन्न इंटीग्रिन महत्वपूर्ण भूमिका निभाते हैं, विशेष रूप से, इंटीग्रिन β1-चेन एक ट्रांसमेम्ब्रेन ग्लाइकोप्रोटीन (CD29) है, जो VICAM-1 और MAaCAM-1 को बाँधने में सक्षम है, फ़ाइब्रोनेक्टिन, लेमिनिन के साथ हेटेरोडिमर्स बनाता है। और कोलेजन β1-श्रृंखला।
CD41 - ग्लाइकोप्रोटीन लिब (GPIIb) की भूमिका कोई कम महत्वपूर्ण नहीं है, जो कि CD41-CD61 कॉम्प्लेक्स की एक सबयूनिट है - एक कैल्शियम-निर्भर हेटेरोडिमर; CD41, साथ ही CD42a, CD42b, CD42c की अभिव्यक्ति की विशेषता यह है कि वे विशेष रूप से प्लेटलेट्स और मेगाकारियोसाइट्स पर दिखाई देते हैं। प्लेटलेट्स के चिपकने वाले गुण इंटरसेलुलर आसंजन अणु - ICAM-2 (CD102) के साथ-साथ संभावित आसंजन अणु - CD147 की अभिव्यक्ति से भी जुड़े हैं।
प्लेटलेट्स के चिपकने वाले गुणों में एक महत्वपूर्ण स्थान पी-सेलेक्टिन (CD62) द्वारा कब्जा कर लिया जाता है - प्लेटलेट्स और एंडोथेलियल कोशिकाओं का एक झिल्ली-बाध्य प्रोटीन, जो मध्यस्थों (हिस्टामाइन, पूरक घटकों, आदि) के प्रभाव में जुटाया जाता है; इसके लिगेंड सियालिल-लुईस एक्स और सियालिल-लुईस ए अणु हैं।
प्लेटलेट्स के कामकाज में, प्लेटलेट ग्रोथ फैक्टर रिसेप्टर (CD140a) की अभिव्यक्ति एक महत्वपूर्ण स्थान रखती है, जो इन कोशिकाओं के प्रसार और प्रवासन में शामिल है। आईजीई के लिए एफसी रिसेप्टर की अभिव्यक्ति की भूमिका कम महत्वपूर्ण नहीं है।
कुछ प्लेटलेट-व्यक्त सतह संरचनाएं सीधे प्रतिरक्षा प्रणाली की कोशिकाओं के कार्यों के नियमन से संबंधित हैं। प्लेटलेट्स की सतह पर एक झिल्लीदार ग्लाइकोप्रोटीन होता है, जो थाइमोसाइट्स और थाइमिक उपकला कोशिकाओं के आसंजन में शामिल होता है।
CD226 जैसे एक अणु, एक ग्लाइकोप्रोटीन, न केवल प्लेटलेट्स द्वारा व्यक्त किया जाता है, बल्कि एनके, मोनोसाइट्स और कुछ टी-लिम्फोसाइट्स द्वारा भी व्यक्त किया जाता है, जो टी-लिम्फोसाइट्स के अन्य कोशिकाओं के आसंजन में भाग लेते हैं जिनके पास संबंधित लिगैंड होता है।
प्लेटलेट्स और प्रतिरक्षा प्रणाली की कुछ कोशिकाओं द्वारा व्यक्त सामान्य एंटीजन में 220-240 kDa के आणविक भार के साथ CD245 एंटीजन शामिल हैं, जो मोनोसाइट्स, लिम्फोसाइट्स, ग्रैन्यूलोसाइट्स द्वारा भी व्यक्त किया जाता है, जो सिग्नल ट्रांसडक्शन और T- के सह-उत्तेजना में शामिल होता है। लिम्फोसाइट्स और प्राकृतिक हत्यारे।
अंत में, यह ध्यान दिया जाना चाहिए कि CD36 मेहतर रिसेप्टर परिवार का भी सदस्य है, जो मोनोसाइट्स और ट्यूमर कोशिकाओं, मान्यता और फागोसाइटोसिस के साथ प्लेटलेट्स की बातचीत में शामिल है।
प्लेटलेट्स CD114, एक प्रकार I ट्रांसमेम्ब्रेन अणु (प्रकार I साइटोकिन रिसेप्टर परिवार का एक सदस्य) को भी व्यक्त करते हैं, जो कार्यों के नियमन और लिम्फोइड कोशिकाओं के प्रसार में शामिल है।
प्लेटलेट्स के पास कोलेजन के साथ बातचीत करने के महान अवसर हैं, जिन रिसेप्टर्स के लिए वे व्यक्त करते हैं, जो बाह्य मैट्रिक्स के साथ उनकी बातचीत में योगदान देता है, जिसमें मुख्य रूप से कोलेजन प्रकार I, II और III होते हैं; प्लेटलेट ग्लाइकोप्रोटीन lb और FVIII/vWF इस प्रक्रिया में शामिल हैं, एंडोथेलियम से लगाव के लिए बाद की आवश्यकता होती है। प्लेटलेट्स HPA-1a एंटीजन को व्यक्त करते हैं।
यह भी बहुत महत्वपूर्ण है कि प्लेटलेट्स हिस्टामाइन और साइटोक्रोम P450 की क्रिया के तहत दूसरे संदेशवाहक के रूप में कार्य करें।
प्लेटलेट्स प्रतिरक्षा प्रणाली की कई कोशिकाओं (टी-लिम्फोसाइट्स, विभिन्न एंटीजन-प्रेजेंटिंग सेल, आदि) पर कुछ नियामक प्रभाव डालने में सक्षम हैं। यह प्रभाव मुख्य रूप से प्लेटलेट ग्रेन्युल उत्पादों की कार्रवाई के साथ-साथ प्लेटलेट फैक्टर 4 (PF4), RANTES, उनके द्वारा उत्पादित CD40L के घुलनशील रूप के कारण होता है।
प्लेटलेट्स की विशेषताओं पर डेटा, जो पूर्ण रूप से प्रस्तुत किए जाने से बहुत दूर हैं, फिर भी इसमें कोई संदेह नहीं है कि उन्हें विभिन्न प्रक्रियाओं में शामिल किया जा सकता है जो इन कोशिकाओं के बारे में विचारों के ढांचे से बहुत आगे जाते हैं।
तालिका में। 11 प्लेटलेट्स की सामान्य विशेषताओं को दर्शाता है।
तालिका 11. प्लेटलेट्स की सामान्य विशेषताएं
प्लेटलेट्स का साइटोटोक्सिक प्रभाव
ईोसिनोफिल्स और बेसोफिल्स की तरह प्लेटलेट्स की साइटोटॉक्सिसिटी, पहली बार शिस्टोसोम्स के विश्लेषण के दौरान नोट की गई थी। इसके अलावा, शिस्टोसोमा मैनसोनी के साथ प्रतिरक्षित चूहों से प्लेटलेट्स का निष्क्रिय हस्तांतरण उन्हें बाद के संक्रमण से बचाने के लिए पाया गया है।कृमिनाशक क्रिया में प्लेटलेट्स की भूमिका को ध्यान में रखते हुए, लेखकों ने इसे मोनोन्यूक्लियर फागोसाइट्स, साथ ही मास्ट कोशिकाओं की साइटोटोक्सिसिटी के लिए एक सहायक के रूप में मूल्यांकन किया, और नोट किया कि प्लेटलेट साइटोटोक्सिसिटी को प्रेरित करने वाला कारक आईजीई के लिए एफसी रिसेप्टर है।
उन्हीं शोधकर्ताओं ने बाद में दिखाया कि, IgE (FceRII) के लिए कम-एफ़िनिटी रिसेप्टर के साथ, वे इस इम्युनोग्लोबुलिन आइसोटाइप, FceRI के लिए उच्च-एफ़िनिटी रिसेप्टर को भी व्यक्त करते हैं; उत्तरार्द्ध की अभिव्यक्ति अत्यधिक विषम है, और प्लेटलेट्स की केवल एक छोटी संख्या दोनों रिसेप्टर्स को सह-व्यक्त करती है।
प्लेटलेट साइटोटॉक्सिसिटी को विभिन्न उत्तेजक (कैल्शियम आयनोपोर, पीएएफ, पीएचए, रिकिन, आदि) द्वारा प्रेरित किया जा सकता है। सभी कारक प्लेटलेट्स द्वारा थ्रोम्बोक्सेन -2 के उत्पादन और थ्रोम्बोक्सेन ए उत्पादों के हाइड्रोलिसिस को बढ़ाते हैं; कुछ ट्यूमर लाइनों की कोशिकाओं के संबंध में, विशेष रूप से K562 में, प्लेटलेट साइटोटोक्सिसिटी दोनों कारकों की सक्रियता के साथ थी।
वर्तमान में, प्लेटलेट साइटोटोक्सिसिटी के दो मुख्य तंत्र ज्ञात हैं - साइक्लोऑक्सीजिनेज उत्पादों (TXA2/PGH2) और नाइट्रिक ऑक्साइड की क्रिया।
प्लेटलेट्स की लाइटिक क्रिया के प्रति ट्यूमर कोशिकाएं अपनी संवेदनशीलता में भिन्न होती हैं, जिसकी पुष्टि विभिन्न लाइनों की सेल लाइनों के अध्ययन के आंकड़ों से होती है: K562, KU812, LU99A, KG1 कोशिकाएं संवेदनशील थीं, जबकि U937, M1APaCa2 और MOLT-4 कोशिकाएं संवेदनशील थीं। पूरी तरह से असंवेदनशील।
विशेष रूप से, K562 और LU99A कोशिकाओं (फेफड़ों के कैंसर) के खिलाफ प्लेटलेट साइटोटोक्सिसिटी के अध्ययन से पता चला है कि वे प्लेटलेट साइटोटॉक्सिक उत्पादों (साइक्लोऑक्सीजिनेज और नाइट्रिक ऑक्साइड के विभिन्न अवरोधकों का उपयोग किया गया था) के प्रति अलग संवेदनशीलता प्रदर्शित करते हैं: यदि K.562 कोशिकाओं की भागीदारी के साथ lysed थे साइक्लोऑक्सीजिनेज उत्पाद, फिर LU99A कोशिकाएं - नाइट्रिक ऑक्साइड की क्रिया के तहत।
व्यक्तिगत ट्यूमर कोशिकाओं की संवेदनशीलता में इन अंतरों के लिए, सक्रिय और गैर-सक्रिय प्लेटलेट्स की कार्रवाई में भी अंतर हैं, जिसकी पुष्टि इलेक्ट्रॉन सूक्ष्म अध्ययन द्वारा की गई थी। यह पता चला कि अस्थिर प्लेटलेट्स K562 कोशिकाओं से जुड़ते हैं, जबकि उत्तेजित नहीं होते हैं।
इससे यह पता चलता है कि प्लेटलेट्स की उत्तेजना के बिना, उनके और ट्यूमर कोशिकाओं के बीच सीधा संपर्क अनिवार्य है, और उत्तेजित प्लेटलेट्स के लिए यह वैकल्पिक है। यह भी माना जाता है कि प्लेटलेट्स द्वारा लिसिस का प्रभाव उनके घुलनशील कारकों से जुड़ा होता है, जो आसानी से निष्क्रिय हो जाते हैं।
ये तथ्य विभिन्न कोशिकाओं के साथ उनकी बातचीत के किसी भी रूप के लिए ट्यूमर कोशिकाओं के जैविक गुणों के महत्व की सार्वभौमिकता की एक और पुष्टि के रूप में काम करते हैं।
लेखकों द्वारा अध्ययन किए गए विभिन्न ट्यूमर लाइनों की कोशिकाओं की विविधता ने उन्हें यह निष्कर्ष निकालने का कारण दिया कि प्लेटलेट्स एंटीट्यूमर रक्षा में प्रभावकारी साइटोटॉक्सिक कोशिकाएं हैं।
अंत में, प्लेटलेट्स, जैसा कि उल्लेख किया गया है, मोनोसाइट्स, एनके और टी-लिम्फोसाइट्स पर नियामक प्रभाव डाल सकते हैं, जिससे उनके साइटोटॉक्सिक प्रभाव बदल सकते हैं। इस तथ्य के बावजूद कि इस मुद्दे का बहुत कम अध्ययन किया गया है, इसके कथन की वैधता की पुष्टि डेटा द्वारा की जाती है कि कुछ मामलों में प्लेटलेट्स की उपस्थिति मोनोसाइट्स की साइटोटोक्सिसिटी को बढ़ाती है।
प्लेटलेट साइटोटोक्सिसिटी के मुख्य तंत्र को अंजीर में दिखाया गया है। 53.

चावल। 53. प्लेटलेट साइटोटोक्सिसिटी के तंत्र
इस प्रकार, प्रस्तुत कुछ आंकड़ों से, यह स्पष्ट हो जाता है कि प्लेटलेट्स में विभिन्न ट्यूमर लक्ष्यों पर साइटोटॉक्सिक प्रभाव डालने की क्षमता भी होती है, लेकिन इस क्रिया के तंत्र आगे के अध्ययन के अधीन हैं।
ट्यूमर के विकास पर प्लेटलेट्स का नकारात्मक प्रभाव
साइटोटोक्सिक क्रिया करने की क्षमता के साथ, प्लेटलेट्स एंटीट्यूमर सुरक्षा को भी नकारात्मक रूप से प्रभावित कर सकते हैं। इस तथ्य के बावजूद कि विकास इम्यूनोस्टिम्यूलेशन में विभिन्न कोशिकाओं की भागीदारी मोनोग्राफ के तीसरे भाग में चर्चा का विषय होगी, यहां प्लेटलेट्स के नकारात्मक प्रभाव के मुद्दे पर चर्चा करना उचित लगा, क्योंकि, सबसे पहले, वे शास्त्रीय कोशिकाएं नहीं हैं प्रतिरक्षा प्रणाली की, और दूसरी बात, इम्युनोस्टिम्यूलेशन में कोई प्रत्यक्ष भागीदारी नहीं है।यह ज्ञात है कि प्लेटलेट्स अक्सर ट्यूमर के ऊतकों में घुसपैठ करते हैं, और इसलिए सवाल उठता है: उनकी उपस्थिति टीएनएफए की कार्रवाई को कैसे प्रभावित करती है, जो साइटोटोक्सिसिटी के महत्वपूर्ण घटकों में से एक है?
इस प्रश्न का उत्तर देने के लिए, प्लेटलेट्स के साथ L929 फाइब्रोसारकोमा कोशिकाओं का प्रदर्शन किया गया और यह दिखाया गया कि प्लेटलेट्स की उपस्थिति TNFa-निर्भर साइटोलिसिस को कमजोर करती है। हालांकि, TNFa के प्रभाव की कमी या तो इसके क्षरण या इस कारक को बाँधने के लिए ट्यूमर कोशिकाओं की क्षमता के नुकसान से जुड़ी नहीं थी। यह पता चला कि TNFa प्लेटलेट्स के कुछ क्षेत्रों के साथ इंटरैक्ट करता है, जिसके परिणामस्वरूप ट्यूमर कोशिकाओं के लिए इसका अधूरा बंधन होता है।
प्लेटलेट्स की नकारात्मक भूमिका में यह तथ्य भी शामिल होना चाहिए कि, कुछ शर्तों के तहत, वे इन विट्रो और इन विवो में प्राकृतिक हत्यारों के लसीका से ट्यूमर कोशिकाओं की रक्षा करते हैं। विभिन्न लाइनों (CFS1, B16) की कोशिकाओं के साथ प्रयोग में, डेटा प्राप्त किया गया था कि ट्यूमर कोशिकाओं के आसपास प्लेटलेट एकत्रीकरण एनके के उनके विश्लेषण को रोकता है।
प्राकृतिक हत्यारों और असंवेदनशील दोनों के प्रति संवेदनशील सेल लाइनों के उपयोग से पता चला है कि सभी मामलों में, प्लेटलेट्स परिधीय रक्त में ट्यूमर कोशिकाओं के अस्तित्व में योगदान करते हैं, मेटास्टेसिस की प्रक्रिया को बढ़ाते हैं।
तथ्य यह है कि प्लेटलेट्स एनके प्रभाव के कार्यान्वयन को रोकते हैं, इसकी पुष्टि एसबीसीएल2 लाइन के गैर-मेटास्टेसाइजिंग मेलेनोमा कोशिकाओं और एरिस्टोस्टैटिन के उपयोग से होती है, जो एआईआईबी3-इंटीग्रिन को बांधता है: इस दवा की कार्रवाई के तहत, मेलेनोमा कोशिकाएं अत्यधिक संवेदनशील हो जाती हैं। एनके-जैसे टाल-104 कोशिकाएं; रिसेप्टर जिसके साथ एरिस्टोस्टैटिन मेलेनोमा कोशिकाओं के साथ संपर्क करता है अज्ञात है।
विशेष रुचि प्लेटलेट्स की ट्यूमर कोशिकाओं के साथ बातचीत करने की क्षमता है। यह क्षमता और इसकी गंभीरता काफी हद तक ट्यूमर सेल की जैविक विशेषताओं पर निर्भर करती है। इस बातचीत की महत्वपूर्ण अभिव्यक्तियों में से एक प्लेटलेट एकत्रीकरण है, जो मेटास्टेस की घटना से जुड़ा हुआ है।
ये डेटा विभिन्न ट्यूमर की सेल लाइनों पर प्राप्त किए गए थे; यह दिखाया गया है कि ट्यूमर और प्लेटलेट्स के बीच बातचीत सक्रिय रूप से अत्यधिक मेटास्टैटिक फाइब्रोसारकोमा आरएके 17.15 में उत्तरार्द्ध के एकत्रीकरण को बढ़ावा देती है (इस तरह के कम-मेटास्टेसाइजिंग ट्यूमर आरएके 17.14 पर प्रभाव कमजोर रूप से व्यक्त किया जाता है)।
मेलेनोमा और एडेनोसारकोमा M7609 कोशिकाओं का अध्ययन करते समय, यह पाया गया कि वे हेपरिनिज्ड प्लाज्मा में प्लेटलेट एकत्रीकरण का कारण बनते हैं; कुछ मामलों में, यह प्रक्रिया झिल्ली ग्लाइकोप्रोटीन GPlb की भागीदारी पर निर्भर करती है, अन्य में, ग्लाइकोप्रोटीन GPIb/IIIa पर।
प्लेटलेट्स छोटे सेल फेफड़े के कार्सिनोमा और न्यूरोब्लास्टोमा कोशिकाओं के प्रभाव में भी सक्रिय होते हैं, एक प्रक्रिया जो पी-चयनिन को सियालिल-लुईस अणुओं वाले कार्बोहाइड्रेट संरचनाओं से बांधकर मध्यस्थता करती है। सियालाइज्ड कार्बोहाइड्रेट श्रृंखला gp44 की उपस्थिति भी माउस एडेनोकार्सिनोमा कोशिकाओं (लाइन 26) के एकत्रीकरण को बढ़ावा देती है।
मानव फेफड़े के कैंसर कोशिकाओं (छोटे सेल, स्क्वैमस, बड़े सेल कार्सिनोमा, एडेनोकार्सिनोमा और वायुकोशीय सेल कार्सिनोमा) के विभिन्न हिस्टोलॉजिकल उपप्रकारों के अध्ययन से पता चला है कि इन पंक्तियों की कोशिकाएं प्लेटलेट सक्रियण के विभिन्न मार्गों का उपयोग करती हैं: कुछ कोशिकाओं के लिए, एकत्रीकरण जुड़ा हुआ है। जमावट कारक VII और X की उपस्थिति, दूसरों के लिए - ट्यूमर और प्लेटलेट्स के बीच सीधे संपर्क की आवश्यकता के साथ।
काफी बार, ट्यूमर कोशिकाओं और प्लेटलेट्स की बातचीत को एंडोथेलियल कोशिकाओं और बाह्य मैट्रिक्स के साथ बातचीत के साथ भी जोड़ा जाता है। प्लेटलेट्स के हिस्से पर ट्यूमर कोशिकाओं, प्लेटलेट्स और बाह्य मैट्रिक्स के बीच बातचीत में एक महत्वपूर्ण स्थान ग्लाइकोप्रोटीन GPIIb / IIIa द्वारा कब्जा कर लिया जाता है, और ट्यूमर के हिस्से पर - a (v) -integrins, जो अध्ययन में दिखाया गया था तीन मानव मेलेनोमा लाइनों की कोशिकाएं और कार्सिनोमा की एक पंक्ति।
अंजीर पर। 54 ट्यूमर कोशिकाओं के साथ बातचीत के दौरान प्लेटलेट एकत्रीकरण में वृद्धि को दर्शाता है।

चावल। 54. ट्यूमर कोशिकाओं के साथ बातचीत के दौरान प्लेटलेट्स का एकत्रीकरण
कुछ मामलों में, इन विट्रो सिस्टम में प्लेटलेट्स एंडोथेलियल कोशिकाओं में ट्यूमर के आसंजन को रोक सकते हैं। हालांकि, विवो में प्लेटलेट्स को हटाना मेटास्टेसिस के निषेध के साथ था, जैसा कि विभिन्न माउस लाइनों (उपकला कोशिकाओं) और ट्यूमर कोशिकाओं जैसे फाइब्रोसारकोमा और थाइमोमा कोशिकाओं की कोशिकाओं द्वारा प्रेरित ट्यूमर के विकास के मॉडल में दिखाया गया है।
मेटास्टेस के विकास पर उनके संशोधक का उपयोग करके विभिन्न चिपकने वाले अणुओं (ICAM-1, LTA-1, VCAM-1, E- और P-selectins) की भूमिका को स्पष्ट करना संभव नहीं था।
कई और तथ्यों का हवाला दिया जा सकता है जो मेटास्टेसिस की वृद्धि में प्लेटलेट्स की भागीदारी को स्पष्ट करेंगे। हालांकि, इसकी परवाह किए बिना, प्लेटलेट्स के जैविक गुण ट्यूमर और एंडोथेलियल कोशिकाओं, बाह्य मैट्रिक्स के साथ सक्रिय रूप से बातचीत करने की उनकी स्पष्ट क्षमता का संकेत देते हैं। प्लेटलेट्स से जुड़े मेटास्टेसिस को बढ़ाने के लिए इस बातचीत का परिणाम कई तंत्र हो सकते हैं।
ये तंत्र मुख्य रूप से हैं:
1) ट्यूमर कोशिकाओं के प्रसार को उत्तेजित करने की संभावना;
2) बाह्य मैट्रिक्स के साथ ट्यूमर कोशिकाओं की बातचीत को बढ़ाना;
3) संवहनी बिस्तर में ट्यूमर कोशिकाओं के प्रवासन में वृद्धि।
पहले से ही ये निस्संदेह तथ्य थक्कारोधी चिकित्सा की वैधता को पहचानने के लिए पर्याप्त हैं, जो प्लेटलेट्स को प्रभावित करके मेटास्टेस के प्रसार के जोखिम को कम करता है। यह मानने का हर कारण है कि प्लेटलेट्स की भूमिका को ध्यान में रखते हुए इम्यूनोलॉजिकल अध्ययनों की सीमा का विस्तार करना, ऑन्कोइम्यूनोलॉजी में काफी आशाजनक दिशा हो सकती है।
बेरेज़्नाया एन.एम., चेखुन वी.एफ.
आज, अधिक से अधिक बीमारियां एक व्यक्ति को दूर करती हैं। तनाव, पारिस्थितिकी, अस्वास्थ्यकर भोजन, बुरी आदतों और थकान के निरंतर प्रभाव में भी शरीर कमजोर हो जाता है। शरीर में पूरा भार प्रतिरक्षा प्रणाली पर पड़ता है, जिसे बीमारियों और अन्य कार्यात्मक विकारों से बचाना चाहिए।
हाल ही में, डॉक्टर इसे आधुनिक बीमारियों का विरोध करने के अवसर के रूप में देखते हुए लगातार बात कर रहे हैं। मजबूत करने के तरीके के रूप में, इम्युनोमॉड्यूलेटर्स प्रस्तावित हैं, जो काफी हद तक मानव होमियोस्टेसिस की संतुलन प्रणाली में हस्तक्षेप करते हैं, इसलिए उन्हें अंतिम उपाय के रूप में और अत्यधिक सावधानी के साथ इस्तेमाल किया जाना चाहिए।
शरीर की सुरक्षा को मजबूत करने का एक और तरीका है रक्त को शिरा से नितंब में स्थानांतरित करना - हेमोथेरेपी। ऐसा करने के लिए, एक व्यक्ति एक नस से रक्त लेता है, और फिर बिना किसी अतिरिक्त प्रसंस्करण के तुरंत त्वचा के नीचे या इंट्रामस्क्युलर रूप से इंजेक्ट किया जाता है। इस तथ्य के कारण कि शारीरिक रूप से नितंब के ऊपरी चतुर्भुज को रक्त वाहिकाओं के साथ अच्छी तरह से आपूर्ति की जाती है, इंजेक्ट किया गया रक्त बहुत तेजी से अवशोषित होता है। यह प्रक्रिया शरीर में प्रतिरक्षा प्रक्रियाओं को बहुत उत्तेजित करती है।
ऑन्कोलॉजी, हेमटोलॉजी में - सबसे कठिन परिस्थितियों में शरीर के संघर्ष को प्रोत्साहित करने के लिए एक नस से नितंब तक रक्त आधान का उपयोग किया जाता है। साथ ही, यह विधि कुछ चिकित्सीय समस्याओं को हल कर सकती है, और हाल ही में, कॉस्मेटिक समस्याओं में रक्त आधान की प्रभावशीलता सिद्ध हुई है।
आमतौर पर, प्रभाव को प्राप्त करने के लिए, कम से कम दस प्रक्रियाएं करना आवश्यक होता है, लेकिन एक व्यक्तिगत नियुक्ति के साथ, डॉक्टर एक अलग संख्या में इंजेक्शन लिख सकता है। इंजेक्ट किए गए रक्त की खुराक भी परिवर्तनशील हो सकती है - यह सब हल की जाने वाली समस्या, इसकी गंभीरता और प्रगतिशील गतिशीलता की उपस्थिति पर निर्भर करता है।
शिरा से नितंब तक रक्त आधान का उपयोग त्वचा रोगों फुरुनकुलोसिस, एक्जिमा), (प्रजनन प्रणाली की सूजन और पुरानी बीमारियों), वनस्पति-संवहनी विकारों के उपचार में किया जाता है। रक्त आधान के बाद, रोगियों को एक सप्ताह के भीतर महत्वपूर्ण राहत महसूस होती है, संक्रमण के लिए शरीर की प्रतिरोधक क्षमता बढ़ जाती है, ऑपरेशन के बाद ऊतक बेहतर तरीके से ठीक हो जाते हैं।
यह याद रखना महत्वपूर्ण है कि प्रक्रिया योग्य चिकित्सा कर्मियों द्वारा अस्पताल में की जानी चाहिए। वे प्रारंभिक नियमों के पालन की निगरानी भी करते हैं, जैसे समूह द्वारा रक्त आधान। रक्त आधान के लिए जाने वाले लोगों को प्रक्रिया की आवश्यकताओं के बारे में पता होना चाहिए। आखिरकार, रक्त आधान के नियम मुख्य रूप से प्रक्रिया की सुरक्षा की गारंटी देते हैं, इसलिए उन्हें उपेक्षित नहीं किया जाना चाहिए। जब आधान आवश्यक हो:
- रक्त समूह का निरीक्षण करें;
- बाहर ले जाने, यदि आवश्यक हो, एक नियंत्रण आसव;
- चिकित्सा उपकरणों को पर्याप्त रूप से सड़न मुक्त करना;
- प्रक्रिया के दौरान और उसके बाद रोगी की स्थिति की निगरानी करें;
- मुख्य महत्वपूर्ण संकेतों की स्थिति का आकलन करें, विशेष रूप से हृदय प्रणाली की ओर से।
एक नस से नितंब में रक्त का आधान आमतौर पर साइड इफेक्ट का कारण नहीं बनता है - केवल कभी-कभी तापमान बढ़ सकता है, और इंजेक्शन साइट सूज सकती है। ऐसी स्थिति में, डॉक्टर एक कोमल इंजेक्शन लिखेंगे।
यदि इंट्रामस्क्युलर प्रशासन किसी व्यक्ति के लिए कम से कम खतरनाक है, तो उपचर्म प्रशासन हस्तक्षेप के लिए स्थानीय एलर्जी प्रतिक्रियाओं की धमकी दे सकता है। इनमें बुखार, मांसपेशियों में दर्द, जोड़ों में दर्द, ठंड लगना शामिल है। यदि ये लक्षण दिखाई देते हैं, तो चिकित्सक को तुरंत प्रक्रिया बंद कर देनी चाहिए और आवश्यक सहायता प्रदान करनी चाहिए।
रोगियों के लिए यह याद रखना महत्वपूर्ण है कि रक्त आधान एक जिम्मेदार प्रक्रिया है, इसलिए यदि कोई मतभेद हैं, तो ऐसा न करना बेहतर है।
