^ błona plazmatyczna , Lub plazmalemma, zajmuje szczególne miejsce wśród różnych błon komórkowych. Jest to powierzchowna struktura obwodowa, która ogranicza komórkę od zewnątrz, co warunkuje jej bezpośrednie połączenie ze środowiskiem pozakomórkowym, a co za tym idzie, ze wszystkimi substancjami i bodźcami działającymi na komórkę. Dlatego rolą błony plazmatycznej jest bycie barierą, barierą między kompleksowo zorganizowaną zawartością wewnątrzkomórkową a środowiskiem zewnętrznym. W tym przypadku plazmolemma spełnia nie tylko rolę bariery mechanicznej, ale przede wszystkim ogranicza swobodny przepływ substancji nisko- i wysokocząsteczkowych w obu kierunkach przez membranę. Ponadto plazmolemma działa jak struktura, która „rozpoznaje” receptory różnych substancji chemicznych i selektywnie reguluje transport tych substancji do iz komórki. Innymi słowy, błona plazmatyczna pełni funkcje związane z regulowanym selektywnym transbłonowym transportem substancji oraz pełni rolę podstawowego analizatora komórkowego. W związku z tym można rozważyć plazmalemę organoid komórkowy wchodzi w skład układu wakuolowego komórki. Podobnie jak inne błony tego układu (błony lizosomów, endosomy, aparat Golgiego itp.), powstaje i jest aktualizowany w wyniku syntetycznej aktywności retikulum endoplazmatycznego i ma podobny skład. Co dziwne, błonę plazmatyczną można porównać do błony wakuoli wewnątrzkomórkowej, ale wywróconej na lewą stronę: nie jest otoczona hialoplazmą, ale ją otacza.
Barierowo-transportowa rola plazmalemmy
Otaczająca komórkę ze wszystkich stron błona plazmatyczna działa jak bariera mechaniczna. Aby przekłuć go mikroigłami lub mikropipetami, trzeba sporo wysiłku. Pod naciskiem mikroigły najpierw mocno się ugina, a dopiero potem przebija. Sztuczne błony lipidowe są mniej stabilne. Ta mechaniczna stabilność błony plazmatycznej może być określona przez dodatkowe składniki, takie jak glikokaliks i warstwa korowa cytoplazmy (ryc. 127).
glikokaliks to zewnętrzna warstwa błony lipoproteinowej zawierająca łańcuchy polisacharydowe białek integralnych błony – glikoprotein. Łańcuchy te zawierają takie węglowodany jak mannoza, glukoza, N-acetyloglukozamina, kwas sialowy itp. Takie heteropolimery węglowodanowe tworzą rozgałęzione łańcuchy, pomiędzy którymi mogą znajdować się glikolipidy i proteoglikany wyizolowane z komórki. Warstwa glikokaliksu jest silnie nawodniona, ma galaretowatą konsystencję, co znacznie zmniejsza szybkość dyfuzji w tej strefie. różne substancje. „Utknąć” mogą tu również wydzielane przez komórkę enzymy hydrolityczne, które biorą udział w pozakomórkowym rozszczepianiu polimerów (trawienie pozakomórkowe) do cząsteczek monomeru, które następnie są transportowane do cytoplazmy przez błonę plazmatyczną.
W mikroskop elektronowy, zwłaszcza gdy specjalne metody W przeciwieństwie do polisacharydów glikokaliks ma postać luźnej włóknistej warstwy o grubości 3-4 nm, pokrywającej całą powierzchnię komórki. Glikokaliks jest szczególnie dobrze wyrażany w rąbku szczoteczkowym komórek wchłaniającego nabłonka jelitowego (enterocytów), jednak występuje w prawie wszystkich komórkach zwierzęcych, ale stopień jego nasilenia jest różny (ryc. 128).
Mechaniczna stabilność błony plazmatycznej jest dodatkowo zapewniona przez strukturę przylegającej do niej warstwy korowej od strony cytoplazmy i wewnątrzkomórkowych struktur włóknistych. korowe(od słowa - kora - kora, skórka) warstwa cytoplazmie leżącej w bliskim kontakcie z lipoproteiną zewnętrzna męmbrana, posiada szereg cech. Tutaj, w grubości 0,1-0,5 mikrona, nie ma rybosomów i pęcherzyków błonowych, ale w w dużych ilościach występują włókniste elementy cytoplazmy - mikrofilamenty i często mikrotubule. Głównym składnikiem włóknistym warstwy korowej jest sieć mikrowłókien aktynowych. Znajduje się tu również szereg białek pomocniczych, które są niezbędne do ruchu odcinków cytoplazmy (więcej szczegółów na temat układu szkieletowo-ruchowego komórek, patrz poniżej). Rola tych białek związanych z aktyną jest bardzo ważna, ponieważ wyjaśnia ich udział w połączeniu, w „zakotwiczeniu” integralnych białek błony plazmatycznej.
U wielu pierwotniaków, zwłaszcza orzęsków, błona plazmatyczna bierze udział w tworzeniu błonki, sztywna warstwa, która często określa kształt komórki. Woreczki błonowe mogą tu przylegać do błony plazmatycznej od wewnątrz; w tym przypadku w pobliżu powierzchni komórek znajdują się trzy warstwy błon: sama błona plazmatyczna i dwie błony pęcherzyków błonkowych. W orzęskach buta błonka tworzy zgrubienia, rozmieszczone w postaci sześciokątów, w środku których wyłaniają się rzęski (ryc. 129). Sztywność formacji błonkowych może być również związana z elementami cytoplazmy leżącej pod błoną plazmatyczną, z warstwą korową. Tak więc w grzebieniach błonki eugleny w pobliżu błony, oprócz wakuoli błonowych, znajdują się równoległe wiązki mikrotubul i mikrofilamentów. To włókniste wzmocnienie obwodowe wraz ze złożonym wielowarstwowym obrzeżem membrany tworzy sztywną strukturę błonki.
Barierowa rola plazmalemmy polega również na ograniczeniu swobodnej dyfuzji substancji. Eksperymenty modelowe na sztucznych błonach lipidowych wykazały, że są one przepuszczalne dla wody, gazów, małych niepolarnych cząsteczek substancji rozpuszczalnych w tłuszczach, ale całkowicie nieprzepuszczalne dla cząsteczek naładowanych (jony) i dużych nienaładowanych (cukry) (ryc. 130).
Naturalne membrany ograniczają również szybkość przenikania związków niskocząsteczkowych do wnętrza komórki.
Transbłonowy transport jonów i związków niskocząsteczkowych
Błona plazmatyczna, podobnie jak inne błony komórkowe lipoprotein, jest półprzepuszczalna. Oznacza to, że różne cząsteczki przechodzą przez nią z różnymi prędkościami i większy rozmiar cząsteczek, tym wolniejszy jest ich przepływ przez błonę. Ta właściwość definiuje błonę plazmatyczną jako barierę osmotyczną. Woda i rozpuszczone w niej gazy mają maksymalną zdolność penetracji, jony penetrują membranę znacznie wolniej (około 10 4 razy wolniej). Dlatego jeśli komórka, na przykład erytrocyt, zostanie umieszczona w środowisku, w którym stężenie soli jest niższe niż w komórce (niedociśnienie), to woda z zewnątrz napłynie do komórki, co doprowadzi do wzrostu objętości komórki i do pęknięcia błony plazmatycznej („wstrząs hipotoniczny”). Wręcz przeciwnie, gdy erytrocyt zostanie umieszczony w roztworach soli, więcej wysokie stężenie niż w komórce nastąpi ujście wody z komórki do środowiska zewnętrznego. W tym samym czasie komórka będzie się marszczyć, zmniejszając objętość.
Taki bierny transport wody z komórki do wnętrza komórki nadal przebiega z małą szybkością. Szybkość przenikania wody przez membranę wynosi około 10 -4 cm/s, czyli 100 000 razy mniej niż szybkość dyfuzji cząsteczek wody przez warstwę wodną o grubości 7,5 nm. Stwierdzono, że w Błona komórkowa, w jego warstwie lipoproteinowej znajdują się specjalne „pory” umożliwiające wnikanie wody i jonów. Ich liczba nie jest tak duża: łączna powierzchnia o wielkości pojedynczego „poru” około 0,3-0,8 nm powinna stanowić zaledwie 0,06% całej powierzchni komórki.
W przeciwieństwie do sztucznych dwuwarstwowych błon lipidowych, błony naturalne, a przede wszystkim błona plazmatyczna, nadal są zdolne do transportu jonów i wielu monomerów, takich jak cukry, aminokwasy itp. Przepuszczalność jonów jest niska, a szybkość przenikania różnych jonów jest nie ten sam. Większa szybkość przejścia dla kationów (K + , Na +) i znacznie niższa dla anionów (Cl -).
Transport jonów przez plazmalemę zachodzi dzięki udziałowi w tym procesie błonowych białek transportujących - permeaz. Białka te mogą transportować jedną substancję w jednym kierunku (uniport) lub kilka substancji jednocześnie (symport) lub wraz z importem jednej substancji usuwać inną z komórki (antyport). I tak np. glukoza może wnikać do komórek symportalnie razem z jonem Na+.
Transport jonów może mieć miejsce wzdłuż gradientu stężenia - biernie bez dodatkowego zużycia energii. Na przykład jon Na + wchodzi do komórki z otoczenie zewnętrzne gdzie jego stężenie jest wyższe niż w cytoplazmie. W przypadku transportu biernego niektóre białka transportu błonowego tworzą kompleksy molekularne, kanały przez którą cząsteczki substancji rozpuszczonej przechodzą przez błonę na drodze prostej dyfuzji wzdłuż gradientu stężeń. Niektóre z tych kanałów są stale otwarte, podczas gdy inne mogą się zamykać lub otwierać w odpowiedzi na wiązanie się z cząsteczkami sygnałowymi lub zmiany wewnątrzkomórkowego stężenia jonów. W innych przypadkach specjalne białka błonowe - przewoźnicy selektywnie wiążą się z jednym lub drugim jonem i przenoszą go przez membranę (dyfuzja ułatwiona) (ryc. 131).
Wydawać by się mogło, że obecność takich kanałów i nośników transportu białek powinna doprowadzić do zrównoważenia stężeń jonów i substancji małocząsteczkowych po obu stronach błony. W rzeczywistości tak nie jest: stężenie jonów w cytoplazmie komórek znacznie różni się nie tylko od tego w środowisku zewnętrznym, ale nawet od osocza krwi, które kąpie komórki w ciele zwierzęcia. Na stole 14 przedstawia stężenia jonów wewnątrz i na zewnątrz komórki.
Tabela 14
| I on | Stężenie wewnątrzkomórkowe, mM | Stężenie pozakomórkowe, mM |
| Na+ | 5-15 | 145 |
| K+ | 140 | 5 |
| Mg2+ | 30 | 1-2 |
| *Ca2+ | 1-2 | 2,5-5 |
| Cl- | 4 | 110 |
* Stężenie Ca 2+ w stanie wolnym w cytozolu komórek eukariotycznych wynosi 10 -7 M, a na zewnątrz 10 -3 M.
Jak widać, w tym przypadku całkowite stężenie kationów jednowartościowych zarówno wewnątrz, jak i na zewnątrz komórek jest prawie takie samo (150 mM), izotoniczny. Okazuje się jednak, że w cytoplazmie stężenie K+ jest prawie 50 razy wyższe, a Na+ niższe niż w osoczu krwi. Co więcej, ta różnica utrzymuje się tylko w żywej komórce: jeśli komórka zostanie zabita lub procesy metaboliczne w niej stłumione, to po pewnym czasie różnice jonowe po obu stronach błony plazmatycznej znikną. Możesz po prostu schłodzić komórki do +2 0 C, a po chwili stężenie K + i Na + po obu stronach membrany stanie się takie samo. Po podgrzaniu komórek różnica ta zostaje przywrócona. Zjawisko to wynika z faktu, że w komórkach znajdują się błonowe nośniki białkowe, które działają wbrew gradientowi stężeń, jednocześnie zużywając energię w wyniku hydrolizy ATP. Ten rodzaj pracy to tzw transport aktywny i odbywa się to za pomocą białka pompy jonowe. Błona plazmatyczna zawiera pompę składającą się z dwóch podjednostek (K + + Na +), która jest również ATPazą. Podczas pracy pompa ta wypompowuje 3 jony Na + w jednym cyklu i pompuje 2 jony K + do komórki wbrew gradientowi stężeń. W tym przypadku zużywana jest jedna cząsteczka ATP, która przechodzi do fosforylacji ATPazy, w wyniku czego Na + jest przenoszony przez błonę z komórki, a K + ma możliwość związania się z cząsteczką białka, a następnie jest przenoszony do komórka (ryc. 132). W wyniku transportu aktywnego za pomocą pomp membranowych dochodzi do regulacji w komórce także stężenia dwuwartościowych kationów Mg 2+ i Ca 2+, również przy zużyciu ATP.
Taki Praca na pełen etat permeazy i pomp tworzy stałe stężenie jonów i substancji niskocząsteczkowych w komórce, tworzy tzw. homeostaza, stałość stężeń osmotycznie substancje czynne. Należy zauważyć, że około 80% całkowitego ATP komórki zużywane jest na utrzymanie homeostazy.
W połączeniu z aktywnym transportem jonów przez błonę plazmatyczną, transportowane są różne cukry, nukleotydy i aminokwasy.
Zatem aktywny transport glukozy, która symportycznie (jednocześnie) dostaje się do komórki wraz z przepływem biernie transportowanego jonu Na+, będzie zależał od aktywności pompy (K++Na+). Jeśli ta (K+-Na+) pompa zostanie zablokowana, to wkrótce różnica w stężeniu Na+ po obu stronach membrany zniknie, natomiast dyfuzja Na+ do komórki zmniejszy się, a jednocześnie przepływ glukozy do komórki zostanie zatrzymany. Gdy tylko praca (K+-Na+)-ATPazy zostaje przywrócona i powstaje różnica w stężeniu jonów, natychmiast zwiększa się rozproszony przepływ Na+ i jednocześnie transport glukozy. Podobnie przez błonę i przepływ aminokwasów, które są transportowane przez specjalne białka nośnikowe, które działają jako układy symportowe, jednocześnie transportując jony.
Aktywny transport cukrów i aminokwasów w komórkach bakteryjnych wynika z gradientu jonów wodorowych.
Już sam udział specjalnych białek błonowych biorących udział w biernym lub aktywnym transporcie związków małocząsteczkowych wskazuje na wysoką specyficzność tego procesu. Nawet w przypadku pasywnego transportu jonów białka „rozpoznają” dany jon, wchodzą z nim w interakcje, specyficznie wiążą się, zmieniają swoją konformację i funkcję. Dlatego już na przykładzie transportu proste substancje membrany działają jak analizatory, jak receptory. Ta rola receptora jest szczególnie widoczna, gdy biopolimery są wchłaniane przez komórkę.
Transport pęcherzykowy: endocytoza i egzocytoza
Makrocząsteczki takie jak białka, kwasy nukleinowe, polisacharydy, kompleksy lipoproteinowe i inne nie przechodzą przez błony komórkowe, w przeciwieństwie do transportu jonów i monomerów. Transport mikrocząsteczek, ich kompleksów, cząstek do iz komórki odbywa się w zupełnie inny sposób - poprzez transfer pęcherzykowy. Termin ten oznacza, że różne makrocząsteczki, biopolimery lub ich kompleksy nie mogą przedostać się do komórki przez błonę plazmatyczną. I nie tylko przez to: żadne błony komórkowe nie są zdolne do transbłonowego przenoszenia biopolimerów, z wyjątkiem błon, które mają specjalne nośniki kompleksów białkowych - poryny (błony mitochondriów, plastydów, peroksysomów). Makrocząsteczki dostają się do komórki lub z jednego przedziału błony do drugiego, zamknięte w wakuolach lub pęcherzykach. Taki transfer pęcherzykowy można podzielić na dwa rodzaje: egzocytoza- usuwanie produktów wielkocząsteczkowych z komórki, oraz endocytoza- absorpcja makrocząsteczek przez komórkę (ryc. 133).
Podczas endocytozy pewna część plazmalemmy wychwytuje niejako otaczającą materiał pozakomórkowy, zamykając go w wakuoli błonowej, która powstała w wyniku inwazji błony plazmatycznej. W takiej pierwotnej wakuoli lub w endosom, mogą przedostać się wszelkie biopolimery, kompleksy makrocząsteczkowe, części komórek lub nawet całe komórki, gdzie następnie rozkładają się, depolimeryzują do monomerów, które dostają się do hialoplazmy przez transfer przezbłonowy. Głównym biologicznym znaczeniem endocytozy jest pozyskiwanie elementów budulcowych trawienie wewnątrzkomórkowe, która jest przeprowadzana w drugim etapie endocytozy po fuzji pierwotnego endosomu z lizosomem, wakuolą zawierającą zestaw enzymów hydrolitycznych (patrz poniżej).
Endocytoza jest formalnie podzielona na pinocytoza I fagocytoza(ryc. 134). Fagocytoza - wychwytywanie i wchłanianie dużych cząstek przez komórkę (czasami nawet komórki lub ich części) - została po raz pierwszy opisana przez II Miecznikowa. Fagocytoza, zdolność do wychwytywania dużych cząstek przez komórkę, występuje wśród komórek zwierzęcych, zarówno jednokomórkowych (na przykład ameba, niektóre drapieżne orzęski), jak i wyspecjalizowanych komórek zwierząt wielokomórkowych. Wyspecjalizowane komórki, fagocyty, są charakterystyczne zarówno dla bezkręgowców (amebocyty krwi lub płynu jamy ustnej), jak i kręgowców (neutrofile i makrofagi). Pinocytoza została pierwotnie zdefiniowana jako wchłanianie wody lub roztwory wodne różne substancje. Obecnie wiadomo, że zarówno fagocytoza, jak i pinocytoza przebiegają bardzo podobnie, dlatego użycie tych terminów może odzwierciedlać jedynie różnice w objętości i masie wchłanianych substancji. Cechą wspólną tych procesów jest to, że zaabsorbowane substancje na powierzchni błony plazmatycznej są otoczone błoną w postaci wakuoli - endosomu, który porusza się wewnątrz komórki.
Endocytoza, w tym pinocytoza i fagocytoza, może być niespecyficzna lub konstytutywna, trwała i specyficzna, w której pośredniczą receptory (receptor). Niespecyficzny endocyt h (pinocytoza i fagocytoza), tak zwana, ponieważ przebiega niejako automatycznie i często może prowadzić do wychwytywania i wchłaniania substancji całkowicie obcych lub obojętnych dla komórki, na przykład cząstek sadzy czy barwników.
Nieswoistej endocytozie często towarzyszy początkowa sorpcja uwięzionego materiału przez glikokaliks błony komórkowej. Glikokaliks, ze względu na kwasowe grupy swoich polisacharydów, ma ładunek ujemny i dobrze wiąże się z różnymi dodatnio naładowanymi grupami białek. Przy takiej adsorpcji niespecyficzna endocytoza wchłania makrocząsteczki i małe cząsteczki (białka kwaśne, ferrytyna, przeciwciała, wiriony, cząsteczki koloidalne). Pinocytoza w fazie ciekłej prowadzi do absorpcji wraz z ciekłym ośrodkiem rozpuszczalnych cząsteczek, które nie wiążą się z plazmalemmą.
NA Następny krok następuje zmiana w morfologii powierzchni komórki: jest to albo pojawienie się małych wgłobień błony plazmatycznej, wgłobienie, albo pojawienie się na powierzchni komórki narośli, fałd lub „falbanek” (rafl - po angielsku) , które niejako nakładają się, fałdują, oddzielając małe objętości płynnego ośrodka (ryc. 135, 136). Pierwszy typ występowania pęcherzyka pinocytowego, pinosomy, jest typowy dla komórek nabłonka jelitowego, śródbłonka, dla ameby, drugi - dla fagocytów i fibroblastów. Procesy te zależą od dostarczania energii: inhibitory oddychania blokują te procesy.
Po tym przegrupowaniu powierzchni następuje proces adhezji i fuzji stykających się błon, co prowadzi do powstania pęcherzyka penicytowego (pinosomu), który odrywa się od powierzchni komórki i wnika w głąb cytoplazmy. Zarówno endocytoza niespecyficzna, jak i receptorowa, prowadząca do rozszczepienia pęcherzyków błonowych, zachodzi w wyspecjalizowanych obszarach błony plazmatycznej. Są to tzw graniczące doły. Nazywa się je tak, ponieważ od strony cytoplazmy błona plazmatyczna jest pokryta, ubrana, cienką (około 20 nm) włóknistą warstwą, która na ultracienkich skrawkach niejako graniczy, pokrywa małe wypukłości, doły (ryc. 137). Prawie wszystkie komórki zwierzęce mają te wgłębienia; zajmują one około 2% powierzchni komórki. Otaczająca warstwa złożona głównie z białka klatryna związany z wieloma dodatkowymi białkami. Trzy cząsteczki klatryny wraz z trzema cząsteczkami białka o niskiej masie cząsteczkowej tworzą strukturę triskelionu, przypominającą trójramienną swastykę (ryc. 138). Triskeliony klatryny na wewnętrznej powierzchni dołów błony plazmatycznej tworzą luźną sieć składającą się z pięciokątów i sześciokątów, ogólnie przypominającą kosz. Warstwa klatryny pokrywa cały obwód oddzielających się pierwotnych wakuoli endocytarnych, otoczonych pęcherzykami.
Clathrin należy do jednego z tzw. białka „dressingowe” (COP – białka powlekane). Białka te wiążą się z integralnymi białkami receptorowymi od strony cytoplazmy i tworzą warstwę opatrunkową wokół obwodu powstającego pinosomu, pierwotnego pęcherzyka endosomalnego - pęcherzyka „granicznego”. w separację pierwotnego endosomu zaangażowane są również białka - dynaminy, które polimeryzują wokół szyi oddzielającego się pęcherzyka (ryc. 139).
Po oddzieleniu pęcherzyka granicznego od plazmolemy i rozpoczęciu przenoszenia w głąb cytoplazmy warstwa klatryny rozpada się, dysocjuje, błona endosomu (pinosomy) uzyskuje swoją zwykłą postać. Po utracie warstwy klatryny endosomy zaczynają się ze sobą łączyć.
Stwierdzono, że błony obrzeży jamek zawierają stosunkowo mało cholesterolu, co może determinować spadek sztywności błony i przyczyniać się do powstawania pęcherzyków. Biologiczne znaczenie pojawienia się „płaszcza” klatryny na obwodzie pęcherzyków może polegać na tym, że zapewnia on adhezję obrzeżonych pęcherzyków do elementów cytoszkieletu i ich dalszy transport w komórce oraz zapobiega ich łączeniu się ze sobą .
Intensywność niespecyficznej pinocytozy w fazie ciekłej może być bardzo wysoka. A więc komórka nabłonkowa jelito cienkie tworzy do 1000 pinosomów na sekundę, a makrofagi tworzą około 125 pinosomów na minutę. Rozmiar pinosomów jest niewielki, ich dolna granica wynosi 60–130 nm, ale ich obfitość prowadzi do tego, że podczas endocytozy plazmolemma jest szybko zastępowana, jakby „wydawana” na tworzenie wielu małych wakuoli. Tak więc w makrofagach cała błona plazmatyczna jest wymieniana w ciągu 30 minut, w fibroblastach - w ciągu dwóch godzin.
Dalszy los endosomów może być inny, część z nich może wrócić na powierzchnię komórki i połączyć się z nią, ale większość wchodzi w proces trawienia wewnątrzkomórkowego. Pierwotne endosomy zawierają głównie obce cząsteczki uwięzione w płynnym ośrodku i nie zawierają enzymów hydrolitycznych. endosomy mogą łączyć się ze sobą, jednocześnie zwiększając rozmiar. Następnie łączą się z pierwotnymi lizosomami (patrz poniżej), które wprowadzają enzymy do jamy endosomu, które hydrolizują różne biopolimery. Działanie tych hydrolaz lizosomalnych powoduje trawienie wewnątrzkomórkowe - rozkład polimerów do monomerów.
Jak już wspomniano, podczas fagocytozy i pinocytozy komórki tracą duży obszar plazmolemy (patrz makrofagi), który jednak jest szybko przywracany podczas recyklingu błony, z powodu powrotu wakuoli i ich włączenia do plazmolemy. Wynika to z faktu, że małe pęcherzyki mogą oddzielać się od endosomów lub wakuoli, a także od lizosomów, które ponownie łączą się z błoną plazmatyczną. Przy takiej recyklizacji następuje swego rodzaju „wahadłowy” transfer błon: plazmolemma - pinosom - wakuola - plazmolemma. Prowadzi to do przywrócenia pierwotnego obszaru błony plazmatycznej. Stwierdzono, że przy takim powrocie, recyklingu membranowym, cały zaabsorbowany materiał zostaje zatrzymany w pozostałym endosomie.
Konkretny Lub Zależny od receptora endocytoza ma wiele różnic od niespecyficznych. Najważniejsze jest to, że wchłaniane są cząsteczki, dla których na błonie komórkowej znajdują się specyficzne receptory, które są związane tylko z tego typu cząsteczkami. Często nazywane są takie cząsteczki, które wiążą się z białkami receptorowymi na powierzchni komórek ligandy.
Endocytoza za pośrednictwem receptorów została po raz pierwszy opisana w akumulacji białek w ptasich oocytach. Białka ziarniste żółtka, witellogeniny, są syntetyzowane w różne tkaniny, ale potem wraz z krwią dostają się do jajników, gdzie wiążą się ze specjalnymi receptorami błonowymi oocytów, a następnie za pomocą endocytozy dostają się do komórki, gdzie następuje odkładanie się ziarnistości żółtka.
Innym przykładem selektywnej endocytozy jest transport cholesterolu do komórki. Lipid ten jest syntetyzowany w wątrobie i w połączeniu z innymi fosfolipidami oraz cząsteczką białka tworzy tzw. lipoproteiny o małej gęstości (LDL), które są wydzielane przez wątrobę i układ krążenia rozprzestrzenia się po całym ciele (ryc. 140). Dedykowane receptory błony plazmatycznej rozproszone na powierzchni różne komórki rozpoznają białkowy składnik LDL i tworzą specyficzny kompleks receptor-ligand. Następnie taki kompleks przemieszcza się do strefy granicznych jamek i ulega internalizacji - otoczonej błoną i zanurzonej głęboko w cytoplazmie. Wykazano, że zmutowane receptory mogą wiązać LDL, ale nie gromadzą się w okolicy dołów granicznych. Oprócz receptorów LDL znaleziono ponad dwa tuziny innych substancji biorących udział w endocytozie receptorów różnych substancji, z których wszystkie wykorzystują tę samą ścieżkę internalizacji przez doły graniczne. Prawdopodobnie ich rola polega na gromadzeniu receptorów: jeden i ten sam obrzeżony dół może gromadzić około 1000 receptorów różnych klas. Jednak w fibroblastach skupiska receptorów LDL są zlokalizowane w strefie graniczących jamek nawet przy braku ligandu w pożywce.
Dalszy los wchłoniętej cząsteczki LDL polega na tym, że ulega ona rozpadowi w składzie lizosom wtórny. Po zanurzeniu w cytoplazmie otoczonego pęcherzyka obciążonego LDL następuje gwałtowna utrata warstwy klatryny, pęcherzyki błonowe zaczynają się ze sobą łączyć, tworząc endosom – wakuolę zawierającą zaabsorbowane cząsteczki LDL wciąż związane z receptorami na powierzchni błony . Następnie następuje dysocjacja kompleksu ligand-receptor, małe wakuole są oddzielane od endosomu, którego błony zawierają wolne receptory. Pęcherzyki te są zawracane, włączane do błony komórkowej, a tym samym receptory wracają na powierzchnię komórki. Los LDL polega na tym, że po fuzji z lizosomami ulegają hydrolizie do wolnego cholesterolu, który może zostać włączony do błon komórkowych.
Endosomy charakteryzują się niższą wartością pH (pH 4-5), bardziej kwaśnym środowiskiem niż inne wakuole komórkowe. Wynika to z obecności białek w ich błonach. pompa protonowa, pompowanie jonów wodorowych przy jednoczesnym zużyciu ATP (H+-zależna ATPaza). Kwaśne środowisko wewnątrz endosomów odgrywa kluczową rolę w dysocjacji receptorów i ligandów. Oprócz, kwaśne środowisko jest optymalny do aktywacji enzymów hydrolitycznych w składzie lizosomów, które aktywują się po fuzji lizosomów z endosomami i prowadzą do powstania endolizosomy, w którym następuje rozszczepienie wchłoniętych biopolimerów.
W niektórych przypadkach los zdysocjowanych ligandów nie jest związany z hydrolizą lizosomalną. Tak więc w niektórych komórkach, po związaniu się receptorów plazmolemmy z określonymi białkami, otoczone klatryną wakuole zatapiają się w cytoplazmie i są przenoszone do innego obszaru komórki, gdzie ponownie łączą się z błoną plazmatyczną, a związane białka dysocjują z receptory. W ten sposób przeprowadza się transfer, transcytozę, niektórych białek przez ścianę komórki śródbłonka z osocza krwi do środowiska międzykomórkowego (ryc. 141). Innym przykładem transcytozy jest przenoszenie przeciwciał. Tak więc u ssaków przeciwciała matki mogą zostać przekazane młodemu poprzez mleko. W tym przypadku kompleks receptor-przeciwciało pozostaje niezmieniony w endosomie.
Fagocytoza
Jak już wspomniano, fagocytoza jest odmianą endocytozy i wiąże się z wchłanianiem przez komórkę dużych agregatów makrocząsteczek aż do żywych lub martwych komórek. Podobnie jak pinocytoza, fagocytoza może być niespecyficzna (na przykład absorpcja cząstek koloidalnego złota lub polimeru dekstranu przez fibroblasty lub makrofagi) i specyficzna, w której pośredniczą receptory na powierzchni błony plazmatycznej komórek fagocytarnych. Podczas fagocytozy powstają duże wakuole endocytarne - fagosom, które następnie łączą się z lizosomami, tworząc fagolizosomy.
Na powierzchni komórek zdolnych do fagocytozy (u ssaków są to neutrofile i makrofagi) znajduje się zestaw receptorów, które oddziałują z białkami ligandowymi. Więc o godz infekcje bakteryjne przeciwciała przeciwko białkom bakteryjnym wiążą się z powierzchniami komórki bakteryjne, tworząc warstwę, w której region Fc przeciwciał skierowany jest na zewnątrz. Ta warstwa jest rozpoznawana przez specyficzne receptory na powierzchni makrofagów i neutrofili, aw miejscach ich wiązania absorpcja bakterii rozpoczyna się od otoczenia jej błoną plazmatyczną komórki (ryc. 142).
Egzocytoza
Błona plazmatyczna bierze udział w usuwaniu substancji z komórki za pomocą egzocytoza- odwrotny proces endocytozy (patrz ryc. 133).
W przypadku egzocytozy produkty wewnątrzkomórkowe zamknięte w wakuolach lub pęcherzykach i oddzielone od hialoplazmy błoną zbliżają się do błony plazmatycznej. W punktach styku błona plazmatyczna i błona wakuoli łączą się, a bańka jest opróżniana do środowiska. Za pomocą egzocytozy zachodzi proces recyklingu błon zaangażowanych w endocytozę.
Egzocytoza jest związana z uwalnianiem różnych substancji syntetyzowanych w komórce. Wydzielając, uwalniając substancje do środowiska, komórki mogą wytwarzać i uwalniać związki niskocząsteczkowe (acetylocholina, aminy biogenne itp.), a także w większości przypadków makrocząsteczki (peptydy, białka, lipoproteiny, peptydoglikany itp.). Egzocytoza lub wydzielanie w większości przypadków następuje w odpowiedzi na sygnał zewnętrzny (impuls nerwowy, hormony, mediatory itp.). Chociaż w niektórych przypadkach egzocytoza występuje stale (wydzielanie fibronektyny i kolagenu przez fibroblasty). Podobnie niektóre polisacharydy (hemicelulozy) zaangażowane w tworzenie ścian komórkowych są usuwane z cytoplazmy komórek roślinnych.
Większość wydzielanych substancji jest wykorzystywana przez inne komórki organizmów wielokomórkowych (wydzielanie mleka, soków trawiennych, hormonów itp.). Ale często komórki wydzielają substancje na własne potrzeby. Na przykład wzrost błony plazmatycznej odbywa się poprzez osadzenie odcinków błony jako części wakuoli egzocytarnych, niektóre elementy glikokaliksu są wydzielane przez komórkę w postaci cząsteczek glikoprotein itp.
Enzymy hydrolityczne wyizolowane z komórek przez egzocytozę mogą być sorpowane w warstwie glikokaliksu i zapewniać związane z błoną zewnątrzkomórkowe rozszczepianie różnych biopolimerów i cząsteczek organicznych. Błonowe trawienie pozakomórkowe ma ogromne znaczenie dla zwierząt. Stwierdzono, że w nabłonek jelitowy ssaków w rejonie tzw. rąbka szczoteczkowego nabłonka ssącego, szczególnie bogatego w glikokaliks świetna ilość różnorodne enzymy. Niektóre z tych enzymów są pochodzenia trzustkowego (amylazy, lipazy, różne proteinazy itp.), a niektóre są wydzielane przez same komórki nabłonka (egzohydrolazy, które rozkładają głównie oligomery i dimery z tworzeniem transportowanych produktów).
Receptorowa rola plazmalemmy
Z tą cechą błony plazmatycznej spotkaliśmy się już przy zapoznawaniu się z jej funkcjami transportowymi. Białka nośnikowe i pompy są również receptorami, które rozpoznają określone jony i wchodzą z nimi w interakcje. Białka receptorowe wiążą się z ligandami i biorą udział w selekcji cząsteczek wchodzących do komórek.
Białka błonowe lub elementy glikokaliksu – glikoproteiny mogą pełnić rolę takich receptorów na powierzchni komórki. Takie miejsca wrażliwe na poszczególne substancje mogą być rozproszone po powierzchni komórki lub gromadzone w małych strefach.
Różne komórki organizmów zwierzęcych mogą mieć różne zestawy receptorów lub różną czułość tego samego receptora.
Rolą wielu receptorów komórkowych jest nie tylko wiązanie określonych substancji czy zdolność reagowania na nie czynniki fizyczne ale także w przekazywaniu sygnałów międzykomórkowych z powierzchni do komórki. Obecnie dobrze zbadano system przekazywania sygnału do komórek za pomocą niektórych hormonów, w tym łańcuchów peptydowych. Stwierdzono, że hormony te wiążą się ze specyficznymi receptorami na powierzchni błony plazmatycznej komórki. Receptory po związaniu się z hormonem aktywują inne białko, znajdujące się już w cytoplazmatycznej części błony komórkowej, cyklazę adenylanową. Enzym ten syntetyzuje cykliczną cząsteczkę AMP z ATP. Rolą cyklicznego AMP (cAMP) jest to, że jest przekaźnikiem wtórnym - aktywatorem enzymów - kinaz powodujących modyfikacje innych białek enzymatycznych. Tak więc, kiedy hormon trzustkowy glukagon, wytwarzany przez komórki A wysepek Langerhansa, działa na komórkę wątroby, hormon ten wiąże się ze specyficznym receptorem, który stymuluje aktywację cyklazy adenylanowej. Zsyntetyzowany cAMP aktywuje kinazę białkową A, która z kolei aktywuje kaskadę enzymów, które ostatecznie rozkładają glikogen (polisacharyd pochodzenia zwierzęcego) do glukozy. Działanie insuliny jest odwrotne – stymuluje ona wnikanie glukozy do komórek wątroby i jej odkładanie w postaci glikogenu.
Ogólnie łańcuch zdarzeń przebiega następująco: hormon oddziałuje specyficznie z częścią receptorową tego układu i bez wnikania do komórki aktywuje cyklazę adenylanową, która syntetyzuje cAMP, który aktywuje lub hamuje wewnątrzkomórkowy enzym lub grupę enzymów . W ten sposób polecenie, sygnał z błony plazmatycznej jest przesyłany do wnętrza komórki. Wydajność tego układu cyklazy adenylanowej jest bardzo wysoka. Tak więc interakcja jednej lub kilku cząsteczek hormonu może prowadzić, w wyniku syntezy wielu cząsteczek cAMP, do tysiąckrotnego wzmocnienia sygnału. W tym przypadku układ cyklazy adenylanowej służy jako konwerter sygnałów zewnętrznych.
Istnieje inny sposób, w jaki wykorzystuje się innych wtórnych posłańców - jest to tzw. szlak fosfatydyloinozytolu. Pod wpływem odpowiedniego sygnału (niektóre mediatory nerwowe i białka) aktywowany jest enzym fosfolipaza C, który rozszczepia fosfolipid difosforanu fosfatydyloinozytolu, będący częścią błony komórkowej. Produkty hydrolizy tego lipidu z jednej strony aktywują kinazę białkową C, która aktywuje kaskadę kinaz prowadzącą do określonych reakcji komórkowych, a z drugiej strony prowadzi do uwalniania jonów wapnia, co reguluje cała linia procesy komórkowe.
Innym przykładem aktywności receptora są receptory dla acetylocholiny, ważnego neuroprzekaźnika. Acetylocholina uwalniana z nerwowe zakończennie, wiąże się z receptorem na włóknie mięśniowym, powoduje impulsowy przepływ Na+ do wnętrza komórki (depolaryzacja błony), natychmiast otwierając około 2000 kanałów jonowych w strefie zakończenia nerwowo-mięśniowego.
Różnorodność i specyficzność zestawów receptorów na powierzchni komórek prowadzi do powstania bardzo złożonego systemu markerów, które umożliwiają odróżnienie własnych komórek (tego samego osobnika lub tego samego gatunku) od komórek innych. Podobne komórki wchodzą ze sobą w interakcje, prowadząc do adhezji powierzchni (koniugacja u pierwotniaków i bakterii, tworzenie kompleksów tkankowo-komórkowych). W tym przypadku komórki, które różnią się zestawem markerów determinant lub ich nie dostrzegają, są albo wykluczane z takiej interakcji, albo ulegają zniszczeniu u zwierząt wyższych w wyniku reakcji immunologicznych (patrz poniżej).
Błona plazmatyczna jest związana z lokalizacją specyficznych receptorów, które reagują na czynniki fizyczne. Tak więc w błonie plazmatycznej lub jej pochodnych w bakteriach fotosyntetyzujących i niebiesko-zielonych algach zlokalizowane są białka receptorowe (chlorofile) oddziałujące z kwantami światła. W błonie plazmatycznej światłoczułych komórek zwierzęcych znajduje się specjalny system białek fotoreceptorowych (rodopsyna), za pomocą których sygnał świetlny jest przekształcany w sygnał chemiczny, co z kolei prowadzi do wytworzenia impulsu elektrycznego.
Rozpoznawanie międzykomórkowe
W organizmach wielokomórkowych w wyniku interakcji międzykomórkowych powstają złożone zespoły komórkowe, których utrzymanie można przeprowadzić różne sposoby. W tkankach zarodkowych, embrionalnych, zwłaszcza na wczesne stadia rozwoju, komórki pozostają ze sobą połączone ze względu na zdolność ich powierzchni do sklejania się. Ta nieruchomość przyczepność(połączenie, adhezja) komórek można określić na podstawie właściwości ich powierzchni, które specyficznie oddziałują na siebie. Mechanizm tych połączeń jest dobrze zbadany, zapewnia go interakcja między glikoproteinami błon plazmatycznych. Przy takim międzykomórkowym oddziaływaniu komórek między błonami plazmatycznymi zawsze pozostaje szczelina o szerokości około 20 nm, wypełniona glikokaliksem. Traktowanie tkanki enzymami naruszającymi integralność glikokaliksu (mukazy działające hydrolitycznie na mucyny, mukopolisacharydy) lub uszkadzające błonę komórkową (proteazy) prowadzi do izolacji komórek od siebie, do ich dysocjacji. Jednakże, jeśli czynnik dysocjacji zostanie usunięty, komórki mogą ponownie złożyć się i ponownie agregować. Można więc dysocjować komórki gąbek o różnych kolorach, pomarańczowym i żółtym. Okazało się, że w mieszaninie tych komórek tworzą się dwa rodzaje agregatów: składające się tylko z komórek żółtych i tylko z komórek pomarańczowych. W tym przypadku mieszane zawiesiny komórek samoorganizują się, przywracając pierwotną strukturę wielokomórkową. Podobne wyniki uzyskano z rozdzielonymi zawiesinami komórkowymi zarodków płazów; w tym przypadku następuje selektywne przestrzenne oddzielenie komórek ektodermy od endodermy i od mezenchymu. Ponadto, jeśli tkanki są używane do ponownej agregacji późne etapy rozwoju zarodków, wówczas różne zespoły komórek o specyfice tkankowej i narządowej niezależnie gromadzą się w probówce, tworzą się agregaty nabłonkowe, podobne do kanaliki nerkowe itp.
Stwierdzono, że glikoproteiny transbłonowe są odpowiedzialne za agregację komórek jednorodnych. Bezpośrednio za połączenie, adhezję komórki odpowiedzialne są cząsteczki tzw. Białka CAM (cząsteczki adhezji komórkowej). Niektóre z nich łączą ze sobą komórki w wyniku oddziaływań międzycząsteczkowych, inne tworzą specjalne połączenia lub kontakty międzykomórkowe.
Interakcje między białkami adhezyjnymi mogą być homofilny gdy sąsiednie komórki wiążą się ze sobą za pomocą jednorodnych cząsteczek, heterofilny gdy różne rodzaje CAM na sąsiednich komórkach biorą udział w adhezji. Wiązanie międzykomórkowe zachodzi poprzez dodatkowe cząsteczki łącznika.
Istnieje kilka klas białek CAM. Są to kadheryny, immunoglobulinopodobne N-CAM (cząsteczki adhezyjne komórek nerwowych), selektyny, integryny.
Kadheryny są integralnymi fibrylarnymi białkami błonowymi, które tworzą równoległe homodimery. Oddzielne domeny tych białek są związane z jonami Ca 2+, co nadaje im pewną sztywność. Istnieje ponad 40 gatunków kadheryn. Tak więc E-kadheryna jest charakterystyczna dla komórek preimplantowanych zarodków i komórek nabłonkowych organizmów dorosłych. P-kadheryna jest charakterystyczna dla komórek trofoblastu, łożyska i naskórka, N-kadheryna jest zlokalizowana na powierzchni komórek nerwowych, komórek soczewki oraz na mięśniach sercowych i szkieletowych.
^ Cząsteczki adhezyjne komórek nerwowych (N-CAM) należą do nadrodziny immunoglobulin, tworzą połączenia między komórkami nerwowymi. Niektóre z N-CAM biorą udział w łączeniu synaps, jak również w adhezji komórek. układ odpornościowy.
selektyny również integralne białka błony komórkowej biorą udział w adhezji komórek śródbłonka, w wiązaniu płytek krwi, leukocytów.
Integryny są heterodimerami o łańcuchach i . Integryny przede wszystkim łączą komórki z substratami pozakomórkowymi, ale mogą również uczestniczyć w adhezji komórek do siebie.
Rozpoznawanie białek obcych
Jak już wspomniano, na obcych makrocząsteczkach (antygenach), które dostały się do organizmu, rozwija się złożona złożona reakcja - odpowiedź immunologiczna. Jego istota polega na tym, że niektóre limfocyty wytwarzają specjalne białka - przeciwciała, które specyficznie wiążą się z antygenami. Na przykład makrofagi rozpoznają kompleksy antygen-przeciwciało z ich receptorami powierzchniowymi i absorbują je (na przykład wchłanianie bakterii podczas fagocytozy).
W ciele wszystkich kręgowców istnieje ponadto system przyjmowania komórek obcych lub własnych, ale ze zmienionymi białkami błony komórkowej, np. infekcje wirusowe lub z mutacjami, często związanymi z nowotworową degeneracją komórek.
Białka znajdują się na powierzchni wszystkich komórek kręgowców, tzw. główny kompleks zgodności tkankowej(główny kompleks zgodności tkankowej – MHC). Są to białka integralne, glikoproteiny, heterodimery. Bardzo ważne jest, aby pamiętać, że każdy osobnik ma inny zestaw tych białek MHC. Wynika to z faktu, że są one bardzo polimorficzne, ponieważ każdy osobnik ma dużą liczbę naprzemiennych form tego samego genu (ponad 100), ponadto istnieje 7-8 loci kodujących cząsteczki MHC. Powoduje to w każdej komórce dany organizm, posiadające zestaw białek MHC, będą różnić się od komórek osobnika tego samego gatunku. specjalny kształt limfocyty, limfocyty T, rozpoznają MHC swojego ciała, ale najmniejsza zmiana w strukturze MHC (na przykład skojarzenie z wirusem lub wynik mutacji w poszczególnych komórkach) prowadzi do tego, że limfocyty T rozpoznają tak zmienione komórki i niszczą je, ale nie poprzez fagocytozę. Wydzielają specyficzne białka perforyny z wakuoli wydzielniczych, które są osadzone w błonie cytoplazmatycznej zmienionej komórki, tworzą w niej kanały transbłonowe, czyniąc błonę komórkową przepuszczalną, co prowadzi do śmierci zmienionej komórki (ryc. 143, 144).
Specjalne połączenia międzykomórkowe
Oprócz tych stosunkowo prostych (ale specyficznych) wiązań adhezyjnych (ryc. 145) istnieje szereg specjalnych struktur międzykomórkowych, styków lub połączeń, które pełnią określone funkcje. Są to połączenia blokujące, kotwiące i komunikacyjne (ryc. 146).
Zamykający Lub ścisłe połączenie charakterystyczne dla nabłonka jednowarstwowego. Jest to strefa, w której zewnętrzne warstwy dwóch błon plazmatycznych znajdują się tak blisko, jak to możliwe. W tym kontakcie często obserwuje się trójwarstwową membranę: dwie zewnętrzne warstwy osmofilne obu membran wydają się łączyć w jedną wspólną warstwę o grubości 2–3 nm. Fuzja membran nie zachodzi na całym obszarze ciasnego kontaktu, ale jest serią punktowych zbieżności membran (ryc. 147a, 148).
Na płaskich preparatach pęknięć błon plazmatycznych w strefie ścisłego kontaktu, metodą wymrażania i odpryskiwania, stwierdzono, że punktami styku błon są rzędy kuleczek. Są to białka okludyna i klaudyna, specjalne integralne białka błony komórkowej, zbudowane w rzędach. Takie rzędy kulek lub pasków mogą przecinać się w taki sposób, że tworzą niejako siatkę lub siatkę na powierzchni rozszczepienia. Ta struktura jest bardzo typowa dla nabłonka, zwłaszcza gruczołowego i jelitowego. W tym drugim przypadku ścisły kontakt tworzy ciągłą strefę fuzji błon plazmatycznych, otaczającą komórkę w części wierzchołkowej (górnej, patrzącej do światła jelita) (ryc. 148). W ten sposób każda komórka warstwy jest niejako otoczona taśmą tego kontaktu. Takie struktury można również zobaczyć za pomocą specjalnych plam w mikroskopie świetlnym. Nazwę otrzymali od morfologów płyty końcowe. Okazało się, że w tym przypadku rola styku zamykającego polega nie tylko na mechanicznym połączeniu ogniw ze sobą. Ta powierzchnia styku jest słabo przepuszczalna dla makrocząsteczek i jonów, przez co blokuje, blokuje przestrzenie międzykomórkowe, izolując je (a wraz z nimi środowisko wewnętrzne organizmu) od środowiska zewnętrznego (w tym przypadku światła jelita).
Można to wykazać za pomocą gęstych elektronowo środków kontrastowych, takich jak roztwór wodorotlenku lantanu. Jeśli światło jelita lub przewodu jakiegoś gruczołu jest wypełnione roztworem wodorotlenku lantanu, to na skrawkach pod mikroskopem elektronowym strefy, w których znajduje się ta substancja, mają dużą gęstość elektronową i będą ciemne. Okazało się, że ani strefa ścisłego kontaktu, ani przestrzenie międzykomórkowe pod nią nie ciemnieją. W przypadku uszkodzenia połączeń ścisłych (w wyniku lekkiej obróbki enzymatycznej lub usunięcia jonów Ca++) lantan wnika również w obszary międzykomórkowe. Podobnie wykazano, że ścisłe połączenia są nieprzepuszczalne dla hemoglobiny i ferrytyny w kanalikach nerkowych.
Zatem połączenia ścisłe stanowią barierę nie tylko dla makrocząsteczek, ale także nieprzepuszczalną dla cieczy i jonów.
Zamykający się lub ciasny kontakt występuje między wszystkimi typami nabłonka jednowarstwowego (śródbłonek, mezotelium, wyściółka).
Zakotwiczenie Lub połączenia blokujące lub kontakty są tak nazywane, ponieważ łączą nie tylko błony plazmatyczne sąsiednich komórek, ale także wiążą się z elementami włóknistymi cytoszkieletu (ryc. 149). Ten rodzaj związków charakteryzuje się obecnością dwóch rodzajów białek. Jednym z nich są transbłonowe białka łącznikowe (wiążące), które biorą udział albo w rzeczywistym połączeniu międzykomórkowym, albo w połączeniu plazmolemy ze składnikami macierzy zewnątrzkomórkowej (błona podstawna nabłonka, zewnątrzkomórkowe białka strukturalne tkanki łącznej).
Drugi to białka wewnątrzkomórkowe, które łączą lub zakotwiczają włókienka cytoplazmatyczne cytoszkieletu za elementami błony takiego kontaktu.
Połączenia kotwiczące obejmują międzykomórkowe połączenia punktów kotwiczących, pasma kotwiczące, połączenia ogniskowe lub płytki kotwiczące, z których wszystkie wiążą się wewnątrzkomórkowo z mikrofilamentami aktyny.
Inna grupa kotwiczących połączeń międzykomórkowych, desmosomy i hemidesmosomy, wiążą się z innymi elementami cytoszkieletu, a mianowicie z włóknami pośrednimi.
Międzykomórkowe połączenia punktowe znaleziono w wielu tkankach innych niż nabłonek, ale ich struktura została dokładniej opisana. taśmy specjalne (przylepne). w nabłonku jednowarstwowym (ryc. 150). Ta struktura otacza cały obwód komórki nabłonka, podobnie jak w przypadku ciasnego połączenia. Najczęściej taki pasek lub taśma leży poniżej ciasnego połączenia (patrz ryc. 146). W tym miejscu błony plazmatyczne nie są zwarte, a nawet nieco rozsunięte na odległość 25–30 nm, a pomiędzy nimi widoczna jest strefa o zwiększonej gęstości. To nic innego jak miejsca interakcji transbłonowych glikoprotein, które specyficznie przylegają do siebie i zapewniają mechaniczne połączenie między błonami dwóch sąsiednich komórek. Te białka łącznikowe należą do E-kadheryn, białek, które zapewniają specyficzne rozpoznawanie jednorodnych błon przez komórki. Zniszczenie tej warstwy glikoprotein prowadzi do izolacji poszczególnych komórek i zniszczenia warstwy nabłonkowej. Po stronie cytoplazmatycznej w pobliżu błony widoczne jest nagromadzenie jakiejś gęstej substancji, do której przylega warstwa cienkich (6-7 nm) włókienek leżących wzdłuż błony plazmatycznej w postaci wiązki biegnącej wzdłuż całego obwodu błony. komórka. Cienkie włókna to fibryle aktyny; wiążą się z błoną plazmatyczną poprzez białko kateniny, które tworzy gęstą warstwę w pobliżu błony.
Funkcjonalne znaczenie takiego połączenia wstęgowego polega jedynie na mechanicznym przyleganiu komórek do siebie: wraz ze skurczem włókien aktynowych we wstędze kształt komórki może się zmieniać. Uważa się, że kooperatywne skurcze włókienek aktyny we wszystkich komórkach warstwy nabłonkowej mogą powodować zmianę jej geometrii, na przykład zwijanie się w rurkę, podobnie jak to zachodzi podczas formowania się cewy nerwowej u zarodków kręgowców.
^ kontakty ogniskowe Lub płytki adhezyjne występują w wielu komórkach i są szczególnie dobrze zbadane w fibroblastach. Są zbudowane wg Ogólny plan z paskami samoprzylepnymi, ale są wyrażone jako małe obszary - blaszki na plazmalemmie. W tym przypadku transbłonowe białka łącznikowe integryny specyficznie wiążą się z białkami macierzy pozakomórkowej (na przykład fibronektyną) (ryc. 151). Od strony cytoplazmy te same glikoproteiny są związane z białkami błonowymi, do których należy również winkulina, która z kolei jest związana z wiązką włókien aktynowych. Funkcjonalne znaczenie kontaktów ogniskowych polega zarówno na zakotwiczeniu komórki w strukturach zewnątrzkomórkowych, jak i na stworzeniu mechanizmu umożliwiającego ruch komórek.
Desmosomy, struktury w postaci płytek lub guzików również łączą ze sobą komórki (ryc. 152, 153a). W przestrzeni międzykomórkowej widoczna jest tu również gęsta warstwa, reprezentowana przez oddziałujące na siebie integralne kadheryny błonowe – desmogleiny, które łączą ze sobą komórki. Po stronie cytoplazmatycznej do plazmolemy przylega warstwa białka desmoplakiny, z którą związane są włókna pośrednie cytoszkieletu. Desmosomy znajdują się najczęściej w nabłonku, w którym to przypadku włókna pośrednie zawierają keratynę. W komórkach mięśnia sercowego kardiomiocyty zawierają włókienka desminy jako część desmosomów. W śródbłonku naczyniowym desmosomy zawierają włókna pośrednie wimentyny.
Półdesmosomy- w zasadzie mają podobną budowę do desmosomu, ale są połączeniem komórek ze strukturami międzykomórkowymi. Tak więc w nabłonku glikoproteiny łącznikowe (integryny) desmosomów oddziałują z białkami tzw. błona podstawna, która zawiera kolagen, lamininę, proteoglikany itp.
Funkcjonalna rola desmosomów i hemidesmosomów jest czysto mechaniczna - mocno przylegają one do siebie i do leżącej pod spodem macierzy zewnątrzkomórkowej, co pozwala warstwom nabłonka wytrzymać duże obciążenia mechaniczne. Podobnie desmosomy ściśle wiążą ze sobą komórki mięśnia sercowego, co pozwala im na wykonywanie ogromnego obciążenia mechanicznego, pozostając związanymi w jednej kurczliwej strukturze.
W przeciwieństwie do styków ścisłych, wszystkie rodzaje styków wiążących są przepuszczalne dla roztworów wodnych i nie odgrywają żadnej roli w ograniczaniu dyfuzji.
^ Luki w kontaktach są uważane za połączenia komunikacyjne komórek; są to struktury zaangażowane w transmisję bezpośrednią substancje chemiczne z komórki do komórki, która może odgrywać ważną fizjologiczną rolę nie tylko w funkcjonowaniu wyspecjalizowanych komórek, ale także zapewniać interakcje międzykomórkowe podczas rozwoju organizmu, podczas różnicowania się jego komórek. Cechą charakterystyczną tego typu kontaktów jest zbieżność błon plazmatycznych dwóch sąsiednich komórek w odległości 2-3 nm (ryc. 147b, 153b). To ta okoliczność przez długi czas nie pozwalał na rozróżnienie na ultracienkich skrawkach ten gatunek styk od ciasnego styku izolującego (zamykającego). Podczas stosowania wodorotlenku lantanu zaobserwowano, że z niektórych ciasnych styków wycieka kontrast. W tym przypadku lantan wypełnił cienką szczelinę o szerokości około 3 nm między sąsiednimi błonami plazmatycznymi sąsiednich komórek. Stąd wziął się termin – kontakt lukowy. Dalszy postęp w rozszyfrowywaniu jego struktury osiągnięto metodą freeze-chipping. Okazało się, że strefy połączeń szczelinowych (o wielkości od 0,5 do 5 µm) na rozcięciach membran są usiane cząstkami o średnicy 7–8 nm ułożonymi heksagonalnie z okresem 8–10 nm, posiadającymi kanał o szerokości około 2 nm w Centrum. Te cząstki to tzw koneksony(ryc. 154). W strefach kontaktu szczelinowego może być od 10-20 do kilku tysięcy koneksonów, w zależności od cechy funkcjonalne komórki. Preparatywnie wyizolowano koneksony, które składają się z sześciu podjednostek koneksonu, białka o masie cząsteczkowej ok. 30 tys. Łącząc się ze sobą, koneksony tworzą cylindryczny agregat - konekson, w środku którego znajduje się kanał. Poszczególne koneksony są osadzone w błonie plazmatycznej w taki sposób, że przebijają się przez nią. Jeden konekson na błonie plazmatycznej komórki dokładnie przeciwstawia się koneksonowi na błonie komórkowej sąsiedniej komórki, tak że kanały dwóch koneksonów tworzą pojedynczą jednostkę. Koneksony pełnią rolę bezpośrednich kanałów międzykomórkowych, przez które jony i substancje niskocząsteczkowe mogą dyfundować z komórki do komórki. Stwierdzono, że koneksony mogą się zamykać, zmieniając średnicę kanału wewnętrznego, a tym samym uczestniczyć w regulacji transportu cząsteczek między komórkami.
Funkcjonalne znaczenie połączeń szczelinowych zostało zrozumiane w badaniu komórek olbrzymich ślinianki muchówki. Ze względu na swoje rozmiary mikroelektrody można łatwo wprowadzić do takich ogniw w celu zbadania przewodnictwa elektrycznego ich membran. Okazało się, że jeśli elektrody zostaną włożone do dwóch sąsiednich komórek, ich błony plazmatyczne wykazują niski opór elektryczny, a prąd przepływa między komórkami. Co więcej, okazało się, że wstrzyknięcie barwnika fluorescencyjnego do jednej komórki powoduje szybkie wykrycie znacznika w sąsiednich komórkach. Za pomocą różnych fluorochromów stwierdzono na komórkach kultur tkankowych ssaków, że substancje o masie cząsteczkowej nie większej niż 1-1,5 tys. o masie do 2 tys.). Wśród tych substancji były różne jony, aminokwasy, nukleotydy, cukry, witaminy, steroidy, hormony, cAMP. Ani białka, ani kwasy nukleinowe nie mogą przechodzić przez połączenia szczelinowe.
Wykorzystuje się w nich zdolność połączeń szczelinowych do służenia jako miejsce transportu związków o małej masie cząsteczkowej systemy komórkowe, gdzie potrzebna jest szybka transmisja impulsu elektrycznego (fali pobudzenia) z komórki do komórki bez udziału mediatora nerwowego. Tak więc wszystkie komórki mięśniowe mięśnia sercowego są połączone za pomocą połączeń szczelinowych (dodatkowo komórki są również połączone połączeniami adhezyjnymi) (ryc. 147b). Stwarza to warunki do synchronicznej redukcji ogromnej liczby komórek. Wraz ze wzrostem hodowli embrionalnych komórek mięśnia sercowego (miokardiocytów) niektóre komórki w warstwie zaczynają samoistnie kurczyć się niezależnie od siebie z inna częstotliwość, i dopiero po utworzeniu połączeń szczelinowych między nimi zaczynają bić synchronicznie jako pojedyncza kurcząca się warstwa komórek. W ten sam sposób zapewniony jest wspólny skurcz komórek mięśni gładkich w ścianie macicy.
Połączenia szczelinowe mogą służyć metabolicznej współpracy między komórkami poprzez wymianę różnych cząsteczek, hormonów, cAMP czy metabolitów. Przykładem tego jest wspólna hodowla zmutowanych komórek kinazy tymidynowej z normalnymi komórkami: gdy między tymi typami komórek występują połączenia szczelinowe, zmutowane komórki otrzymują trifosforan tymidyny z normalnych komórek przez połączenia szczelinowe i mogą uczestniczyć w syntezie DNA.
We wczesnych zarodkach kręgowców, począwszy od stadium 8-komórkowego, większość komórek jest połączona ze sobą za pomocą połączeń szczelinowych. Gdy zarodek się różnicuje, połączenia między wszystkimi komórkami znikają i pozostają tylko między grupami wyspecjalizowanych komórek. Na przykład podczas tworzenia cewy nerwowej połączenie komórek tej struktury z resztą naskórka zostaje przerwane, rozłączone.
Integralność i funkcjonowanie połączeń szczelinowych w dużym stopniu zależy od poziomu jonów Ca 2+ wewnątrz komórki. Zwykle stężenie wapnia w cytoplazmie jest bardzo niskie. Jeśli Ca 2+ zostanie wstrzyknięty do jednej z komórek warstwy hodowli tkankowej, wówczas nie nastąpi wzrost poziomu Ca 2+ w cytoplazmie w sąsiednich komórkach; komórki niejako są odłączone od swoich sąsiadów, przestają przewodzić Elektryczność i barwniki. Po pewnym czasie, po akumulacji wprowadzonego wapnia przez mitochondria, przywracana jest struktura i funkcje połączeń szczelinowych. Ta właściwość jest bardzo ważna dla zachowania integralności i działania całej warstwy komórek, ponieważ uszkodzenie jednej z nich nie jest przenoszone na sąsiednią przez połączenia szczelinowe, które przestają działać jako międzykomórkowe kanały dyfuzyjne.
^ kontakt synaptyczny (synapsy). Ten rodzaj kontaktu jest typowy dla tkanka nerwowa i występuje zarówno między dwoma neuronami, jak i między neuronem a jakimś innym elementem - receptorem lub efektorem (na przykład zakończeniem nerwowo-mięśniowym). Synapsy to obszary kontaktu między dwiema komórkami wyspecjalizowanymi w jednokierunkowej transmisji pobudzenia lub hamowania z jednego elementu do drugiego (ryc. 155). Zasadniczo tego rodzaju obciążenia funkcjonalnego, przekazywanie impulsów może odbywać się również przez inne rodzaje styków (np. styk szczelinowy w mięśniu sercowym), jednak w połączeniu synaptycznym wysoka wydajność w realizacji impulsu nerwowego. Synapsy powstają na procesach komórek nerwowych - są to końcowe odcinki dendrytów i aksonów. Synapsy międzyneuronalne mają zwykle wypustki w kształcie gruszki, blaszki na końcu procesu komórki nerwowej. Takie końcowe przedłużenie wyrostka jednej z komórek nerwowych może stykać się i tworzyć połączenie synaptyczne zarówno z ciałem innej komórki nerwowej, jak iz jej wypustkami. Obwodowe wyrostki komórek nerwowych (aksonów) tworzą specyficzne kontakty z komórkami efektorowymi lub receptorowymi. Dlatego synapsa jest strukturą, która tworzy się między regionami dwóch komórek (a także desmosomem). Błony tych komórek są oddzielone przestrzenią międzykomórkową - szczeliną synaptyczną o szerokości około 20-30 nm. Często w świetle tej szczeliny widoczny jest drobnowłóknisty materiał prostopadły do membran. Błona w obszarze kontaktu synaptycznego jednej komórki nazywana jest presynaptyczną, druga, odbierająca impuls, nazywana jest postsynaptyczną. W mikroskopie elektronowym obie membrany wyglądają na gęste i grube. W pobliżu błony presynaptycznej ujawnia się ogromna liczba małych wakuoli, pęcherzyków synaptycznych wypełnionych neuroprzekaźnikami. Pęcherzyki synaptyczne w momencie przejścia impulsu nerwowego wyrzucają swoją zawartość do szczeliny synaptycznej. Błona postsynaptyczna często wygląda na grubszą niż zwykłe błony ze względu na nagromadzenie wokół niej wielu cienkich włókienek od strony cytoplazmy.
plazmodesmy. Ten rodzaj komunikacji międzykomórkowej występuje w roślinach. Plazmodesmy to cienkie kanaliki cytoplazmatyczne łączące dwie sąsiednie komórki. Średnica tych kanałów wynosi zwykle 20-40 nm. Błona ograniczająca te kanały przechodzi bezpośrednio do błon plazmatycznych sąsiednich komórek. Plasmodesmy przechodzą przez ścianę komórkową, która oddziela komórki (ryc. 156, 157). Tak więc w niektórych komórkach roślinnych plazmodesmy łączą hialoplazmę sąsiednich komórek, więc formalnie nie ma pełnego rozróżnienia, oddzielenie ciała jednej komórki od drugiej, jest to raczej syncytium: połączenie wielu terytoriów komórkowych za pomocą cytoplazmy mosty. Elementy rurkowe błony mogą przenikać do plazmodesmy, łącząc cysterny retikulum endoplazmatycznego sąsiednich komórek. Plazmodesmy powstają podczas podziału komórki, kiedy budowana jest pierwotna ściana komórkowa (patrz poniżej). W nowo podzielonych komórkach liczba plazmodesmy może być bardzo duża (do 1000 na komórkę), wraz ze starzeniem się komórki ich liczba maleje z powodu pęknięć wraz ze wzrostem grubości. Ściana komórkowa.
Funkcjonalna rola plazmodesmy jest bardzo duża: z ich pomocą krążenie międzykomórkowe roztworów zawierających składniki odżywcze, jony i inne związki. Kropelki lipidów mogą przemieszczać się wzdłuż plazmodesmy.Komórki są zakażane wirusami roślinnymi przez plazmodesmy. Eksperymenty pokazują jednak, że swobodny transport przez plazmodesmy jest ograniczony do cząstek o masie nie większej niż 800 daltonów.
> Funkcje błony plazmatycznej. Mechanizmy transportu substancji przez plazmalemę. Funkcja receptorowa plazmalemmy
Błona plazmatyczna pełni szereg ważnych funkcji:
1) Bariera. Funkcją barierową błony plazmatycznej jest ograniczenie swobodnej dyfuzji substancji z komórki do komórki, aby zapobiec wyciekaniu rozpuszczalnej w wodzie zawartości komórki. Ale ponieważ komórka musi otrzymywać niezbędne składniki odżywcze, uwalniać końcowe produkty metabolizmu i regulować wewnątrzkomórkowe stężenie jonów, powstały w niej specjalne mechanizmy przenoszenia substancji przez błonę komórkową.
2) Transport. Funkcja transportowa jest Zapewnienie wejścia i wyjścia różnych substancji do iz komórki. Ważna właściwość membrany - selektywna przepuszczalność, Lub półprzepuszczalność. Z łatwością przepuszcza wodę i gazy rozpuszczalne w wodzie oraz odpycha molekuły polarne, takie jak glukoza czy aminokwasy.
Istnieje kilka mechanizmów transportu substancji przez błonę:
transport pasywny;
transport aktywny;
transport w opakowaniu membranowym.
Transport pasywny.Rozpowszechnianie - Jest to ruch cząstek ośrodka, prowadzący do przeniesienia substancji z obszaru o wysokim stężeniu do obszaru o niskim stężeniu. Podczas transportu dyfuzyjnego membrana działa jak bariera osmotyczna. Szybkość dyfuzji zależy od wielkości cząsteczek i ich względnej rozpuszczalności w tłuszczach. Jak mniejsze rozmiary cząsteczki i im bardziej są rozpuszczalne w tłuszczach (lipofilowe), tym szybciej będą przechodzić przez dwuwarstwę lipidową. Dyfuzja może być neutralny(przenoszenie nienaładowanych cząsteczek) i lekki(przy pomocy specjalnych białek nośnikowych). Dyfuzja ułatwiona jest szybsza niż dyfuzja neutralna. Woda ma maksymalną zdolność przenikania, ponieważ jej cząsteczki są małe i pozbawione ładunku. Dyfuzja wody przez błonę komórkową nazywa się osmoza. Przyjmuje się, że w błonie komórkowej istnieją specjalne „pory” umożliwiające przenikanie wody i niektórych jonów. Ich liczba jest niewielka, a średnica wynosi około 0,3-0,8 nm. Najszybciej przez błonę dyfundują cząsteczki łatwo rozpuszczalne w dwuwarstwie lipidowej, takie jak O, oraz nienaładowane cząsteczki polarne o małej średnicy (CO, mocznik).
Transfer molekuł polarnych (cukrów, aminokwasów) realizowany za pomocą specjalnych białek transportujących błonę to tzw ułatwiona dyfuzja. Takie białka znajdują się we wszystkich typach błon biologicznych, a każde określone białko jest zaprojektowane do przenoszenia cząsteczek określonej klasy. Białka transportujące są transbłonowe; ich łańcuch polipeptydowy kilkakrotnie przecina dwuwarstwę lipidową, tworząc w niej przejścia. Zapewnia to przenoszenie określonych substancji przez membranę bez bezpośredniego z nią kontaktu. Istnieją dwie główne klasy białek transportowych: białka nośnikowe (transportery) I kanałotwórczy białka (kanały białkowe). Białka nośnikowe przenoszą cząsteczki przez błonę, najpierw zmieniając ich konfigurację. Białka tworzące kanały tworzą w membranie wypełnione wodą pory. Gdy pory są otwarte, przechodzą przez nie cząsteczki określonych substancji (najczęściej jony nieorganiczne o odpowiedniej wielkości i ładunku). Jeżeli cząsteczka transportowanej substancji nie ma ładunku, to o kierunku transportu decyduje gradient stężeń. Jeżeli cząsteczka jest naładowana, to na jej transport oprócz gradientu stężeń wpływa również ładunek elektryczny błony (potencjał błony). Wewnętrzna strona Plazmalemma jest zwykle naładowana ujemnie w stosunku do zewnętrznej. Potencjał błony ułatwia przenikanie dodatnio naładowanych jonów do komórki i zapobiega przechodzeniu jonów naładowanych ujemnie.
transport aktywny. Transport aktywny to ruch substancji wbrew gradientowi elektrochemicznemu. Jest zawsze przeprowadzany przez białka transportujące i jest ściśle związany ze źródłem energii. Białka nośnikowe mają miejsca wiązania z transportowaną substancją. Im więcej takich miejsc związanych z substancją, tym większa szybkość transportu. Nazywa się selektywne przeniesienie jednej substancji uniport. Przeprowadza się transfer kilku substancji systemy współtransportowe. Jeśli transfer idzie w jednym kierunku, to tak symportować, jeśli naprzeciw antyport. Na przykład glukoza jest transportowana z płynu zewnątrzkomórkowego do komórki w sposób jednokierunkowy. Przenoszenie glukozy i Na4 odpowiednio z jamy jelitowej lub kanalików nerkowych do komórek jelita lub krwi odbywa się symportalnie, a przenoszenie C1~ i HCO "jest antyportem. .
Przykładem białka nośnikowego, które wykorzystuje energię uwolnioną podczas hydrolizy ATP do transportu substancji jest Na + -DO + pompa, znajduje się w błonie plazmatycznej wszystkich komórek. Pompa Na + -K działa na zasadzie antyportu, pompując Na "z komórki i K t do komórki wbrew ich gradientom elektrochemicznym. Gradient Na + wytwarza ciśnienie osmotyczne, utrzymuje objętość komórek i zapewnia transport cukrów i aminokwasów , Jedna trzecia całej energii jest wydawana na tę pompę niezbędną do życiowej aktywności komórek.Podczas badania mechanizmu działania pompy Na + -K + stwierdzono, że jest to enzym ATPaza i integralne białko transbłonowe. obecność Na+ i ATP, pod działaniem ATPazy końcowy fosforan jest oddzielany od ATP i przyłączany do reszty kwas asparaginowy na cząsteczce ATPazy. Cząsteczka ATPazy ulega fosforylacji, zmienia swoją konfigurację, a Na+ jest wydalany z komórki. Po usunięciu Na z komórki, K "jest zawsze transportowany do komórki. Aby to zrobić, wcześniej przyłączony fosforan jest odszczepiany od ATPazy w obecności K. Enzym jest defosforylowany, przywraca swoją konfigurację, a K 1 jest " wpompowana" do komórki.
ATPaza składa się z dwóch podjednostek, dużej i małej. Duża podjednostka składa się z tysięcy reszt aminokwasowych, które kilkakrotnie przechodzą przez dwuwarstwę. Ma aktywność katalityczną i może być odwracalnie fosforylowany i defosforylowany. Duża podjednostka po stronie cytoplazmatycznej ma miejsca wiązania Na + i ATP i dalej poza-miejsca wiązania K + i ouabainy. Mała podjednostka jest glikoproteiną, a jej funkcja nie jest jeszcze znana.
Pompa Na + -K ma działanie elektrogeniczne. Usuwa z ogniwa trzy dodatnio naładowane jony Na f i wprowadza do niego dwa jony K. W efekcie przez membranę przepływa prąd, tworząc potencjał elektryczny o wartości ujemnej w wewnętrznej części ogniwa względem jego zewnętrznej powierzchni . Pompa Na"-K+ reguluje objętość komórek, kontroluje stężenie substancji wewnątrz komórki, utrzymuje ciśnienie osmotyczne, bierze udział w tworzeniu potencjału błonowego.
Transport w opakowaniu membranowym. Przenoszenie makrocząsteczek (białek, kwasów nukleinowych, polisacharydów, lipoprotein) i innych cząstek przez błonę odbywa się poprzez sekwencyjne tworzenie i fuzję pęcherzyków (pęcherzyków) otoczonych błoną. Proces transportu pęcherzykowego przebiega dwuetapowo. Początkowo błona pęcherzyka i plazmalemia sklejają się, a następnie łączą. Dla przebiegu etapu 2 konieczne jest przemieszczanie cząsteczek wody przez oddziałujące dwuwarstwy lipidowe, które zbliżają się do siebie na odległość 1-5 nm. Uważa się, że proces ten jest aktywowany przez specjalne białka fuzyjne(były dotychczas izolowane tylko w wirusach). Transport pęcherzykowy ma ważna cecha- zaabsorbowane lub wydzielane makrocząsteczki w pęcherzykach zwykle nie mieszają się z innymi makrocząsteczkami lub organellami komórki. Pęcherzyki mogą łączyć się ze specyficznymi błonami, co zapewnia wymianę makrocząsteczek między przestrzenią pozakomórkową a zawartością komórki. Podobnie makrocząsteczki są przenoszone z jednego przedziału komórkowego do drugiego.
Nazywa się transport makrocząsteczek i cząstek do wnętrza komórki endocytoza. W tym przypadku transportowane substancje są otoczone częścią błony plazmatycznej, tworzy się pęcherzyk (wakuola), który porusza się wewnątrz komórki. W zależności od wielkości utworzonych pęcherzyków wyróżnia się dwa rodzaje endocytozy - pinocytoza i fagocytoza.
pinocytoza zapewnia wchłanianie cieczy i rozpuszczonych substancji w postaci małych pęcherzyków (d=150 nm). Fagocytoza - jest to wchłanianie dużych cząstek, mikroorganizmów lub fragmentów organelli, komórek. W tym przypadku tworzą się duże pęcherzyki, fagosomy lub wakuole (d-250 nm lub więcej). U pierwotniaków funkcja fagocytarna jest formą odżywiania. U ssaków funkcję fagocytarną pełnią makrofagi i neutrofile, które chronią organizm przed infekcją, pochłaniając atakujące drobnoustroje. Makrofagi biorą również udział w usuwaniu starych lub uszkodzonych komórek i ich fragmentów (w organizmie człowieka makrofagi wchłaniają dziennie ponad 100 starych krwinek czerwonych). Fagocytoza rozpoczyna się dopiero wtedy, gdy wchłonięta cząsteczka zwiąże się z powierzchnią fagocytu i aktywuje wyspecjalizowane komórki receptorowe. Wiązanie cząstek do określonych receptorów błonowych powoduje powstawanie pseudopodiów, które otaczają cząstkę i łącząc się na krawędziach tworzą bańkę - fagosom. Powstanie fagosomu i właściwa fagocytoza zachodzi tylko wtedy, gdy podczas procesu otaczania cząsteczka pozostaje w stałym kontakcie z receptorami plazmalemmy, jakby „zapinała się”.
Znaczna część materiału wchłoniętego przez komórkę na drodze endocytozy trafia do lizosomów. Duże cząstki są zawarte w fagosomy które następnie łączą się z lizosomami, tworząc fagolizosomy. Płyn i makrocząsteczki pobrane podczas pinocytozy są początkowo przenoszone do endosomów, które również łączą się z lizosomami, tworząc endolizosomy. Różne enzymy hydrolityczne obecne w lizosomach szybko niszczą makrocząsteczki. Produkty hydrolizy (aminokwasy, cukry, nukleotydy) są transportowane z lizosomów do cytosolu, gdzie są wykorzystywane przez komórkę. Większość składników błony pęcherzyków endocytarnych z fagosomów i endosomów jest zwracana przez egzocytozę do błony plazmatycznej i tam ponownie wykorzystywana. Główny znaczenie biologiczne Endocytoza to nabywanie elementów budulcowych poprzez wewnątrzkomórkowe trawienie makrocząsteczek w lizosomach.
Absorpcja substancji w komórki eukariotyczne rozpoczyna się w wyspecjalizowanych obszarach błony komórkowej, tzw graniczące doły. Na mikrografach elektronowych wgłębienia wyglądają jak inwazje błony plazmatycznej, której cytoplazmatyczna strona pokryta jest włóknistą warstwą. Warstwa niejako graniczy z małymi dołkami plazmalemmy. Dołki zajmują około 2% całkowitej powierzchni błony komórkowej eukariota. W ciągu minuty zagłębienia rosną, wnikają coraz głębiej, wciągane są do komórki, a następnie, zwężając się u podstawy, odszczepiają się, tworząc otoczone pęcherzyki. Ustalono, że około jedna czwarta błony w postaci otoczonych pęcherzyków jest oddzielona od błony plazmatycznej fibroblastów w ciągu jednej minuty. Pęcherzyki szybko tracą swoją granicę i nabywają zdolność łączenia się z lizosomem.
Endocytoza może być niespecyficzne(konstytutywny) i konkretny(chwytnik). Na niespecyficzna endocytoza komórka wychwytuje i absorbuje substancje, które są jej całkowicie obce, na przykład cząstki sadzy, barwniki. Początkowo cząstki osadzają się na glikokaliksie plazmalemmy. Dodatnio naładowane grupy białek są szczególnie dobrze wytrącane (adsorbowane), ponieważ glikokaliks ma ładunek ujemny. Następnie zmienia się morfologia błony komórkowej. Może tonąć, tworząc wklęsłości (wklęsłości) lub odwrotnie, tworzyć wyrostki, które wydają się fałdować, oddzielając małe objętości płynnego ośrodka. Powstawanie wklęsłości jest bardziej typowe dla komórek nabłonka jelitowego, ameb i wyrostków - dla fagocytów i fibroblastów. Procesy te mogą być blokowane przez inhibitory dróg oddechowych. Powstałe pęcherzyki - pierwotne endosomy - mogą łączyć się ze sobą, zwiększając rozmiar. Następnie łączą się z lizosomami, zamieniając się w endolizosom - wakuolę trawienną. Intensywność niespecyficznej pinocytozy w fazie ciekłej jest dość wysoka. Makrofagi tworzą do 125, a komórki nabłonka jelita cienkiego do tysiąca pinosomów na minutę. Obfitość pinosomów prowadzi do tego, że plazmalemia szybko zużywa się na tworzenie wielu małych wakuoli. Odbudowa błony przebiega dość szybko podczas recyklizacji podczas egzocytozy z powodu powrotu wakuoli i ich włączenia do plazmalemmy. W makrofagach cała błona plazmatyczna jest wymieniana w ciągu 30 minut, aw fibroblastach w ciągu 2 godzin.
Więcej efektywny sposób absorpcja z płynu pozakomórkowego określonych makrocząsteczek jest specyficzna endocytoza(za pośrednictwem receptorów). W tym przypadku makrocząsteczki wiążą się z komplementarnymi receptorami na powierzchni komórki, gromadzą się w graniczącym dole, a następnie tworząc endosom, zanurzają się w cytosolu. Endocytoza receptora zapewnia akumulację określonych makrocząsteczek na jego receptorze. Nazywa się cząsteczki, które wiążą się z receptorem na powierzchni plazmalemy ligandy. Za pomocą endocytozy receptorowej w wielu komórkach zwierzęcych cholesterol jest wchłaniany ze środowiska pozakomórkowego.
Błona plazmatyczna bierze udział w usuwaniu substancji z komórki (egzocytoza). W tym przypadku wakuole zbliżają się do plazmalemmy. W punktach styku plazmolemma i błona wakuoli łączą się, a zawartość wakuoli przedostaje się do środowiska. U niektórych pierwotniaków miejsca egzocytozy na błonie komórkowej są z góry określone. Tak więc w błonie plazmatycznej niektórych orzęsków występują pewne obszary z prawidłowym ułożeniem dużych kulek integralnych białek. Mukocysty i trichocysty orzęsków, które są całkowicie gotowe do wydzielania, mają halo integralnych kulek białkowych w górnej części plazmalemmy. Te odcinki błony mukocyst i trichocyst stykają się z powierzchnią komórki. W neutrofilach obserwuje się szczególną egzocytozę. Są w stanie, w określonych warunkach, uwolnić swoje lizosomy do środowiska. W niektórych przypadkach tworzą się małe wyrostki zawierające lizosomy zawierające plazmalemę, które następnie odrywają się i przedostają do środowiska. W innych przypadkach dochodzi do wpuklenia plazmalemmy w głąb komórki i wychwytywania przez nią lizosomów znajdujących się daleko od powierzchni komórki.
Procesy endocytozy i egzocytozy są przeprowadzane przy udziale układu włóknistych składników cytoplazmy związanej z plazmolemą.
Funkcja receptorowa plazmalemmy. Jest to jedna z głównych, uniwersalnych dla wszystkich komórek, funkcji receptora plazmalemmy. Decyduje o interakcji komórek między sobą oraz ze środowiskiem zewnętrznym.
Całą różnorodność informacyjnych interakcji międzykomórkowych można schematycznie przedstawić jako łańcuch następujących po sobie reakcji sygnał-receptor-wtórny przekaźnik-odpowiedź (koncepcja sygnał-odpowiedź). Przekazywanie informacji z komórki do komórki odbywa się za pomocą cząsteczek sygnałowych, które są wytwarzane w niektórych komórkach i specyficznie wpływają na inne wrażliwe na sygnał (komórki docelowe). Cząsteczka sygnałowa - główny pośrednik wiąże się z receptorami zlokalizowanymi na komórkach docelowych, które reagują tylko na określone sygnały. Cząsteczki sygnałowe - ligandy - zbliżają się do swojego receptora jak klucz do zamka. Ligandami dla receptorów błonowych (receptorów plazmalemmy) są cząsteczki hydrofilowe, hormony peptydowe, neuroprzekaźniki, cytokiny, przeciwciała, a dla receptorów jądrowych cząsteczki rozpuszczalne w tłuszczach, hormony steroidowe i tarczycowe, witamina D. Białka błonowe lub elementy glikokaliksu mogą pełnić rolę receptorów na powierzchnia komórki - polisacharydy i glikoproteiny. Uważa się, że obszary wrażliwe na poszczególne substancje są rozproszone na powierzchni komórki lub zebrane w małych strefach. Tak więc na powierzchni komórek prokariotycznych i komórek zwierzęcych istnieje ograniczona liczba miejsc, z którymi cząsteczki wirusa mogą się wiązać. Białka błonowe (nośniki i kanały) rozpoznają, oddziałują i przenoszą tylko określone substancje. Receptory komórkowe biorą udział w przekazywaniu sygnałów z powierzchni komórki do jej wnętrza. Różnorodność i specyficzność zestawów receptorów na powierzchni komórki prowadzi do powstania bardzo złożonego systemu markerów, które umożliwiają odróżnienie własnych komórek od komórek innych. Podobne komórki oddziałują na siebie, ich powierzchnie mogą się sklejać (koniugacja u pierwotniaków, tworzenie tkanki u wielokomórkowców). Komórki, które nie dostrzegają markerów, a także te, które różnią się zestawem markerów determinujących, są niszczone lub odrzucane. Kiedy tworzy się kompleks receptor-ligand, aktywowane są białka transbłonowe: białko konwertujące, białko wzmacniające. W efekcie receptor zmienia swoją konformację i wchodzi w interakcję z prekursorem drugiego posłańca znajdującym się w komórce – posłaniec. Posłańcy mogą być zjonizowany wapń, fosfolipaza C, cyklaza adenylanowa, cyklaza guanylanowa. Pod wpływem przekaźnika następuje aktywacja enzymów biorących udział w syntezie cykliczne monofosforany - AMP Lub HMF. Te ostatnie zmieniają aktywność dwóch rodzajów enzymów kinazy białkowej w cytoplazmie komórki, prowadząc do fosforylacji wielu białek wewnątrzkomórkowych.
Najczęstszą formacją cAMP, pod wpływem której zwiększa się wydzielanie szeregu hormonów - tyroksyny, kortyzonu, progesteronu, rozpad glikogenu w wątrobie i mięśniach, częstotliwość i siła skurczów serca, osteodestrukcja i odwracanie nasila się wchłanianie wody w kanalikach nefronu.
Aktywność układu cyklazy adenylanowej jest bardzo wysoka – synteza cAMP prowadzi do dziesięciotysięcznego wzrostu sygnału.
Pod wpływem cGMP zwiększa się wydzielanie insuliny przez trzustkę, histaminy przez komórki tuczne, serotoniny przez płytki krwi i zmniejsza się tkanka mięśni gładkich.
W wielu przypadkach podczas tworzenia kompleksu receptor-ligand następuje zmiana potencjału błonowego, co z kolei prowadzi do zmiany przepuszczalności plazmalemmy i procesy metaboliczne w klatce.
Na błonie plazmatycznej znajdują się specyficzne receptory, które reagują na czynniki fizyczne. Tak więc w bakteriach fotosyntetyzujących chlorofile znajdują się na powierzchni komórki, która reaguje na światło. U zwierząt światłoczułych błona plazmatyczna zawiera cały system białka fogoreceptorowe - rodopsyny, za pomocą których bodziec świetlny jest przekształcany w sygnał chemiczny, a następnie w impuls elektryczny.
Błona komórkowa (plazmatyczna) jest półprzepuszczalną barierą oddzielającą cytoplazmę komórek od środowiska. Obecnie za podstawę w biologii przyjmuje się płynno-mozaikowy model membrany, zaproponowany w latach 70. przez J. Singera i G. Nicholsona.
Model ten opiera się na kilku podstawowych zasadach:
1. Błona składa się z podwójnej warstwy cząsteczek lipidów. Hydrofilowe, polarne części cząsteczek (głowy) znajdują się na zewnątrz błony, hydrofobowe, niepolarne części (ogon) - wewnątrz.
2. Białka błonowe są mozaikowo osadzone w dwuwarstwie lipidowej. Niektóre z nich przechodzą przez membranę (nazywane są integralnymi), inne znajdują się na zewnętrznej lub wewnętrznej powierzchni membrany (nazywane są obwodowymi).
3. Baza lipidowa błony ma właściwości cieczy (np płynny olej) i może zmieniać swoją gęstość. Lepkość błon zależy od składu lipidów i temperatury. Pod tym względem białka błonowe i same lipidy mogą swobodnie przemieszczać się wzdłuż błony i wewnątrz niej. Jest to bardzo ważna właściwość membrany, która zapewnia, że membrana spełnia wiele funkcji (patrz poniżej)
4. Błony większości wewnątrzkomórkowych organelle błonowe są zasadniczo podobne do błony plazmatycznej.
5. Pomimo wspólnej budowy błon wszystkich komórek, skład białek i lipidów w każdym typie komórki i wewnątrz komórki jest inny. Różny jest również skład zewnętrznej i wewnętrznej warstwy lipidowej.
Funkcje błony plazmatycznej
Błona spełnia w komórce cały szereg funkcji związanych z utrzymaniem integralności komórki, zapewnieniem wymiany substancji i energii pomiędzy komórką a środowisko i interakcji z innymi komórkami.
funkcja transportowa
Błona komórkowa ma właściwości półprzepuszczalnej bariery, która przepuszcza i nie przepuszcza tylko niektórych substancji i cząsteczek. Istnieje kilka rodzajów transportu przez błonę: transport bierny, transport aktywny, transport jonów, transport w opakowaniu membranowym (endo i egzocytoza).
Transport pasywny to transport substancji przez błonę z obszaru o wysokim stężeniu do obszaru o niskim stężeniu. Realizowana jest w dwóch formach: w formie dyfuzji prostej oraz w formie dyfuzji „ułatwionej”. Oba te procesy nie wymagają energii, są stosunkowo powolne i zatrzymują się, gdy stężenie substancji po obu stronach membrany wyrówna się. Szybkość dyfuzji i sama możliwość transportu substancji przez błonę zależy (oprócz stężenia) od wielu czynników: temperatury, wielkości cząsteczek, zdolności rozpuszczania się w lipidach. Substancje rozpuszczalne w tłuszczach łatwo przechodzą przez warstwy lipidowe, substancje rozpuszczalne w wodzie z trudem. W błonie znajdują się specjalne „pory” lipidowe i białkowe, przez które przechodzi dyfuzja. Prosta dyfuzja jest stosunkowo powolnym procesem, a natura przystosowała specjalne błonowe białka nośnikowe, aby przyspieszyć transport. Łączą się z transportowaną substancją i przenoszą ją z jednej strony membrany na drugą. Dla każdej grupy substancji membrana musi mieć własne nośniki. Taki proces nazywany jest „dyfuzją ułatwioną” i przebiega dziesięć razy szybciej niż dyfuzja prosta.
Transport jonowy jest rodzajem transportu biernego dla naładowanych jonów, ale ma swoje własne cechy. Białka w cytoplazmie komórki zwykle niosą ładunek ujemny na swojej powierzchni, tworząc pewne tło elektryczne w komórce. Jeśli przepływy jonów dodatnich (kationy) lub ujemnych (anionów) są kierowane do komórki, to wtedy jony dodatnie więcej wejdzie, ponieważ część kationów zostanie związana przez białka cytoplazmatyczne, zneutralizowana i stworzy dodatkową różnicę w stężeniu różnie naładowanych jonów wewnątrz i na zewnątrz komórki. Do transportu jonów w membranie służą albo specjalne pory jonowe, albo nośniki.
transport aktywny- bardzo ważna forma transport dla komórki. Dyfuzja, jeśli trwa wystarczająco długo, prowadzi do tego, że równowaga ustala się po obu stronach błony, co jest dla komórki nie do przyjęcia - to dla niej śmierć. Skład cytoplazmy i płyn śródmiąższowy bardzo się różnią. Dlatego w komórce istnieje system „aktywnego transportu”. W tym przypadku transport cząsteczek odbywa się wbrew gradientowi stężeń (od strefy niskiego stężenia do strefy wysokiego). W tym celu istnieją specjalne kompleksy błony białkowej (kanały jonowe i molekularne), które działają przy zużyciu energii. Do 40% całej energii wyprodukowanej przez ogniwo idzie na koszty transportu!
Transport w opakowaniach membranowych (endo - i egzocytoza). W wielu przypadkach komórka musi transportować przez błonę nie pojedyncze cząsteczki czy jony, ale całe kompleksy molekularne, a nawet cząsteczki. Nie przechodzą przez pory membrany. W związku z tym istnieje specjalny rodzaj transportu w komórce - transport w opakowaniu membranowym. W niektórych przypadkach dochodzi do wypukłości zewnętrznej błony plazmatycznej, przykrywającej obcą cząsteczkę (np. cząstkę pokarmu lub bakterię), zamykającą ją w pierścień błony i zanurzającą się głęboko w cytoplazmie komórki. Taki proces został odkryty przez słynnego rosyjskiego naukowca, laureata Nagrody Nobla I.I. Miecznikowa i nazwany fagocytozą. Zjawisko to zostało odkryte podczas studiów właściwości ochronne komórki krwi, które wychwytują bakterie i neutralizują je. Komórka wychwytuje mniejsze cząsteczki i kropelki cieczy, tworząc wklęsłości błony – proces ten nazywa się pinocytozą (gr. pinos – ciecz).
W rzeczywistości fagocytoza i pinocytoza to odmiany powszechnego zjawiska charakterystycznego dla większości komórek - endocytozy. Odwrotny proces endocytozy - usuwanie wszelkich substancji i produktów z komórek nazywa się egzocytozą. Na bazie transportu błonowego budowany jest cały proces wydalania i wchłaniania przez komórki sekretów i hormonów. Należy podkreślić, że endo- i egzocytoza są procesami energochłonnymi, a zatem są rodzajami aktywnego transportu.
Funkcja receptora błonowego
Zasady działania receptorów błonowych.
Komórka nieustannie otrzymuje sygnały ze środowiska zewnętrznego o obecności różnych cząsteczek sygnałowych i musi odpowiednio na te sygnały reagować, przekazując z nich informacje do komórki. W tym celu w błonie plazmatycznej wbudowane są specjalne kompleksy receptorów. Z reguły są to złożone formacje kilku cząsteczek białka (w skład receptorów mogą również wchodzić lipidy błonowe i węglowodany).
Wszystkie różne receptory błony komórkowej mają wiele wspólnych cech:
1. Receptory są specyficzne – tj. wiążą się tylko z niektórymi substancjami. Specyficzność receptora jest określona przez strukturę „miejsca aktywnego” w jego cząsteczce oraz zdolność innych cząsteczek do wiązania się z tym miejscem aktywnym.
2. Proces odbioru i transmisji sygnału do błony lub w głąb komórki odbywa się ze znacznym nakładem energii.
3. Zgodnie z zasadą działania wszystkie receptory można podzielić na trzy grupy: receptory akcja bezpośrednia; receptory pośrednie i receptory katalityczne. W pierwszym przypadku cząsteczka wiąże się z częścią receptorową kompleksu i przekazuje sygnał bezpośrednio do kanału jonowego. W drugiej wersji część receptorowa kompleksu przekazuje sygnał do kanału jonowego w błonie lub w głąb komórki poprzez system białek pomocniczych zwanych „wtórnymi posłańcami”. W trzecim wariancie część receptorowa kompleksu po interakcji z cząsteczką sygnałową zostaje aktywowana i pełni funkcje enzymu, wpływając tym samym na funkcjonowanie komórki.
Izolacyjna funkcja membrany. Kontakty międzykomórkowe
W organizm wielokomórkowy komórki są w ciągłym kontakcie ze sobą, co czasami nabiera cech ścisłej interakcji. Jest to szczególnie widoczne w tkankach graniczących ze środowiskiem zewnętrznym (powłoki, jelita, Drogi oddechowe) lub gdzie istnieje potrzeba bliskiego kontaktu komórek do skoordynowanej pracy (mięśni gładkich i mięśnia sercowego, komórki nerwowe i włókna).
Istnieją cztery rodzaje połączeń międzykomórkowych: złącza izolujące (złącze ciasne), złącza ścisłe (złącze szczelinowe), desmosomy (desmosomy) i połączenia adhezyjne (złącze adhezyjne).
Izolowanie kontaktów zasługuje na swoją nazwę - kompleksy białkowe w błonach sąsiednich komórek są połączone w taki sposób, że żadne cząsteczki i jony nie przechodzą przez ten kontakt. Ciasne połączenia umożliwiają przechodzenie małych cząsteczek i jonów, przez które może zachodzić wymiana między komórkami. W szczególności ciasne połączenia są adaptowane przez nerwy i Komórki mięśniowe do przesyłania sygnałów elektrycznych. Desmosomy są zaprojektowane do utrzymywania grupy komórek względem siebie lub innego podłoża.
Mogą szybko zniknąć i pojawić się ponownie. Styki adhezyjne są również przeznaczone do łączenia komórek ze sobą. Są bardziej nietrwałe i mogą szybko tworzyć się i znikać w razie potrzeby.
Jądro jest odpowiedzialne za przechowywanie materiału genetycznego zapisanego w DNA, a także kontroluje wszystkie procesy zachodzące w komórce. Cytoplazma zawiera organelle, z których każda ma swoje własne funkcje, takie jak na przykład synteza materia organiczna, trawienie itp. O ostatnim składniku porozmawiamy bardziej szczegółowo w tym artykule.
w biologii?
rozmawiając zwykły język, to skorupa. Jednak nie zawsze jest całkowicie nieprzenikniony. Transport niektórych substancji przez błonę jest prawie zawsze dozwolony.
W cytologii błony można podzielić na dwa główne typy. Pierwszym z nich jest błona plazmatyczna, która pokrywa komórkę. Drugi to błony organelli. Istnieją organelle, które mają jedną lub dwie błony. Komórki jednobłonowe obejmują retikulum endoplazmatyczne, wakuole i lizosomy. Plastydy i mitochondria należą do dwubłonowych.
Ponadto błony mogą znajdować się wewnątrz organelli. Zwykle są to pochodne błony wewnętrznej organelli dwubłonowych.
Jak ułożone są błony organelli dwubłonowych?
Plastydy i mitochondria mają dwie błony. Zewnętrzna błona obu organelli jest gładka, ale wewnętrzna tworzy struktury niezbędne do funkcjonowania organoidu.
Tak więc skorupa mitochondriów ma wypukłości do wewnątrz - cristae lub grzbiety. Na nich zachodzi cykl reakcji chemicznych niezbędnych do oddychania komórkowego.
Pochodnymi błony wewnętrznej chloroplastów są worki w kształcie dysku - tylakoidy. Są zbierane w stosy - ziarna. Oddzielne grana łączy się ze sobą za pomocą lameli - długich struktur uformowanych również z membran.
Budowa błon organelli jednobłonowych
Te organelle mają tylko jedną membranę. Zwykle jest to gładka błona zbudowana z lipidów i białek.
Cechy struktury błony komórkowej komórki
Błona składa się z substancji takich jak lipidy i białka. Struktura błony plazmatycznej zapewnia jej grubość 7-11 nanometrów. Większość błony składa się z lipidów. 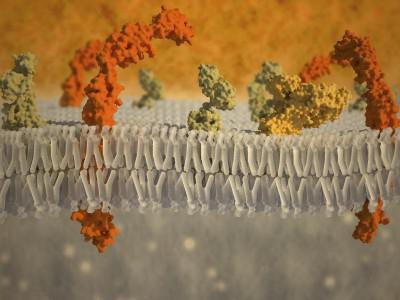
Struktura błony plazmatycznej zapewnia obecność w niej dwóch warstw. Pierwsza to podwójna warstwa fosfolipidów, a druga to warstwa białek.
Lipidy błony komórkowej
Lipidy tworzące błonę plazmatyczną dzielą się na trzy grupy: steroidy, sfingofosfolipidy i glicerofosfolipidy. Cząsteczka tego ostatniego ma w swoim składzie resztę trójwodorotlenowego alkoholu glicerolu, w którym atomy wodoru dwóch grup hydroksylowych są zastąpione łańcuchami kwasów tłuszczowych, a atom wodoru trzeciej grupy hydroksylowej jest zastąpiony resztą kwasu fosforowego , do którego z kolei przyłączona jest reszta jednej z zasad azotowych.
Cząsteczkę glicerofosfolipidu można podzielić na dwie części: głowę i ogony. Głowa jest hydrofilowa (to znaczy rozpuszcza się w wodzie), a ogony są hydrofobowe (odpychają wodę, ale rozpuszczają się w rozpuszczalnikach organicznych). Dzięki tej strukturze cząsteczkę glicerofosfolipidów można nazwać amfifilową, czyli jednocześnie hydrofobową i hydrofilową.
Sfingofosfolipidy są podobne w struktura chemiczna dla glicerofosfolipidów. Różnią się jednak od wymienionych powyżej tym, że w swoim składzie zamiast reszty glicerolu mają resztę alkoholu sfingozyny. Ich cząsteczki również mają głowy i ogony.
Poniższy rysunek wyraźnie pokazuje strukturę błony plazmatycznej.
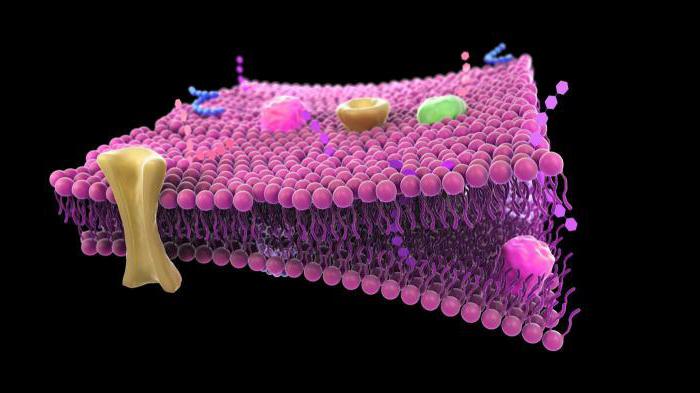
Białka błony plazmatycznej
Jeśli chodzi o białka, które tworzą strukturę błony komórkowej, są to głównie glikoproteiny.
W zależności od umiejscowienia w powłoce można je podzielić na dwie grupy: peryferyjne i integralne. Pierwsze to te, które znajdują się na powierzchni błony, a drugie to te, które penetrują całą grubość błony i znajdują się wewnątrz warstwy lipidowej.
W zależności od funkcji, jakie pełnią białka, można je podzielić na cztery grupy: enzymatyczną, strukturalną, transportową i receptorową.
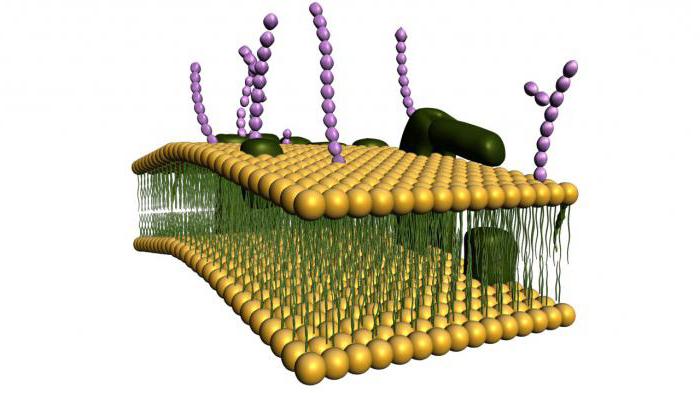
Wszystkie białka wchodzące w skład błony komórkowej nie są chemicznie związane z fosfolipidami. Dlatego mogą swobodnie poruszać się w głównej warstwie błony, gromadzić się w grupach itp. Dlatego struktury błony komórkowej komórki nie można nazwać statyczną. Jest dynamiczny, bo cały czas się zmienia.
Jaka jest rola błony komórkowej?
Struktura błony plazmatycznej pozwala jej spełniać pięć funkcji.
Pierwszym i głównym jest ograniczenie cytoplazmy. W rezultacie komórka ma stała forma i rozmiar. Ta funkcja jest zapewniona przez fakt, że błona plazmatyczna jest mocna i elastyczna.
Drugą rolą jest zaopatrzenie Ze względu na swoją elastyczność błony plazmatyczne mogą tworzyć wyrostki i fałdy na swoich połączeniach.
Następna funkcja Ściana komórkowa- transport. Dostarczają go specjalne białka. Dzięki nim odpowiednie substancje można transportować do klatki, a zbędne można z niej usuwać.
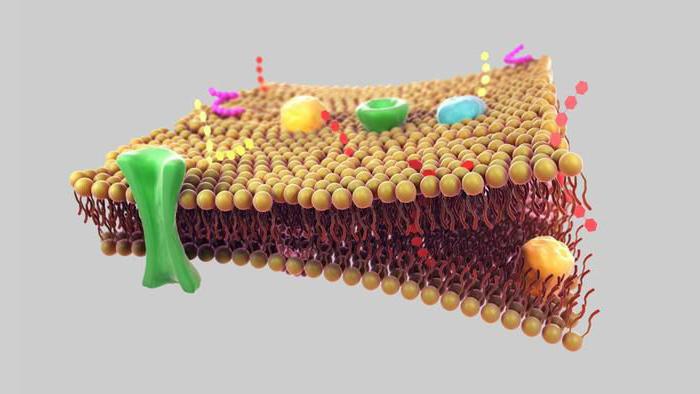
Ponadto błona plazmatyczna pełni funkcję enzymatyczną. Odbywa się to również dzięki białkom.
Ostatnią funkcją jest sygnalizacja. Dzięki temu, że białka pod wpływem określonych warunków mogą zmieniać swoją strukturę przestrzenną, błona plazmatyczna może wysyłać sygnały do komórek.
Teraz wiesz wszystko o błonach: czym jest błona w biologii, czym one są, jak ułożona jest błona plazmatyczna i błony organoidów, jakie pełnią funkcje.
Wykład nr 4.
Liczba godzin: 2
błona plazmatyczna
1.
2.
3. Kontakty międzykomórkowe.
1. Struktura błony plazmatycznej
Błona plazmatyczna lub plazmalemma, jest powierzchniową strukturą peryferyjną, która ograniczakomórki z zewnątrz i zapewniając jej połączenie z innymi komórkami i środowiskiem zewnątrzkomórkowym. Ma grubośćokoło 10 nm. Spośród innych błon komórkowych plazmalemia jest najgrubsza. Z chemicznego punktu widzenia błona plazmatyczna jest kompleks lipoproteinowy. Głównymi składnikami są lipidy (około 40%), białka (ponad 60%) i węglowodany (około 2-10%).
Lipidy są duża grupa substancje organiczne, które mają słabą rozpuszczalność w wodzie (hydrofobowość) i dobrą rozpuszczalność w rozpuszczalnikach organicznych i tłuszczach (lipofilowość).Reprezentatywnymi lipidami znajdującymi się w błonie komórkowej są fosfolipidy, sfingomieliny i cholesterol. W komórki roślinne cholesterol jest zastępowany fitosterolem. Przez rola biologiczna Białka błony komórkowej można podzielić na białka enzymatyczne, receptorowe i strukturalne. Węglowodany Plasmalemmy są częścią plazmalemmy w stanie związanym (glikolipidy i glikoproteiny).
Obecnie jest to powszechnie akceptowane płynno-mozaikowy model struktury błony biologicznej. Zgodnie z tym modelem strukturalną podstawę błony stanowi podwójna warstwa fosfolipidów inkrustowanych białkami. Ogony cząsteczek znajdują się naprzeciw siebie w podwójnej warstwie, podczas gdy bieguny pozostają na zewnątrz, tworząc hydrofilowe powierzchnie. Cząsteczki białek nie tworzą ciągłej warstwy, znajdują się w warstwie lipidowej, zanurzając się na różne głębokości (istnieją białka obwodowe, niektóre białka przenikają przez błonę, inne są zanurzone w warstwie lipidowej). Większość białek nie jest związana z lipidami błonowymi; wydają się unosić w „lipidowym jeziorze”. Dlatego cząsteczki białka mogą przemieszczać się wzdłuż błony, gromadzić się w grupach lub odwrotnie, rozpraszać się na powierzchni błony. Sugeruje to, że błona plazmatyczna nie jest statyczną, zamrożoną formacją.
Na zewnątrz plazmalemmy znajduje się warstwa epimembrany - glikokaliks. Grubość tej warstwy wynosi około 3-4 nm. Glycocalyx znajduje się w prawie wszystkich komórkach zwierzęcych. Jest związany z błoną plazmatyczną kompleks glikoproteinowy. Węglowodany tworzą długie, rozgałęzione łańcuchy polisacharydów związanych z białkami i lipidami błony komórkowej. Glikokaliks może zawierać białka enzymatyczne zaangażowane w zewnątrzkomórkowy rozkład różnych substancji. Produkty aktywności enzymatycznej (aminokwasy, nukleotydy, kwas tłuszczowy itp.) są transportowane przez błonę plazmatyczną i wchłaniane przez komórki.
Błona plazmatyczna jest stale odnawiana. Dzieje się tak poprzez sznurowanie małych pęcherzyków z jej powierzchni do komórki i osadzenie wakuoli z wnętrza komórki w błonie. Tak więc w komórce występuje stały przepływ elementów błonowych: z błony plazmatycznej do cytoplazmy (endocytoza) oraz przepływ struktur błonowych z cytoplazmy na powierzchnię komórki (egzocytoza). W krążeniu błon wiodącą rolę odgrywa układ wakuoli błonowych kompleksu Golgiego.
4. Funkcje błony plazmatycznej. Mechanizmy transportu substancji przez plazmalemę. Funkcja receptorowa plazmalemmy
Błona plazmatyczna pełni szereg ważnych funkcji:
1) Bariera.Funkcją barierową błony plazmatycznej jestograniczenie swobodnej dyfuzji substancji z komórki do komórki, zapobieganiewyciek obrotowy rozpuszczalnej w wodzie zawartości komórki. Lecz odkądjak komórka musi otrzymać niezbędne składniki odżywcze, tydzielą metaboliczne produkty końcowe, regulują wewnątrzkomórkowostężenia jonów, a następnie tworzyły specjalne mechanizmy przenoszenia substancji przez błonę komórkową.
2) Transport.Funkcja transportowa jest Zapewnienie wejścia i wyjścia różnych substancji do iz komórki. Ważną właściwością membrany jest selektywna przepuszczalność, Lub półprzepuszczalność. Łatwo przepuszcza wodę i jest rozpuszczalny w wodziegazy i odpycha cząsteczki polarne, takie jak glukoza lub aminokwasy.
Istnieje kilka mechanizmów transportu substancji przez błonę:
transport pasywny;
transport aktywny;
transport w opakowaniu membranowym.
Transport pasywny. Rozpowszechnianie -jest to ruch cząstek ośrodka, prowadzący do przeniesieniasubstancji z obszaru o wysokim stężeniu do obszaru o niskim stężeniucja. Podczas transportu dyfuzyjnego membrana działa jak bariera osmotyczna. Szybkość dyfuzji zależy od wartościcząsteczki i ich względna rozpuszczalność w tłuszczach. Im mniej razymiary cząsteczek i im bardziej są one rozpuszczalne w tłuszczach (lipofilowe), tym szybciej będą przechodzić przez dwuwarstwę lipidową.Dyfuzja może być neutralny(przelew nieodpłatnycząsteczki) i lekki(za pomocą specjalnych białeknosy). Dyfuzja ułatwiona jest szybsza niż dyfuzja neutralna.Maksymalna penetracjawoda ma zdolnośćjak jego cząsteczki są małe i pozbawione ładunku. Dyfuzja wody przez komórkinazywa się membrana osmo sumZakłada się, że w komórcemembrana do penetracjizasadniczo woda i niektóre jonyistnieją specjalne „pory”. Ich liczbamały, a średnica jestokoło 0,3-0,8 nm. Dyfuzują najszybciej przez membranę dobrze rozpuszczalny w lipidach dwuwarstwa cząsteczki, na przykład O, i nienaładowane cząsteczki polarnely o małej średnicy (SO, mo szewina).
Transport cząsteczek polarnych (zcukry, aminokwasy), wdrożonedostarczane za pomocą specjalnego transportu membranowegonazywa się białka ułatwiona dyfuzja. Takie białka sąznajdują się we wszystkich typach błon biologicznych, a każda jest specyficzna Białko ny jest przeznaczone do przenoszenia cząsteczek określonej klasy sa. Białka transportowe są transbłonowe, ich łańcuch polipeptydowy kilkakrotnie przecina dwuwarstwę lipidową, tworząc się ma przejścia. Gwarantuje to przekazanie konkretnychsubstancji przez membranę bez bezpośredniego kontaktu z nią.Istnieją dwie główne klasy białek transportowych: wiewiórki- przewoźnicy (transporterzy) I kanałotwórczy białka (białekanały Ki). Białka nośnikowe przenoszą cząsteczki przez błonę, najpierw zmieniając ich konfigurację. Białka tworzące kanały tworzą wypełnione błony woda porowa. Gdy pory są otwarte, cząsteczki określonych substancji(zwykle jony nieorganiczne o odpowiedniej wielkości i ładunku) przechodzą przez nie. Jeśli cząsteczka transportowanej substancji nie ma ładunku, to kierunek transportu określa gradient stężeń. Jeśli cząsteczka jest naładowana, to podczas jej transportu, oprócz gradientu, con stężenie, wpływa również ładunek elektryczny membrany (membranapotencjał). Wewnętrzna strona plazmalemmy jest zwykle ładowana z negatywny w stosunku do otoczenia. Potencjał błony ułatwia przenikanie dodatnio naładowanych jonów do wnętrza komórki i zapobiega przedostawaniu się ujemnie naładowanych jonów.
transport aktywny. Transport aktywny to ruch substancji wbrew gradientowi elektrochemicznemu. Jest to zawsze przeprowadzane przez białka trans.tragarzy i blisko spokrewnieni zan ze źródłem energiiOjej. W transferze białek chiki mają działki wiązanie z transportemsubstancja wiążąca. Im więcej takich tkov komunikuje się z rzeczamiim wyższa prędkośćwzrost transportu. Nazywa się selektywne przeniesienie jednej substancji uniport. Przeprowadza się transfer kilku substancji kotran systemy sportowe. Jeśli transfer idzie w jednym kierunku -Ten symportować, jeśli naprzeciw antyport. Więc,na przykład glukoza jest transportowana z płynu zewnątrzkomórkowego do komórki w sposób jednokierunkowy. Przenoszenie glukozy i Na 4 z przewodu pokarmowego lubkanaliki nerkowe odpowiednio do komórek jelita lub krwi są przeprowadzane symportalnie, a transfer C1 ~ i HCO "jest antyportem. Przypuszczalnie Przyjmuje się, że podczas przenoszenia następuje odwracalna konformacja zmiany w przenośniku, który umożliwia przemieszczanie się podłączonych do niego substancji.
Przykład białka nośnikowego stosowanego do transportusubstancje, energia uwalniana podczas hydrolizy ATP wynosiNa + -pompa K+, znajduje się w błonie plazmatycznej wszystkich komórek. Na+-K Pompa działa na zasadzie antyportu, pompowania wai Na „z ogniwa i do wnętrza ogniwa przeciwko ich elektrochemicznym właściwościom gradienty. Gradient Na+ wytwarza ciśnienie osmotyczne, utrzymuje objętość komórek oraz zapewnia transport cukrów i aminokwasównokwasy. Działanie tej pompy pochłania jedną trzecią całej energii niezbędnej do życiowej aktywności komórek.Podczas badania mechanizmu działania Na + - K + pompa została zainstalowanawiadomo, że jest to enzym ATPaza i enzym transbłonowy białko tegralu. W obecności Na+ i ATP pod działaniem ATP-końcowy fosforan jest oddzielany od ATP i przyłączany do resztykwas asparaginowy na cząsteczce ATPazy. Cząsteczka ATPazy Fosforylowany, zmienia swoją konfigurację i Na+ pochodzi z komórki. Po wycofaniu Na K" jest zawsze transportowany z komórki do komórki. W tym celu odcinany jest od ATPazy wcześniej przyłączony fosforan w obecności K. Enzym jest defosforylowany, przywraca swoją konfigurację, a K 1 jest "wpompowywany" do komórki.
ATPaza składa się z dwóch podjednostek, dużej i małej.Duża podjednostka składa się z tysięcy reszt aminokwasowych,kilkakrotnie przekraczając dwuwarstwę. Posiada katalizator aktywność i jest zdolny do odwracalnej fosforylacji i defosfobruzdowany. Duża podjednostka po stronie cytoplazmatycznejnie ma miejsc wiążących Na+ i ATP, a na zewnątrz -miejsca wiązania K + i ouabainy. Mała podjednostka jestglikoproteina i jej funkcja nie jest jeszcze znana.
Na+-K pompa ma efekt elektrogeniczny. Usuwa trzydodatnio naładowany jon Na f z celi i wprowadza dwajon K W rezultacie prąd przepływa przez membranę, tworząc elektronpotencjał ric o wartości ujemnej w wewnętrznej części komórki w stosunku do jej zewnętrznej powierzchni. Na "-K + pompa reguluje objętość komórek, kontroluje stężenie substancjiwewnątrz komórki, utrzymuje ciśnienie osmotyczne, bierze udział w tworzeniu potencjału błonowego.
Transport w opakowaniu membranowym. Transfer przez błonę makrocząsteczek (białek, kwasów nukleinowych)partia, polisacharydy, lipoproteiny) i inne cząstki są przeprowadzane poprzez sekwencyjne tworzenie i łączenie otoczonychpęcherzyki związane z błoną (pęcherzyki). Proces transportu pęcherzykowegoprzechodzi przez dwa etapy. Na początkubłona pęcherzykowa i plazmalemiatrzymać się razem, a następnie połączyć.Do przejścia etapu 2 jest to koniecznedimo, aby cząsteczki wody były tobąsą zatłoczone przez oddziałujące dwuwarstwy lipidowe, które zbliżają się do siebie na odległość 1-5 nm. uważa że proces ten jest aktywnyspecjalny białka fuzyjne(Oni dotychczas izolowane tylko od wirusów). Transport pęcherzykowy maważna cecha - zaabsorbowane lub wydzielane makrocząsteczki,zawarte w pęcherzykach, zwykle niemieszalny z innymi makromolamiculae lub organelli komórkowych. Pu pęcherzyki mogą łączyć się ze specyficznymi membrany, które zapewniająChivaet wymiana makrocząsteczek międzydu przestrzeni zewnątrzkomórkowej izawartość komórki. podobniemakrocząsteczki są przenoszone z jednego przedziału komórkowego do drugiego.
Nazywa się transport makrocząsteczek i cząstek do wnętrza komórki endo cytoza.W tym przypadku transportowane substancje są otoczone herbatąbłonie plazmatycznej powstaje pęcherzyk (wakuola), któryktóry przenosi się do komórki. W zależności od rozmiaru obrazubąbelki, istnieją dwa rodzaje endocytozy - pinocytoza i fagocytoza.
pinocytozazapewnia wchłanianie cieczy i rozpuszczonychsubstancje w postaci małych bąbelków ( D =150 nm). Fagocytoza -jest wchłanianie dużych cząstek, mikroorganizmówwezwanie lub fragmenty organelli, komórek. Jednocześnie tworząXia duże pęcherzyki, fagosomy lub wakuole ( d -250 nm lub więcej). Na funkcja fagocytarna pierwotniaków - forma odżywiania. U ssaków funkcję fagocytarną pełnią makrofagi i neutprofile, które chronią organizm przed infekcją poprzez wchłanianie atakujących drobnoustrojów. W utylizację zaangażowane są również makrofagistarych lub uszkodzonych komórek i ich fragmentów (w organizmieludzkie makrofagi zjadają dziennie ponad 100 starych erytrytydówrotocyty). Fagocytoza rozpoczyna się dopiero po połknięciu cząstkiwiąże się z powierzchnią fagocytu i aktywuje wyspecjalizowanekomórki receptorowe ye. Kojarzenie cząstek z określonym rereceptorów błonowych powoduje powstawanie pseudopodiów, któreżyto otacza cząstkę i łącząc się na krawędziach, tworzy bańkę -fagosom.Tworzenie fagosomów i właściwa fagocytozachodzi tylko wtedy, gdy jest w trakcie otaczania cząstkijest w ciągłym kontakcie z receptorami plazmalemmy, jakby „stagnował”. migająca błyskawica”.
Znaczna część materiału wchłanianego przez komórkę przez endocytosis, kończy się w lizosomach. Duże cząstki, w tymnadzieja pokładana w fagosomy które następnie łączą się z lizosomami, tworząc fagolizosomy. Ciecz i makrocząsteczki wchłaniane podczaspinocytoza, są początkowo przenoszone do endosomów, którełączą się z lizosomami, tworząc endolizosomy. Jestem obecna różne enzymy hydrolityczne obecne w lizosomachro zniszczyć makrocząsteczki. produkty hydrolizy (aminokwasypartie, cukry, nukleotydy) są transportowane z lizosomów do cytozolu, gdzie są wykorzystywane przez komórkę. Większość elementów membrany pęcherzyki endocytarne z fagosomów i endosomów powracają w wyniku egzocytozy do błony plazmatycznej i tam ponownie znikająliza. Głównym biologicznym znaczeniem endocytozy jest istnieje odbiór bloków budulcowych z powodu wewnątrzkomórkowego trawienie makrocząsteczek w lizosomach.
Wchłanianie substancji w komórkach eukariotycznych rozpoczyna się wzjalizowane obszary błony plazmatycznej, tzwjesteśmy X graniczące doły. O mikrografach elektronowychdoły wyglądają jak inwazje błony plazmatycznej, cytoplazmyktórego strona maty pokryta jest włóknistą warstwą. warstwa jakgraniczyłoby z placem małych dołów malemmy. Doły zajmują około 2 procnad powierzchnią błony komórkowejjesteśmy eukariontami. W ciągu minuty doły pogłębiają się i pogłębiają Xia, zostają wciągnięci do klatki, a następnie, zwężający się u nasady, rozszczepiony,tworząc pęcherzyki z frędzlami.Ustalono, że odfibroblast błony matycznejtov w ciągu jednej minutyokoło jednej czwartejmembrany w postaci obramowanego pu zyrkow. Bąbelki szybko się gubią ich granicę i zdobyć drogęzdolność do fuzji z lizosomem
Endocytoza może być niespecyficzne(składowy)I konkretny(chwytnik).Na niespecyficzna endocytoza komórka przejmuje kontrolępochłania substancje zupełnie mu obce, na przykład cząstki sadzy,barwniki. Najpierw cząsteczki osadzają się na glikokaliksie plazmalemma. Szczególnie dobrze wytrącony (adsorbowany) na dodatnio naładowane grupy białek, ponieważ niesie je glikokaliks ładunek ujemny. Następnie zmienia się morfologia komórkimembrany. Może albo zatonąć, tworząc wklęsłości(wklęsłość) lub odwrotnie, tworzą wyrostki, które wydają się sumować, oddzielając małe objętości płynne środowisko. Bardziej charakterystyczne jest powstawanie wgnieceń dla komórek nabłonka jelitowego, ameby i wyrostków - dla fagocytów i fibroblasty. Procesy te mogą być blokowane przez inhibitoryoddechowy. Powstałe pęcherzyki to pierwotne endosomy, które mogą się łączyć siebie, powiększając się. W przyszłości dołączą mieszają się z lizosomami, zamieniając się w endolizosom - środek trawiący nowa wakuola. Intensywność niespecyficznej pinocytozy w fazie ciekłej doszalenie wysoki. Makrofagi tworzą do 125, a komórki nabłonkowe drobnojelita do tysiąca pinosomów na minutę. Obfitość pinosomów prowadzi do tego, że plazmalemma jest szybko zużywana na tworzenie wieluobecność małych wakuoli. Regeneracja błony jest dość szybka.tro podczas recyklingu w procesie egzocytozy w wyniku powrotu wakuoles i ich włączenie do plazmalemmy. W makrofagach całe osoczeKlasyczna membrana jest wymieniana w ciągu 30 minut, aw fibroblastach w ciągu 2 godzin.
Bardziej efektywny sposób wchłaniania z płynu pozakomórkowegomakrocząsteczek specyficznych dla kości konkretny en docytoza(za pośrednictwem receptorów). Makrocząsteczki w tymwiążą się z komplementarnymi receptorami na powierzchnikomórki gromadzą się w graniczącym dole, a następnie, tworząc endosom, są zanurzane w cytosolu. Endocytoza receptora zapewnia akumulację określonych makrocząsteczek na jego receptorze.Cząsteczki, które wiążą się na powierzchni plazmalemy z receptoremnazywa się torus ligandy. Z pomocą receptora endocytozą w wielu komórkach zwierzęcych jest wchłanianiezewnątrzkomórkowy cholesterolśrodowisko.
Błona plazmatyczna bierze udział w usuwaniu substancji z komórki (egzocytoza). W tym przypadku wakuole zbliżają się do plazmalemmy. W punktach styku plazmolemma i błona wakuoli łączą się, a zawartość wakuoli przedostaje się do środowiska.U niektórych pierwotniaków miejsca egzocytozy na błonie komórkowej są z góry określone. A więc w błonie plazmatycznej niektóre orzęski rzęskowe mają pewne obszary z prawidłowym ułożeniem dużych kulek integralnych białek. Namukocysty i trichocysty orzęsków całkowicie gotowe do wydzielenia, w górnej części plazmalemmy znajduje się korona integralnych kuleczekbiałka. Te sekcje błony mukocyst i trichocyst soprikaprzylegać do powierzchni komórki.W neutrofilach obserwuje się szczególną egzocytozę. Oni widząmogą być uwalniane do środowiska w określonych warunkachwysadź swoje lizosomy. W niektórych przypadkach tworzą się małe wyrostki zawierające lizosomy zawierające plazmalemę, które następnie odrywają się i przedostają do środowiska. W innych przypadkach dochodzi do wpuklenia plazmalemmy w głąb komórki i wychwytywania przez nią lizosomów, zlokalizowanych nyh daleko od powierzchni komórki.
Procesy endocytozy i egzocytozy są przeprowadzane przy udziale układu włóknistych składników cytoplazmy związanej z plazmolemą.
Funkcja receptorowa plazmalemmy. Ten głównym, uniwersalnym dla wszystkich komórek, jest refunkcja receptorowa plazmalemmy. Definiuje interakcjękomórki między sobą oraz z otoczeniem.
Całą różnorodność informacyjnych interakcji międzykomórkowych można schematycznie przedstawić jako łańcuch następujących po sobiereakcje sygnał-receptor-wtórny posłaniec-odpowiedź (pojęcie sygnał-odpowiedź).Sygnały przekazują informacje z komórki do komórkimolekuły nye, które są wytwarzane w niektórych komórkach i specjalnefizycznie wpływać na inne wrażliwe na sygnał (komórki-mi sheni). Cząsteczka sygnałowa - główny pośrednik wiążący etsya z receptorami zlokalizowanymi na komórkach docelowych reagują tylko dla niektórych sygnałów. Cząsteczki sygnałowe - ligandy- zbliżają się do swojego receptora jak klucz do zamka. Ligand-mi dla receptorów błonowych (receptorów plazmalemmy) jestcząsteczki hydrofilowe, hormony peptydowe, neuromedia tori, cytokiny, przeciwciała, a dla receptorów jądrowych - tłuszcz cząsteczki rozpuszczalne, hormony steroidowe i tarczycowe, witamina DJako receptory na wierzchukomórki mogą działać jako białkamembrany lub elementy glikokalityczneca - polisacharydy i glikoproteiny.Uważa się, że wrażliwy narozdzielać obszary substancji, rozpraszaćsan wzdłuż powierzchni komórki lubbran w małe paski. Tak, napowierzchnia komórek prokariotycznychi komórek zwierzęcych istnieją graniceustaloną liczbę miejsc, z którymi mogąwiążą cząstki wirusa. ja jawiewiórki (nosiciele i canaly) uczyć się, wchodzić w interakcje i przekazywaćnosić tylko niektóre substancje.Receptory komórkowe biorą udział wprzekazywanie sygnałów z powierzchni komórki do wnętrza.Różnorodność i specyfikarów receptorów na powierzchni komórkiprowadzi do bardzo złożonego systemujesteśmy znacznikami do odróżnieniawłasne komórki od obcych. Podobne komórkiwchodzą ze sobą w interakcje, ich powierzchnie mogą się sklejać (koniugacja wpierwotniaki, tworzenie tkanek w organizmach wielokomórkowych). Komórki nie postrzegająwspólne znaczniki, jak i te różniące siębor markerów determinującychsą rozdarte lub odrzucone.Po utworzeniu kompleksu receptor-ligand,białka transbłonowe: konwerter białek, wzmacniacz białek.W rezultacie receptor zmienia swoją konformację i oddziaływanienie z komórkowym prekursorem drugiego posłańca ka- posłaniec.Posłańcami mogą być zjonizowany wapń, fosfolipiddla C cyklaza adenylanowa, cyklaza guanylanowa. Pod wpływem posłańcaaktywacja enzymów biorących udział w syntezie cykliczne monofosforany - AMP Lub HMF. Te ostatnie zmieniają składnik aktywówObecność dwóch rodzajów enzymów kinazy białkowej w cytoplazmie komórki, prowadząca do fosforylacji licznych białek wewnątrzkomórkowych.
Najczęstsza formacja cAMP, pod działaniemzwiększa się wydzielanie szeregu hormonów – tyroksyny, kortyzonu, progesteronu, zwiększa się rozpad glikogenu w wątrobie i mięśniach,tętno i siła, osteodestrukcja, rewers wchłanianie wody w kanalikach nefronu.
Aktywność układu cyklazy adenylanowej jest bardzo wysoka – synteza cAMP prowadzi do dziesięciotysięcznego wzrostu sygnału.
Pod wpływem cGMP następuje wydzielanie insuliny przez trzustkę, histaminy przez komórki tuczne, serotoninybocytów, tkanka mięśni gładkich jest zmniejszona.
W wielu przypadkach po utworzeniu kompleksu receptor-ligandnastępuje zmiana potencjału błonowego, co z kolei prowadzi do zmiany przepuszczalności plazmalemmy i metabolizmuniektóre procesy w komórce.
Błona plazmatyczna zawiera specyficzne receptory tori reagujące na czynniki fizyczne. Tak więc w bakteriach fotosyntetyzujących chlorofile znajdują się na powierzchni komórki,reagujące na światło. U zwierząt światłoczułych w osoczuW żrącej błonie znajduje się cały system białek fogoreceptorowych -rodopsyny, za pomocą których przekształca się bodziec świetlny jest przekształcany w sygnał chemiczny, a następnie w impuls elektryczny.
3. Kontakty międzykomórkowe
U zwierząt wielokomórkowych plazmolemma bierze udział w tworzeniu połączenia międzykomórkowe zapewniając interakcje międzykomórkowe. Istnieje kilka rodzajów takich struktur.
§ Prosty kontakt.Prosty kontakt występuje wśród większości przylegających do siebie komórek różnego pochodzenia. Reprezentuje zbieżność błon plazmatycznych sąsiednich komórek w odległości 15-20 nm. W tym przypadku zachodzi interakcja warstw glikokaliksu sąsiednich komórek.
§ Mocny (zamykający) styk. Przy takim połączeniu zewnętrzne warstwy dwóch błon plazmatycznych są jak najbliżej siebie. Zbliżenie jest tak gęste, że dochodzi do pewnego rodzaju łączenia odcinków błon plazmatycznych dwóch sąsiednich komórek. Fuzja membran nie zachodzi na całym obszarze ścisłego kontaktu, ale jest serią punktowych zbieżności membran. Rolą ścisłego kontaktu jest mechaniczne połączenie komórek ze sobą. Obszar ten jest nieprzenikalny dla makrocząsteczek i jonów, dlatego blokuje, odgradza szczeliny międzykomórkowe (a wraz z nimi środowisko wewnętrzne organizmu) od środowiska zewnętrznego.
§ Plaster adhezji lub desmosom. Desmosom to mały obszar o średnicy do 0,5 µm. W strefie desmosomu po stronie cytoplazmy znajduje się obszar cienkich włókienek. Funkcjonalna rola desmosomów polega głównie na mechanicznym połączeniu między komórkami.
§ Luka w kontakcie lub nexus. Przy tego rodzaju kontakcie błony plazmatyczne sąsiednich komórek są oddzielone szczeliną 2-3 nm na odcinku 0,5-3 µm. W strukturze plazmolemów znajdują się specjalne kompleksy białkowe (koneksony). Jeden konekson na błonie plazmatycznej komórki dokładnie przeciwstawia się koneksonowi na błonie plazmatycznej sąsiedniej komórki. W rezultacie kanał jest tworzony z jednej komórki do drugiej. Koneksony mogą się kurczyć, zmieniając średnicę kanału wewnętrznego, a tym samym uczestniczyć w regulacji transportu cząsteczek między komórkami. Ten rodzaj połączenia występuje we wszystkich grupach tkanek. Funkcjonalną rolą złącza szczelinowego jest przenoszenie jonów i małych cząsteczek z komórki do komórki. Tak więc w mięśniu sercowym pobudzenie, które opiera się na procesie zmiany przepuszczalności jonów, jest przenoszone z komórki do komórki przez nexus.
§ Kontakt synaptyczny lub synapsa. Synapsy to obszary kontaktu między dwiema komórkami wyspecjalizowanymi w jednokierunkowej transmisji pobudzenia lub hamowania z jednego elementu do drugiego. Ten rodzaj połączenia jest charakterystyczny dla tkanki nerwowej i występuje zarówno między dwoma neuronami, jak i między neuronem a jakimś innym elementem. Błony tych komórek są oddzielone przestrzenią międzykomórkową - szczeliną synaptyczną o szerokości około 20-30 nm. Błona w obszarze kontaktu synaptycznego jednej komórki nazywana jest presynaptyczną, druga - postsynaptyczną. W pobliżu błony presynaptycznej ujawnia się ogromna liczba małych wakuoli (pęcherzyków synaptycznych) zawierających neuroprzekaźnik. W momencie przejścia impulsu nerwowego pęcherzyki synaptyczne wyrzucają neuroprzekaźnik do szczeliny synaptycznej. Mediator oddziałuje z miejscami receptorowymi błony postsynaptycznej, co ostatecznie prowadzi do przeniesienia impulsu nerwowego. Oprócz przekazywania impulsu nerwowego, synapsy zapewniają sztywne połączenie między powierzchniami dwóch oddziałujących ze sobą komórek.
§ Plazmodesma.Ten rodzaj komunikacji międzykomórkowej występuje w roślinach. Plazmodesmy to cienkie kanaliki rurkowe, które łączą dwie sąsiednie komórki. Średnica tych kanałów wynosi zwykle 40-50 nm. Plazmodesmy przechodzą przez ścianę komórkową, która oddziela komórki. W młodych komórkach liczba plazmodesmy może być bardzo wysoka (do 1000 na komórkę). Wraz ze starzeniem się komórek ich liczba maleje z powodu pęknięć wraz ze wzrostem grubości ściany komórkowej. Funkcjonalną rolą plazmodesmy jest zapewnienie międzykomórkowego krążenia roztworów zawierających składniki odżywcze, jony i inne związki. Plasmodesmy infekują komórki wirusami roślinnymi.
Wyspecjalizowane struktury błony plazmatycznej
Plazmalemma wielu komórek zwierzęcych tworzy wyrostki różnych struktur (mikrokosmki, rzęski, wici). Najczęściej znajduje się na powierzchni wielu komórek zwierzęcych mikrokosmki. Te wyrostki cytoplazmy, ograniczone plazmalemmą, mają kształt walca z zaokrąglonym wierzchołkiem. Mikrokosmki są charakterystyczne dla komórek nabłonka, ale występują również w komórkach innych tkanek. Mikrokosmki mają około 100 nm średnicy. Ich liczba i długość są różne dla różne rodzaje komórki. Znaczenie mikrokosmków polega na znacznym wzroście powierzchni powierzchni komórki. Jest to szczególnie ważne dla komórek biorących udział w absorpcji. Tak więc w nabłonku jelitowym na 1 mm 2 powierzchni znajduje się do 2x10 8 mikrokosmków.
[Poprzedni wykład] [Spis treści] [Następny wykład]