Bakterie są wokół nas. Istnieją pożyteczne i chorobotwórcze, tj. bakterie chorobotwórcze. W tym artykule znajdziesz ogólne informacje o bakteriach, a także listę nazw bakterii chorobotwórczych i chorób, które wywołują.
Bakterie są wszędzie, w powietrzu, wodzie, żywności, glebie, głębinach oceanów, a nawet na szczycie Mount Everestu. Różne rodzaje bakterie żyją na ludzkim ciele, a nawet w jego wnętrzu. Na przykład dużo pożyteczne bakterieżyje w układ trawienny. Pomagają kontrolować wzrost bakterii chorobotwórczych, a także pomagają układowi odpornościowemu zwalczać infekcje. Wiele bakterii zawiera enzymy, które pomagają rozkładać wiązania chemiczne w żywności, którą spożywamy, a tym samym pomagają nam uzyskać optymalne odżywianie. Bakterie, które żyją na ludzkim ciele, nie powodując żadnych chorób ani infekcji, są znane jako bakterie kolonialne.
Kiedy dana osoba otrzymuje skaleczenie lub uraz, który prowadzi do naruszenia integralności bariery skórnej, niektóre organizmy oportunistyczne uzyskują dostęp do ciała.
Jeśli dana osoba jest zdrowa i ma silny układ odpornościowy, może oprzeć się takiej niechcianej inwazji. Jeśli jednak stan zdrowia danej osoby jest zły, wynikiem jest rozwój chorób wywoływanych przez bakterie. Bakterie powodujące problemy zdrowotne nazywane są ludzkimi bakteriami chorobotwórczymi. Te chorobotwórczy bakterie mogą również dostać się do organizmu przez żywność, wodę, powietrze, ślinę i inne płyny ustrojowe. Lista bakterii chorobotwórczych jest ogromna. Zacznijmy od kilku przykładów chorób zakaźnych.
Przykłady chorób zakaźnych
paciorkowce
Paciorkowce to powszechnie występujące bakterie w organizmie człowieka. Jednak niektóre szczepy paciorkowców mogą powodować różne choroby u ludzi. Bakterie chorobotwórcze, takie jak paciorkowce ropotwórcze (paciorkowce grupy A), powodują bakteryjne zapalenie gardła, tj. ból gardła. Nieleczona dusznica bolesna może wkrótce doprowadzić do ostrej gorączki reumatycznej i zapalenia kłębuszków nerkowych. Inne infekcje to powierzchowna piodermia i, co najgorsze, martwicze zapalenie powięzi (choroba wywoływana przez bakterie, które jedzą miękkie chusteczki).
gronkowce
Staphylococcus, w szczególności Staphylococcus aureus, są najczęstszymi bakteriami chorobotwórczymi dla człowieka. Obecne są na skórze i błonach śluzowych i wykorzystują każdą okazję do wywołania zakażenia powierzchownego lub ogólnoustrojowego. Przykłady chorób wywoływanych przez te bakterie obejmują miejscowe infekcje ropne mieszki włosowe, powierzchowne ropne zapalenie skóry i zapalenie mieszków włosowych. Gronkowce mogą również powodować poważne infekcje, takie jak zapalenie płuc, bakteriemia oraz infekcje ran i kości. Ponadto Staphylococcus aureus wytwarza pewne toksyny, które mogą powodować zatrucia pokarmowe i wstrząs toksyczny.
Przykłady chorób zakaźnych obejmują również:
Ta lista chorób zakaźnych jest długa. Poniżej znajduje się tabela, z której można dowiedzieć się o innych chorobach zakaźnych, a także o bakteriach, które je wywołują.
Lista bakterii chorobotwórczych
| Bakterie chorobotwórcze człowiek | Choroba zakaźna |
| Czynnik sprawczy wąglika (Bacillus anthracis) | krosta wąglika Płucny wąglik Wąglik żołądkowo-jelitowy |
| Pałeczka krztuśca (Bordetella pertussis) | Krztusiec Wtórne bakteryjne zapalenie płuc (powikłanie) |
| Borrelia burgdorferi (Borrelia burgdorferi) | Borelioza przenoszona przez kleszcze (choroba z Lyme) |
| Brucella abortus (Brucella abortus) Brucella canis (Brucella canis) Brucella melitensis (Brucella melitensis) Brucella suis (Brucella suis) |
Bruceloza |
| Campylobacter jejuni (Campylobacter jejuni) | Ostre zapalenie jelit |
| Chlamydia zapalenie płuc (Chlamydia pneumoniae) | pozaszpitalne infekcje dróg oddechowych |
| Chlamydia psittaci (Chlamydia psittaci) | Ornitoza (gorączka papugi) |
| Chlamydia trachomatis (Chlamydia trachomatis) | Nierzeżączkowe zapalenie cewki moczowej Trachoma Noworodkowe wtrętowe zapalenie spojówek Limfogranuloma weneryczna |
| Clostridium botulinum (Clostridium botulinum) | Botulizm |
| Clostridium difficile (Clostridium difficile) | rzekomobłoniaste zapalenie jelita grubego |
| Pałeczka zgorzeli gazowej ( Clostridium perfringens ) |
zgorzel gazowa Ostry zatrucie pokarmowe Beztlenowe zapalenie tkanki łącznej |
| Bacillus tężca (Clostridium tetani) | Tężec |
| Bacillus błonicy (Corynebacterium diphtheriae) | Błonica |
| Enterococcus kałowy (Enterococcus faecalis) Enterococcus facium (Enterococcus faecium) |
Zakażenia szpitalne |
| coli Escherichia coli | infekcje dróg moczowych Biegunka zapalenie opon mózgowych u niemowląt |
| Enterotoksyczna Escherichia coli (ETEC) | Biegunka podróżnika |
| Enteropatogenna Escherichia coli Enteropatogenna E. coli | Biegunka u niemowląt |
| E. coli O157:H7 (E. coli O157:H7) | Zapalenie okrężnicy Zespół hemolityczno-mocznicowy |
| Czynnik sprawczy tularemii (Francisella tularensis) | Tularemia |
| Hemophilus influenzae (Haemophilus influenzae) | Bakteryjne zapalenie opon mózgowych Górne infekcje drogi oddechowe Zapalenie płuc Zapalenie oskrzeli |
| Helicobacter pylori ( Helicobacter pylori) | wrzód trawienny czynnik ryzyka raka żołądka Chłoniak z komórek B przewód pokarmowy |
| Legionella pneumophila (Legionella pneumophila) | Choroba legionistów (legionelloza) Gorączka Pontiac |
| Leptospira chorobotwórcza (Leptospira interrogans) | Leptospiroza |
| Listeria monocytogenes (Listeria monocytogenes) | Listerioza |
| Mycobacterium trąd (Mycobacterium leprae) | Trąd (choroba Hansena) |
| Mycobacterium tuberculosis (Mycobacterium tuberculosis) | Gruźlica |
| Mycoplasma pneumoniae (Mycoplasma pneumoniae) | Mykoplazmowe zapalenie płuc |
| Gonokok (Neisseria gonorrhoeae) | Rzeżączka Okulistyka noworodków Septyczne zapalenie stawów |
| Meningokoki (Neisseria meningitidis) |
infekcje meningokokowe w tym zapalenie opon mózgowych Zespół Friederiksena-Waterhouse'a |
| Pseudomonas aeruginosa (Pseudomonas aeruginosa) | Miejscowe infekcje oczu, uszu, skóry, dróg moczowych i oddechowych Infekcje żołądkowo-jelitowe Infekcje centralne system nerwowy Infekcje ogólnoustrojowe (bakteremia) wtórne zapalenie płuc Infekcje kości i stawów Zapalenie wsierdzia |
| Rickettsia rickettsia (Rickettsia rickettsii) | szczypce dur plamisty |
| Salmonella typhi (Salmonella typhi) | dur brzuszny Czerwonka Zapalenie jelita grubego |
| Tyfus myszy (Salmonella typhimurium) | Salmonelloza (zapalenie żołądka i jelit oraz zapalenie jelit) |
| Shigella koszatka (Shigella sonnei) | Czerwonka bakteryjna/Shigelloza |
| Staphylococcus aureus(Staphylococcus aureus) | Koagulaza dodatnia infekcje gronkowcowe: Zlokalizowane infekcje skóry Rozproszone choroby skóra (liszajec) Głębokie ropienie, miejscowe infekcje Pikantny infekcyjne zapalenie wsierdzia Posocznica (posocznica) Martwicze zapalenie płuc Toksyczność Wstrząs zakaźno-toksyczny Gronkowcowe zatrucie pokarmowe |
| Staphylococcus naskórka (Staphylococcus epidermidis) | Infekcje wszczepionych protez, takich jak zastawki serca i cewniki |
| Staphylococcus saprophyticus (Staphylococcus saprophyticus) | zapalenie pęcherza moczowego u kobiet |
| Streptococcus agalactia (Streptococcus agalactiae) | Zapalenie opon mózgowych i posocznica u noworodków Zapalenie błony śluzowej macicy u kobiet po porodzie Zakażenia oportunistyczne (posocznica i zapalenie płuc) |
| Streptococcus pneumoniae (Streptococcus pneumoniae) | Ostre bakteryjne zapalenie płuc i zapalenie opon mózgowych u dorosłych Zapalenie ucha środkowego i zapalenie zatok u dzieci |
| Paciorkowiec ropotwórczy (Streptococcus pyogenes) | Paciorkowcowe zapalenie gardła purpurowa gorączka gorączka reumatyczna liszajec i róża sepsa poporodowa Martwicze zapalenie powięzi |
| Treponema pallidum ( Treponema blada) | Syfilis kiła wrodzona |
| Vibrio cholerae (Vibrio cholerae) | Cholera |
| Czynnik sprawczy dżumy (Yersinia pestis) | Plaga Dżuma dżumowe zapalenie płuc |
To jest lista bakterii chorobotwórczych i przykładów chorób zakaźnych. Ludzkie bakterie chorobotwórcze mogą powodować świetna ilość poważna choroba, epidemie i pandemie. Prawdopodobnie słyszałeś o czarnej zarazie średniowiecza, wywoływanej przez bakterię Yersinia pestis, była to najbardziej śmiercionośna pandemia w historii ludzkości. Wraz z rozwojem standardów higieny osobistej i czystości znacznie zmniejszyła się częstość występowania epidemii i pandemii.
Wideo
Choroby te obejmują ostre infekcje dróg oddechowych, niektóre zapalenia płuc, odmiedniczkowe zapalenie nerek, szkarlatynę, kiłę, salmonellozę, tężec, dżumę, rzeżączkę, gruźlicę, różę, zapalenie wsierdzia i wiele innych. Ich osobliwością jest to, że są wywoływane przez mikroorganizmy, które posiadają ścianę komórkową i unikalny zestaw czynników ochronnych i agresywnych.
Co to jest bakteria
Bakteria to jednokomórkowy mikroorganizm, który ma ścianę komórkową, w przeciwieństwie do wirusów i prionów.
Ze względu na rozwój chorób u ludzi wszystkie bakterie dzielą się na:
- patogenny;
- warunkowo patogenny;
- nie chorobotwórcze.
Bakterie chorobotwórcze, gdy dostaną się do organizmu człowieka, zawsze powodują wywołaną przez nie chorobę. Ta ich cecha jest określona przez obecność specjalnych urządzeń przeznaczonych do agresji wobec ludzi. Wśród tych czynników agresji można wyróżnić:
Te mikroorganizmy obejmują:
- Bacillus Luffner, który powoduje błonicę;
- salmonella, która powoduje salmonellozę;
- Bacillus anthracis, który powoduje wąglika;
- gonococcus, który powoduje rzeżączkę;
- blady treponema, powodujący kiłę i inne.
Warunkowo chorobotwórcze mikroorganizmy mogą żyć na ludzkim ciele, normalnie nie powodując choroby, ale w pewnych warunkach stają się chorobotwórcze.
Bakterie te obejmują:
- coli;
- paciorkowiec;
- gronkowiec;
- proteus i kilka innych.
Mikroorganizmy niepatogenne w żadnych okolicznościach nie powodują chorób u ludzi.
Co się dzieje, gdy patogeny dostają się do organizmu człowieka
Aby patogen spowodował chorobę u ludzi, musi zostać spełnionych kilka warunków.
- Liczba bakterii musi być wystarczająco duża. Jedna czy dwie bakterie praktycznie nie są w stanie zarazić człowieka, a niespecyficzne i swoiste systemy obronne ludzkiego organizmu z łatwością poradzą sobie z tak znikomym zagrożeniem.
- Bakterie muszą być kompletne, to znaczy muszą mieć wszystkie swoje właściwości chorobotwórcze. Osłabione szczepy bakterii również nie stanowią zagrożenia dla człowieka, są jedynie w stanie poinformować układ odpornościowy o swoich właściwościach, aby w przyszłości układ odpornościowy mógł odpowiednio rozpoznać swojego wroga. Działanie różnych szczepionek opiera się na tej zasadzie.
- Bakterie muszą dostać się do miejsca w ciele, w którym mogą się przyczepić, infiltrować, zakorzenić i rozmnażać. Jeśli np. salmonella dostanie się na skórę człowieka, a nie do przewodu pokarmowego, to taka osoba nie zachoruje na salmonellozę. Dlatego przed jedzeniem należy umyć ręce.
- Ludzki układ odpornościowy nie powinien być gotowy na atak bakterii. Jeśli odporność zostanie zaszczepiona naturalnie lub sztucznie, w większości przypadków bakterie nie będą w stanie przebić się przez mechanizmy obronne organizmu. Wręcz przeciwnie, jeśli odporność nie spotkała się z tego typu bakteriami lub jest znacznie osłabiona (np. przy AIDS), oznacza to, że taki organizm ma otwarte wszystkie bramy do inwazji infekcji bakteryjnej.
 Jeśli wszystkie te warunki są spełnione, dochodzi do zakaźnej infekcji bakteryjnej. Ale każda infekcja ma okres wylęgania, który może trwać od kilku godzin ( zatrucie pokarmowe), do kilku lat (trąd, borelioza przenoszona przez kleszcze). W tym okresie bakterie namnażają się, osiedlają, przyzwyczajają do nowych warunków bytowania, rozprzestrzeniają się po całym świecie środowiska wewnętrzne organizm.
Jeśli wszystkie te warunki są spełnione, dochodzi do zakaźnej infekcji bakteryjnej. Ale każda infekcja ma okres wylęgania, który może trwać od kilku godzin ( zatrucie pokarmowe), do kilku lat (trąd, borelioza przenoszona przez kleszcze). W tym okresie bakterie namnażają się, osiedlają, przyzwyczajają do nowych warunków bytowania, rozprzestrzeniają się po całym świecie środowiska wewnętrzne organizm.
Od momentu pojawienia się pierwszych objawów choroby kończy się okres inkubacji, a sama choroba rozpoczyna się z odpowiednim obrazem klinicznym. Z niektórymi zakaźnymi chorobami bakteryjnymi organizm radzi sobie sam, z innymi może potrzebować pomocy z zewnątrz.
Jak diagnozuje się infekcję bakteryjną?
Rozpoznanie infekcji bakteryjnej przeprowadza się następującymi metodami:
- za pomocą mikroskopu (mikroskopia z barwieniem);
- za pomocą siewu (materiał z bakteriami jest rozmazany na specjalnej pożywce i pozostawiony do ogrzania przez około tydzień, po czym patrzą, co tam wyrosło i wyciągają wnioski);
- poprzez wykrywanie antygenów i przeciwciał ( metody laboratoryjne: ELISA, RIF, PCR i inne);
- zakażając zwierzęta (metoda biologiczna: szczury, myszy zakaża się materiałem, następnie otwiera i bada wnętrze pod mikroskopem)
Jak leczy się infekcję bakteryjną?
Główną metodą leczenia chorób bakteryjnych jest chemioterapia przeciwbakteryjna. Istnieje wiele grup i odmian antybiotyków, które są przeznaczone ściśle pewne grupy mikroorganizmy.
DO leczenie antybakteryjne należy traktować poważnie, ponieważ niewłaściwe zarządzanie antybiotykami w Ostatnio spowodowały prawdziwe katastrofy we współczesnym świecie. Faktem jest, że mikroorganizmy, ze względu na swoje wrodzone mutacje, stopniowo przyzwyczajają się do antybiotyków i prędzej czy później pojawia się tzw. antybiotykooporność mikroorganizmów. Innymi słowy, antybiotyki po prostu przestają na nie działać, a wtedy trzeba zastosować silniejsze antybiotyki (antybiotyki rezerwowe), które wciąż są w stanie oprzeć się bakteriom.
Tym samym medycyna jest pośrednio winna narodzin infekcji związanych z jej stosowaniem opieka medyczna(ISOMP). Wcześniej takie infekcje nazywano szpitalnymi (HAI) lub szpitalnymi (HI). Te infekcje różnią się od zwykłych tym, że standardowe antybiotyki nie działają na nie i można je pokonać tylko za pomocą silniejszych leków.
Ostatnio pojawiły się wielolekooporne szczepy zakażenia gruźlicą. Nie ma tak wielu leków przeciw gruźlicy. Medycyna wykorzystuje głównie to, co zostało opracowane w czasach sowieckich. Od tego czasu rozwój phthisiology wyraźnie się zatrzymał. A teraz żadne leki przeciwgruźlicze (jest ich tylko 6) nie mają wpływu na ten typ zakażenia gruźlicą. Innymi słowy, osoby z tą formą infekcji są nieuleczalne. Ale co więcej, są śmiertelne dla otaczających ich ludzi, ponieważ są nosicielami.
Przyczyny oporności na antybiotyki
 Oporność na antybiotyki jest procesem naturalnym, ponieważ bakterie, podobnie jak wszystkie żywe organizmy, są w stanie przystosować się do zmieniających się warunków środowisko. Ale na szybkość tego procesu znacząco wpłynęło nieumiejętne użycie leki przeciwbakteryjne. Kiedy antybiotyki sprzedawano w aptekach bez recepty, każdy (albo, co gorsza, farmaceuta!) mógł „zabawić się” w lekarza i przepisać sobie kurację. Ale z reguły leczenie to kończyło się po 1-2 dniach, po ustąpieniu objawów choroby. Doprowadziło to do tego, że bakterie nie zostały całkowicie zniszczone, ale przeszły w inne formy (formy L) i długi czasżył w „ciemnych zakamarkach” ciała „wyleczonych” ludzi, czekając na odpowiedni moment. Wraz ze spadkiem odporności z tego czy innego powodu, ponownie zmienili się w swoje pierwotne formy i spowodowali tę samą chorobę, którą można było przenieść na innych ludzi i tak dalej.
Oporność na antybiotyki jest procesem naturalnym, ponieważ bakterie, podobnie jak wszystkie żywe organizmy, są w stanie przystosować się do zmieniających się warunków środowisko. Ale na szybkość tego procesu znacząco wpłynęło nieumiejętne użycie leki przeciwbakteryjne. Kiedy antybiotyki sprzedawano w aptekach bez recepty, każdy (albo, co gorsza, farmaceuta!) mógł „zabawić się” w lekarza i przepisać sobie kurację. Ale z reguły leczenie to kończyło się po 1-2 dniach, po ustąpieniu objawów choroby. Doprowadziło to do tego, że bakterie nie zostały całkowicie zniszczone, ale przeszły w inne formy (formy L) i długi czasżył w „ciemnych zakamarkach” ciała „wyleczonych” ludzi, czekając na odpowiedni moment. Wraz ze spadkiem odporności z tego czy innego powodu, ponownie zmienili się w swoje pierwotne formy i spowodowali tę samą chorobę, którą można było przenieść na innych ludzi i tak dalej.
Z tego powodu antybiotyki są przepisywane na 5-7-10-14 dni. Bakterie muszą zostać całkowicie zniszczone, a nie przyzwyczajone do antybiotyków.
Ale jest jeszcze jeden problem z antybiotykoterapią. Polega to na tym, że oprócz bakterie chorobotwórcze podczas przyjmowania antybiotyków niszczone są również przydatne (laktobakterie, bifidobakterie przewodu pokarmowego). Może to być początkiem przejścia warunkowo patogennej flory przewodu pokarmowego w chorobotwórczą i doprowadzić do rozwoju takiego powikłania antybiotykoterapii jak dysbakterioza, która wymaga leczenia w postaci stymulacji wzrostu korzystna mikroflora jelitowa.
Jak postępuje infekcja bakteryjna?
Wraz z rozwojem bakterii proces zakaźny jednym z pierwszych objawów będzie gorączka. Jest zwykle wysoka. Gorączka jest spowodowana faktem, że kompleks LPS ściany komórkowej bakterii po jej zniszczeniu przedostaje się do krwioobiegu i wraz z przepływem krwi dociera do podwzgórza, czyli do znajdującego się w nim ośrodka termoregulacji. Kompleks LPS przesuwa punkt nastawy ośrodka termoregulacji i organizm „myśli”, że jest zimno i zwiększa produkcję ciepła, zmniejsza wymianę ciepła.
 Gorączka jest reakcją obronną organizmu, gdyż temperatura ciała dochodząca do 39 stopni pobudza do pracy układ odpornościowy. Jeśli temperatura ciała wzrośnie powyżej 39 stopni, należy ją obniżyć paracetamolem lub pośrednio antybiotykami (obniżenie temperatury ciała w ciągu 24-48 godzin od rozpoczęcia antybiotykoterapii jest oznaką odpowiednio dobranego leku przeciwbakteryjnego) .
Gorączka jest reakcją obronną organizmu, gdyż temperatura ciała dochodząca do 39 stopni pobudza do pracy układ odpornościowy. Jeśli temperatura ciała wzrośnie powyżej 39 stopni, należy ją obniżyć paracetamolem lub pośrednio antybiotykami (obniżenie temperatury ciała w ciągu 24-48 godzin od rozpoczęcia antybiotykoterapii jest oznaką odpowiednio dobranego leku przeciwbakteryjnego) .
Innym przejawem bakteryjnego procesu zakaźnego jest zespół zatrucia. Objawia się pogorszeniem samopoczucia, apatią, obniżeniem nastroju, możliwymi bólami głowy, bólami mięśni i stawów, nudnościami, wymiotami i tym podobnymi. Aby złagodzić te objawy, musisz dużo pić. ciepła woda(co najmniej 2 litry dziennie). Nadmiar wody rozrzedzi toksyny bakteryjne, zmniejszając ich stężenie, a także usunie część z nich z moczem.
Te dwa znaki zapalenie bakteryjne są uniwersalne dla prawie wszystkich infekcji. Wszystkie inne objawy wynikają z cech konkretnego patogenu, jego egzotoksyn i innych czynników agresji.
Osobno należy powiedzieć o takich specyficznych infekcjach, jak gruźlica, kiła, trąd (który jednak już nie istnieje). Infekcje te różnią się nieco od pozostałych. Faktem jest, że istnieją od dawna z ludzkością i Ludzkie ciało trochę się do nich przyzwyczaiłem. Z reguły nie powodują jasnego obrazu zakaźnego procesu bakteryjnego, objawy kliniczne z nimi nie są jasne. Ale powodują specyficzne stany zapalne w organizmie, które można zobaczyć pod mikroskopem (ziarniniaki). Choroby te są leczone z dużym trudem, a leczenie polega jedynie na eliminacji klinicznych objawów choroby. Obecnie nie jest możliwe całkowite oczyszczenie organizmu człowieka z tych patogenów (erradication).
Jak organizm walczy z bakteriami
 Układ odpornościowy organizmu składa się z dwóch podsystemów: humoralnego i komórkowego.
Układ odpornościowy organizmu składa się z dwóch podsystemów: humoralnego i komórkowego.
Układ humoralny ma na celu tworzenie specjalnych przeciwciał przeciwko antygenom patogenów. Te przeciwciała, podobnie jak pociski, są w stanie przebić ścianę komórkową bakterii. Dzieje się to w następujący sposób. Gdy szkodliwa bakteria dostaje się do organizmu, w jakiś sposób spotyka się ze specjalnymi komórkami ochronnymi układu odpornościowego - makrofagami. Te makrofagi atakują i pożerają bakterię, badając w ten sposób jej strukturę antygenową (w rzeczywistości patrzą na „skórę” bakterii i szukają na niej „wypukłości” - antygenów, do których można przyczepić przeciwciało, aby zrobiło dziury w tej skóra). Po zbadaniu bakterii makrofagi, zwane już komórkami prezentującymi antygen (APC), trafiają do władze centralne układ odpornościowy (czerwony szpik kostny) i zgłaszają bakterie. Dają rozkaz wytworzenia przeciwciał (białek), które będą mogły przyczepić się do danej ściany komórkowej. Utworzone przeciwciała są po prostu uwalniane do krwioobiegu. Kiedy przeciwciało znajdzie swój antygen, przyłącza się do niego. Z krwi do tego kompleksu „antygen-przeciwciało” zaczynają przyłączać się białka, które zmieniają konfigurację przestrzenną przeciwciała w taki sposób, że przeciwciało rozwija się, wygina i przebija (perforuje) ścianę bakteryjną, powodując jej śmierć.
Odporność komórkowa działa inaczej. Białe krwinki (leukocyty), jak armia żołnierzy, masowo atakują wroga, używając do tego specjalnych enzymów proteolitycznych, nadtlenku wodoru i innej broni. Na zewnątrz wygląda jak ropa. To właśnie dzięki takiej obfitości enzymów proteolitycznych w ropie jest w stanie rozpuścić otaczające tkanki i wybić się, usuwając w ten sposób obce substancje z organizmu.
Co dzieje się po wyzdrowieniu
Powrót do zdrowia może być kliniczny, laboratoryjny lub całkowity.
powrót do zdrowia klinicznego oznacza brak jakichkolwiek objawów związanych z tą chorobą.
Kuracja laboratoryjna umieścić, gdy niemożliwe jest wykrycie jakichkolwiek laboratoryjnych oznak obecności tej choroby.
Pełne wyzdrowienie będzie, gdy ludzkie ciało nie pozostanie drobnoustroje chorobotwórcze który spowodował tę chorobę.
Oczywiście nie wszystkie zakaźne procesy bakteryjne kończą się wyzdrowieniem. Czasami jest to również możliwe zgony. Możliwe jest również przejście ostrego procesu zakaźnego w przewlekły (wyzdrowienie kliniczne).
Wideo: Oporność bakterii na antybiotyki
Pomimo aktywnego rozwoju medycyny problem chorób zakaźnych, w tym bakteryjnych, jest bardzo istotny. Bakterie spotyka się na każdym kroku: w transporcie publicznym, w pracy, w szkole. Niewiarygodne liczby zaludniają klamki, pieniądze, myszy komputerowe, Telefony komórkowe. Nie ma na naszej planecie miejsc, w których nie byłoby tych mikroorganizmów. Występują w soli wody umarłych morzach, w gejzerach, których temperatura przekracza 100ºС, w wodach oceanu na głębokości 11 km, w atmosferze na wysokości 41 km, nawet w reaktorach jądrowych.
Klasyfikacja bakterii
Bakterie to małe stworzenia, które można zobaczyć tylko pod mikroskopem, o średniej wielkości 0,5-5 mikronów. wspólna cecha wszystkich bakterii jest brak jądra, co odnosi się do prokariotów. Istnieje kilka sposobów ich rozmnażania: rozszczepienie binarne, pączkowanie, dzięki egzosporom lub fragmentom grzybni. Bezpłciowy sposób reprodukcja polega na replikacji DNA w komórce i jej późniejszym podziale na dwie części.
W zależności od kształtu bakterie dzielą się na:
- cocci - kulki;
- w kształcie pręta;
- spirilla - skręcone nici;
- vibrios to zakrzywione pręty.
Choroby grzybicze, wirusowe i bakteryjne, w zależności od mechanizmu przenoszenia i umiejscowienia patogenu, dzielimy na jelitowe, krwionośne, oddechowe i zewnętrzne.
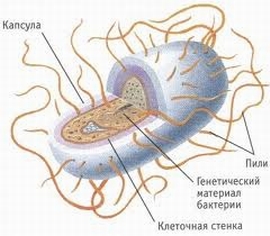
Struktura bakterii i infekcji
Cytoplazma jest główną częścią komórka bakteryjna, w których zachodzi metabolizm, tj. syntezę składników, w tym wpływających na jego patogeniczność, z składniki odżywcze. Obecność w cytoplazmie enzymów, katalizatorów o charakterze białkowym determinuje metabolizm. Zawiera również „jądro” bakterii - nukleoid, bez określonego kształtu i zewnętrznie ograniczony przez błonę. uderzyć różne substancje do komórki i wydalanie produktów przemiany materii odbywa się przez błonę cytoplazmatyczną.
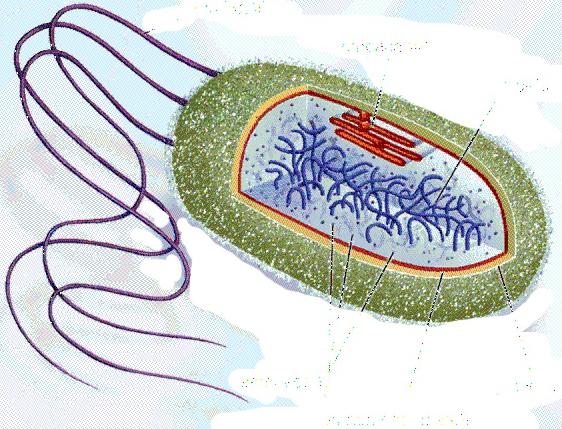 Otacza błonę cytoplazmatyczną Ściana komórkowa, na którym może znajdować się warstwa śluzu (torebki) lub wici, przyczyniając się do aktywny ruch bakterie w płynach.
Otacza błonę cytoplazmatyczną Ściana komórkowa, na którym może znajdować się warstwa śluzu (torebki) lub wici, przyczyniając się do aktywny ruch bakterie w płynach.
Pokarmem dla bakterii są różnorodne substancje: od prostych np. dwutlenek węgla, jony amonowe, aż do kompleksu związki organiczne. Na aktywność życiową bakterii ma również wpływ temperatura i wilgotność otoczenia, obecność lub brak tlenu. Wiele rodzajów bakterii do przeżycia niekorzystne warunki zdolne do tworzenia zarodników. właściwości bakteriobójcze kto znalazł szerokie zastosowanie zarówno w medycynie, jak iw przemyśle gorączka lub ciśnienie promieniowanie ultrafioletowe niektóre związki chemiczne.
Właściwości chorobotwórczości, wirulencji i inwazyjności
Patogeniczność odnosi się do zdolności pewien rodzaj mikroorganizmy powodują bakterie choroba zakaźna. Jednak u tego samego gatunku jego poziom może mieścić się w szerokim zakresie, w którym to przypadku mówi się o zjadliwości - stopniu zjadliwości szczepu. Patogeniczność mikroorganizmów wynika z toksyn, które są produktami ich życiowej aktywności. Wiele bakterii chorobotwórczych nie jest w stanie rozmnażać się w makroorganizmach, jednak wydzielają one najsilniejsze egzotoksyny wywołujące chorobę. Dlatego istnieje również pojęcie inwazyjności - zdolności do rozprzestrzeniania się w makroorganizmie. Ze względu na opisane powyżej właściwości, w określonych warunkach mogą powodować wysoce chorobotwórcze mikroorganizmy śmiertelne choroby, a słabo chorobotwórcze bakterie są po prostu obecne w organizmie, nie powodując żadnych szkód.
Rozważ niektóre ludzkie choroby bakteryjne, których lista jest zbyt duża, aby opisać wszystko w jednym artykule.
Infekcje jelitowe
salmonelloza. Czynnikiem sprawczym może być około 700 gatunków serowarów z rodzaju Salmonella. Do zakażenia może dojść drogą wodną, kontaktową z gospodarstwem domowym lub drogą pokarmową. Rozmnażanie się tych bakterii, któremu towarzyszy gromadzenie się toksyn, jest możliwe w różne produkty wartość odżywczą i zostaje zachowana, gdy podczas gotowania nie zostaną poddane wystarczającej obróbce cieplnej. Źródłem infekcji mogą być również zwierzęta domowe, ptaki, gryzonie, chorzy ludzie.
Konsekwencją działania toksyn jest zwiększenie wydzielania płynu do jelita i zwiększenie jego perystaltyki, wymiotów i biegunek, które prowadzą do odwodnienia. Po przejściu okresu inkubacji, który trwa od 2 godzin do 3 dni, temperatura wzrasta, pojawiają się dreszcze, ból głowy, kolkowe bóle brzucha, nudności, a po kilku godzinach - częste wodniste i cuchnące stolce. Te choroby bakteryjne trwają około 7 dni.
W niektórych przypadkach mogą wystąpić powikłania w postaci ostrej niewydolność nerek, wstrząs infekcyjno-toksyczny, choroby ropno-zapalne czy powikłania zakrzepowe.
Dur brzuszny i paratyfus A i B. Ich patogenami są S. paratyphi A, S. paratyphi B, Salmonella typhi. Drogi przenoszenia – żywność, woda, zakażone przedmioty, źródło – chory. Cechą choroby jest sezonowość lato-jesień. 
Czas trwania okresu inkubacji wynosi 3 - 21 dni, najczęściej 8 - 14, po czym następuje stopniowy wzrost temperatury do 40ºС. Gorączce towarzyszy bezsenność, ból głowy, brak apetytu, bladość skóry, wysypka różowata, powiększenie wątroby i śledziony, wzdęcia, zatrzymanie stolca, rzadziej biegunka. Chorobie towarzyszą również niedociśnienie tętnicze, bradykardia, delirium, letarg. Możliwe komplikacje- zapalenie płuc, zapalenie otrzewnej, krwawienie z jelit.
zatrucie pokarmowe. Jego czynnikami sprawczymi są warunkowo patogenne mikroorganizmy. Bakterie chorobotwórcze dostają się do organizmu z produkty żywieniowe, które albo nie zostały poddane obróbce cieplnej, albo zostały poddane niewystarczającej obróbce cieplnej. Najczęściej jest to nabiał lub produkty mięsne, Cukiernia.
Czas trwania okresu inkubacji wynosi od 30 minut do jednego dnia. Infekcja objawia się nudnościami, wymiotami, wodnisty stolec do 15 razy dziennie, dreszcze, bóle brzucha, gorączka. Więcej ciężkie przypadki towarzyszą choroby obniżone ciśnienie, tachykardia, drgawki, suchość błon śluzowych, skąpomocz, wstrząs hipowolemiczny. Choroba trwa od kilku godzin do trzech dni.
Czerwonka. Czynnikiem sprawczym jednej z najczęstszych infekcji jelitowych jest bakteria z rodzaju Shigella. Mikroorganizmy dostają się do organizmu podczas spożywania skażonej żywności, wody, przez artykuły gospodarstwa domowego I brudne ręce. Źródłem zakażenia jest osoba chora.
Okres inkubacji może wynosić od kilku godzin do tygodnia, zwykle 2-3 dni. Choroba pojawia się często płynny stolec z zanieczyszczeniami śluzem i krwią, skurczowymi bólami w lewym i podbrzuszu, gorączką, zawrotami głowy, dreszczami, bólem głowy. Ona też jest w towarzystwie niedociśnienie tętnicze, tachykardia, wzdęcia, palpacja okrężnica esowata. Czas trwania choroby zależy od ciężkości: od 2-3 do 7 dni lub dłużej.
escherichioza. Ta choroba jest również nazywana biegunką podróżnych. Nazywa się to coli Escherichia coli szczepy enteroinwazyjne lub enterotoksygenne.
W pierwszym przypadku okres inkubacji trwa od 1 do 6 dni. Objawami choroby są luźne stolce i skurczowe bóle brzucha, rzadziej parcia. Czas choroby 3-7 dni z lekkim zatruciem.  W drugim przypadku okres utajony może trwać do 3 dni, po czym zaczynają się wymioty, częste luźne stolce, przerywana gorączka i ból brzucha. Bakterie chorobotwórcze w dużym stopniu dotykają dzieci młodym wieku. Choroba towarzyszy ciepło, gorączka, niestrawność. Takie choroby bakteryjne mogą być powikłane zapaleniem wyrostka robaczkowego, zapaleniem pęcherzyka żółciowego, zapaleniem dróg żółciowych, zapaleniem opon mózgowych, zapaleniem wsierdzia, chorobami zapalnymi dróg moczowych.
W drugim przypadku okres utajony może trwać do 3 dni, po czym zaczynają się wymioty, częste luźne stolce, przerywana gorączka i ból brzucha. Bakterie chorobotwórcze w dużym stopniu dotykają dzieci młodym wieku. Choroba towarzyszy ciepło, gorączka, niestrawność. Takie choroby bakteryjne mogą być powikłane zapaleniem wyrostka robaczkowego, zapaleniem pęcherzyka żółciowego, zapaleniem dróg żółciowych, zapaleniem opon mózgowych, zapaleniem wsierdzia, chorobami zapalnymi dróg moczowych.
kampylobakterioza. Jest to powszechna infekcja wywoływana przez bakterię Campylobacter fetus jejuni, która występuje u wielu zwierząt domowych. Możliwe są również zawodowe choroby bakteryjne człowieka.
Okres inkubacji trwa 1 - 6 dni. Chorobie towarzyszy gorączka, zapalenie żołądka i jelit, ciężkie zatrucie, wymioty, obfite luźne stolce. W rzadkich przypadkach uogólniona postać choroby.
Leczenie i zapobieganie infekcjom jelitowym
Z reguły za skuteczne leczenie zalecana jest hospitalizacja pacjenta, ponieważ większość z tych chorób może prowadzić do powikłań, a także zmniejszać ryzyko szerzenia się zakażenia. Leczenie obejmuje kilka głównych punktów.
Na infekcja jelitowa niezbędny ścisłe przestrzeganie oszczędna dieta. Lista dozwolonych produktów: spowolnienie aktywność silnika jelita i zawierające znaczące ilości garbniki - jagody, czeremcha, mocna herbata, a także puree zbożowe, śluzowate zupy, kisiele, twarogi, krakersy, dania rybne i mięsne na parze. W żadnym wypadku nie należy jeść smażonych i tłustych, surowych warzyw i owoców.
W przypadku infekcji toksycznych płukanie żołądka jest obowiązkowe w celu usunięcia patogenów z błony śluzowej przewodu pokarmowego. Detoksykację i nawodnienie przeprowadza się za pomocą podanie doustne do organizmu roztworów soli glukozy.
Leczenie bakteryjnych chorób jelit koniecznie wiąże się z normalizacją stolca. W tym celu najczęściej stosowanym środkiem jest „Indometocyna”, preparaty wapnia, różne sorbenty, z których najtańszy, Węgiel aktywowany. Ponieważ chorobom bakteryjnym towarzyszy dysbakterioza, przepisywane są leki normalizujące mikroflorę jelitową (Linex, Bifidumbacterin itp.)
Dotyczący środki przeciwbakteryjne, wówczas w zależności od rodzaju patogenu można stosować antybiotyki z grupy monobaktamów, penicylin, cefalosporyn, tetracyklin, chloramfenikoli, karbapenemów, aminoglikozydów, polimyksyn, chinolonów, fluorochinolonów, nitrofuranów, a także mieszane preparaty sulfonamidów.
Aby zapobiec chorobom bakteryjnym człowieka, lista codziennych czynności powinna zawierać następujące pozycje: higiena osobista, staranna obróbka cieplna niezbędnej żywności, mycie warzyw i owoców przed jedzeniem, używanie przegotowanej lub butelkowanej wody, krótkotrwałe przechowywanie łatwo psującej się żywności.
Infekcje dróg oddechowych
W drogach oddechowych bakterie i infekcje wirusowe które zazwyczaj są sezonowe. Bakteryjne i choroby wirusowe osoby różnią się przede wszystkim lokalizacją. Wirusy wpływają na cały organizm, podczas gdy bakterie działają lokalnie. Najczęstszymi chorobami wirusowymi są SARS i grypa.
Choroby bakteryjne są po infekcjach drogi oddechowe:
Zapalenie migdałków(zapalenie migdałków) mogą być powodowane zarówno przez wirusy, jak i bakterie - mykoplazmy, paciorkowce, chlamydie (A. Haemolyticum, N. Gonorrhoeae, C. Diphtheriae). Towarzyszyły mu zmiany migdałki podniebienne, ból gardła, dreszcze, ból głowy, wymioty.
Zapalenie nagłośni. Czynnikami sprawczymi są bakterie S. Pneumoniae, S. Pyogenes i S. Aureus. Choroba charakteryzuje się zapaleniem nagłośni, któremu towarzyszy zwężenie krtani, szybkie pogorszenie, ból gardła, gorączka.  Ze względu na ciężki przebieg choroby wymagana jest obowiązkowa hospitalizacja chorego.
Ze względu na ciężki przebieg choroby wymagana jest obowiązkowa hospitalizacja chorego.
Zapalenie zatok- zapalenie zatoki szczękowe spowodowane przez bakterie, które dostały się do jamy nosowej przez krew lub z Górna szczęka. Charakteryzuje się początkowo miejscowym bólem, który następnie rozprzestrzenia się, zamieniając się w „ból głowy”.
Zapalenie płuc. Jest to choroba płuc, podczas której zaatakowane są pęcherzyki płucne i oskrzela końcowe. Bakterie chorobotwórcze - paciorkowce, gronkowce, Klebsiella pneumoniae, pneumokoki, Haemophilus influenzae i Escherichia coli. Chorobie towarzyszy kaszel z plwociną, gorączka, duszność, dreszcze, bóle głowy i ból w mięśniach, utrata apetytu, zwiększone zmęczenie, osłabienie zatrucia.
Leczenie i zapobieganie infekcjom dróg oddechowych
W leczeniu zakażeń hospitalizację chorego przeprowadza się tylko w przypadkach ciężkiego i zaniedbanego przebiegu choroby. Głównymi środkami są antybiotyki, dobierane indywidualnie w zależności od rodzaju patogenu. Leczenie nosogardzieli można przeprowadzić za pomocą lokalnych środków antyseptycznych („Gexoral”, „Septifril”, „Stopangin”, „Kameton”, „Ingalipt”). Dodatkowo zaleca się stosowanie inhalacji, fizjoterapii, ćwiczeń oddechowych, Terapia manualna, masaż klatka piersiowa. Za pomocą połączone fundusze o działaniu antyseptycznym i przeciwbólowym na początku choroby (leki z Rośliny lecznicze, „TeraFlu”, „Anti-Angina”, „Strepsils”, NovaSept) prawdopodobnie nie ma potrzeby dalszego stosowania antybiotyków.
Profilaktyka chorób bakteryjnych układu oddechowego obejmuje następujące czynności: spacery świeże powietrze, ćwiczenia oddechowe, profilaktyczne inhalacje, zaprzestanie palenia tytoniu, stosowanie opatrunków z gazy bawełnianej w kontakcie z chorym.
Infekcje powłoki zewnętrznej
Na ludzkiej skórze, która ma pewne właściwości chroniące ją przed mikroorganizmami, znajduje się ogromna ilość pokojowo żyjących bakterii. Jeśli te właściwości zostaną naruszone (nadmierne nawilżenie, choroby zapalne, urazy) mikroorganizmy mogą powodować infekcję. Choroby bakteryjne skóry występuje również wtedy, gdy bakterie chorobotwórcze przedostają się z zewnątrz.
Liszajec. Istnieją dwa rodzaje chorób: pęcherzowa, wywołana przez gronkowce i niepęcherzowa, której czynnikami sprawczymi są S. aulreuls i S. Pyogenes.
Choroba objawia się w postaci czerwonych plam, które zamieniają się w pęcherzyki i krosty, które łatwo się otwierają, tworząc grube żółtawo-brązowe łuski. 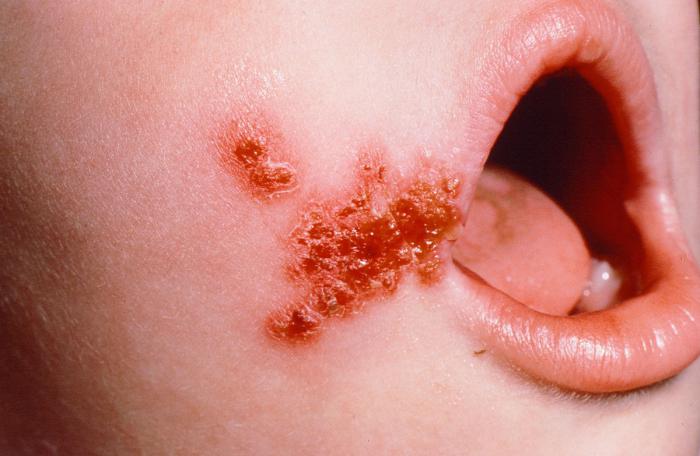 Postać pęcherzowa charakteryzuje się pęcherzami o wielkości 1-2 cm W skomplikowanych chorobach bakteryjnych powoduje zapalenie kłębuszków nerkowych.
Postać pęcherzowa charakteryzuje się pęcherzami o wielkości 1-2 cm W skomplikowanych chorobach bakteryjnych powoduje zapalenie kłębuszków nerkowych.
Czyraki i karbunkuły. Choroba występuje z głęboką penetracją gronkowców mieszki włosowe. Infekcja tworzy konglomerat zapalny, z którego następnie pojawia się ropa. Typowe lokalizacje karbunkułów to twarz, nogi, tylny koniec szyja.
Róża i cellulit. To są infekcje wpływając na skórę i tkanki leżące poniżej, których czynnikami sprawczymi są paciorkowce z grup A, G, C. W porównaniu z różą lokalizacja cellulitu jest bardziej powierzchowna.
Typowa lokalizacja róż - twarz, cellulit - łydki. Obie choroby są często poprzedzone urazem, uszkodzeniem skóry. Powierzchnia skóry jest czerwona, obrzęknięta, z nierównymi brzegami objętymi stanem zapalnym, czasem z pęcherzykami i pęcherzami. Powiązane funkcje choroby - gorączka i dreszcze.
Róża i zapalenie tkanki łącznej mogą powodować powikłania, objawiające się zapaleniem powięzi, zapaleniem mięśni, zakrzepicą zatoki jamistej, zapaleniem opon mózgowych, różnymi ropniami.
Leczenie i zapobieganie infekcjom skóry
Zaleca się miejscowe lub miejscowe leczenie chorób bakteryjnych skóry człowieka akcja ogólna w zależności od ciężkości i rodzaju infekcji. Stosowane są również różne środki antyseptyczne. W niektórych przypadkach ich stosowanie trwa przez długi czas, w tym przez zdrowych członków rodziny w celach profilaktycznych. 
szef środek zapobiegawczy, zapobiegającym występowaniu infekcji skórnych, jest higiena osobista, stosowanie indywidualnych ręczników, a także ogólny wzrost odporność.
Infekcje zwierząt
Należy również wspomnieć o bakteryjnych chorobach zwierzęcych przenoszonych na człowieka, zwanych zooantroponozami. Źródłem zakażenia są zwierzęta domowe i dzikie, którymi można zarazić się podczas polowań, a także gryzonie.
Wymieniamy główne choroby bakteryjne, których lista obejmuje około 100 infekcji: tężec, zatrucie jadem kiełbasianym, pastereloza, kolibakterioza, dżuma dymienicza, nosacizna, melioidoza, ersinioza, wibrioza, promienica.
Dennis R. Schaberg, Marvin Turck
Wstęp. Enterobakterie to Gram-ujemne, nietworzące przetrwalników pałeczki, które chociaż są tlenowe, mogą rosnąć w warunkach beztlenowych i mają tendencję do zasiedlania przewodu pokarmowego. Właściwości biochemiczne tych mikroorganizmów charakteryzują się zdolnością do fermentacji glukozy i redukcji azotanów do azotynów, a także brakiem aktywności oksydazy. Członkowie rodziny Enterobacteriaceae różne rodzaje, w tym Escherichia, Salmonella, Shigella, Klebsiella, Serratia, Enterobacter, Proteus, Morganella, Yersinia, Providencia i inne mniej znane rodzaje, różnicuje się na podstawie testów serologicznych i komputerowej analizy wyników reakcji biochemicznych. Różnicowanie Enterobacteriaceae jest ważne nie tylko z taksonomicznego punktu widzenia, ale również ze względów epidemiologicznych i terapeutycznych.
Infekcje mogą być również powodowane przez inne bakterie Gram-ujemne, które nie należą do rodziny Enterobacteriaceae. Do najważniejszych z nich należą przedstawiciele rodzajów Pseudomonas, Acinetobacter i Eikenella.
Infekcje Escherichia coli
Etiologia. E. coli – członek rodziny Enterobacteriaceae – jest komensalem przewodu pokarmowego, skąd pochodzi, w przypadku naruszenia przepuszczalności normalnych barier anatomicznych, co obserwuje się np. podczas perforacji załącznik, może rozprzestrzeniać się i wpływać na sąsiednie narządy. Uważa się, że infekcja bakteriami jelitowymi dróg moczowych odbywa się nie przez zakażone nimi drogi moczowe, ale z bezpośrednim hematogennym rozprzestrzenianiem się infekcji do nerek. Gdy infekcja dostanie się do ogniska pierwotnego, jej dalsze rozprzestrzenianie się na odległe narządy odbywa się za pomocą krwioobiegu. W rezultacie bakteriemia, która jest możliwa przy wszystkich zakażeniach bakteriami Gram-ujemnymi, może prowadzić do rozwoju wstrząsu spowodowanego endotoksynami (rozdz. 86). W ponad 50% chorób wywołanych przez Escherichia coli drogi moczowe służą jako brama wejściowa do zakażenia; częste są również infekcje pochodzące z wątroby i dróg żółciowych Jama brzuszna, skóry i płuc. U niektórych pacjentów z bakteriemią E. coli bramka wejściowa zakażenia nie jest wykrywana; często mają nowotwór lub choroby hematologiczne. Można również zaobserwować inne defekty odporności żywiciela, w tym cukrzyca marskość wątroby, niedokrwistość sierpowatokrwinkowa lub skutki niedawnej ekspozycji na promieniowanie, stosowanie leków cytotoksycznych, adrenosteroidów lub antybiotyków. Istnieją również dowody epidemiologiczne, że E. coli i inne enterobakterie mają tendencję do kolonizacji skóry i błon śluzowych pacjentów osłabionych, co może wyjaśniać częstsze występowanie tych zakażeń u osób z zaawansowaną chorobą. Jest znany zła pozycja, Co infekcje bakteryjne wywołanym przez Escherichia coli towarzyszy wydzielanie cuchnącego, mętnego wysięku. Jest to jednak spowodowane paciorkowcami beztlenowymi lub Bacteroides spp., często występującymi w połączeniu z bakterie jelitowe.
Epidemiologia. Szczepy E. coli charakteryzują się antygenami somatycznymi (O), wiciowymi (H) i otoczkowymi (K). Istnieją setki różnych wariantów serologicznych. Każdy z tych szczepów może wywołać chorobę. Badania kliniczne i epidemiologiczne wykazały, że niektóre określone serotypy E. coli częściej niż inne powodują biegunkę u dzieci. Różne wieki, a także flary choroby jelit u dorosłych.
Szczepy E. coli wywołujące biegunkę u małych dzieci są prawdopodobnie przenoszone w żłobkach przez dzieci będące nosicielami (z objawami lub bez), matki i personel. Chociaż w zwykły sposób Rozprzestrzenianie się patogenu następuje poprzez skażenie kałem, infekcja może nastąpić drogą aerogenną lub poprzez artykuły gospodarstwa domowego.
Niektóre badania epidemiologiczne sugerują, że E. coli 04, 06 i 075 są odpowiedzialne za większość infekcji E. coli innych niż biegunka u małych dzieci. Nie jest jasne, czy te szczepy są rzeczywiście bardziej zjadliwe, czy też są po prostu bardziej powszechne niż szczepy innych typów somatycznych.
Szczepy E. coli z antygenem K1 wyizolowanym z duża liczba noworodki z zapaleniem opon mózgowych. Te antygeny K biorą udział w aktywacji adhezji do komórek makroorganizmu i zapobieganiu fagocytozie.
Manifestacje. Infekcje dróg moczowych. E. coli odpowiada za ponad 75% zmiany zakaźne dróg moczowych, w tym zapalenie pęcherza moczowego, zapalenie miednicy, odmiedniczkowe zapalenie nerek i bezobjawowa bakteriuria(rozdz. 225). Patogeny wyizolowane przez hodowlę od pacjentów z ostrymi niepowikłanymi zakażeniami dróg moczowych prawie zawsze należą do E. coli, natomiast u pacjentów z przewlekłe infekcje dominują inne Enterobacteriaceae i szczepy Pseudomonas.
infekcje otrzewnej i drogi żółciowe. E. coli można zazwyczaj wyizolować przez hodowlę z perforowanego lub objętego stanem zapalnym wyrostka robaczkowego lub z ropni wtórnych do perforacji uchyłków, wrzodów trawiennych, ropni lub ropni podprzeponowych, małego worka, zawałów krezki. Często wraz z E. coli izolowane są również inne mikroorganizmy: paciorkowce beztlenowe, Clostridia, Bacteroides. Często związane z infekcją coli ostre zapalenie pęcherzyka żółciowego z gangreną i perforacją. Ostre rozedmowe zapalenie pęcherzyka żółciowego charakteryzuje się obecnością radiologicznie wykrywalnego poziomu płynu i powietrza z powodu obecności kamieni lub obwodowej warstwy gazu w ścianie pęcherzyka żółciowego. Z pęcherzyka żółciowego infekcja może rozprzestrzeniać się w górę przez drogi żółciowe, powodując zapalenie dróg żółciowych i liczne ropnie wątroby. Znacznie rzadziej, jeśli infekcja w jamie brzusznej powoduje septyczne zakrzepowe zapalenie żył żyła wrotna(zapalenie żył), co z kolei może prowadzić do ropnia wątroby.
bakteriemia. Najpoważniejszym objawem zakażenia coli jest przedostanie się do krwioobiegu. Proces ten charakteryzuje się zwykle nagłym pojawieniem się gorączki i dreszczy, ale czasami objawia się jedynie splątaniem, dusznością i niedociśnieniem. Najczęściej podobne stany obserwowane u pacjentów z zawałem dróg moczowych i pęcherzyka żółciowego lub posocznicą wewnątrzbrzuszną; w niektórych przypadkach nie jest możliwe wykrycie bramy wejściowej infekcji. Najczęściej takie infekcje obserwuje się u mężczyzn w podeszłym wieku, prawdopodobnie ze względu na dużą częstość zabiegów instrumentalnych na cewce moczowej i cewnikowania w tej grupie. Wczesny znak infekcja może służyć jako hiperwentylacja. Niedociśnienie może towarzyszyć temu procesowi od samego początku, ale zwykle rozwija się po 6-12 godzinach od wystąpienia bakteriemii. Jeśli utrzymuje się, temu stanowi towarzyszy skąpomocz i często splątanie, otępienie i śpiączka, zespół znany jako wstrząs Gram-ujemny lub wstrząs endotoksynowy (rozdz. 86). Rzadko bakteriemia wywołana przez Escherichia coli rozwija się u pacjentów z marskością wątroby przy braku oczywistej bramy wejściowej zakażenia. Przypisuje się to przeciekom wrotno-systemowym zarówno w wątrobie, jak i wokół niej, zaburzonej funkcji siateczkowo-śródbłonkowej oraz osłabionym humoralnym i komórkowym mechanizmom obronnym. Utrzymywanie się lub nawrót bakteriemii wywołanej przez E. coli lub inne enterobakterie w trakcie leczenia, tzw. bakteriemia przebijająca, charakteryzuje się złym rokowaniem i sugeruje obecność zakażenia w jamie brzusznej lub niedrenowaną ropę.
Inne objawy E. coli mogą powodować powstawanie ropni w dowolnym miejscu ciała. Podskórne ogniska zakażenia występują w miejscach wstrzyknięć insuliny u chorych na cukrzycę, w obszarach niedokrwienia kończyn oraz w ranach chirurgicznych. U pacjentów z białaczką często obserwuje się ropowicę okołoodbytniczą. Ropniom podskórnym, zwłaszcza u chorych na cukrzycę, często towarzyszy tworzenie się gazów w tkankach, co można wykryć na podstawie pojawienia się trzeszczenia lub w badaniu rentgenowskim. Objaw ten należy odróżnić od zakażenia Clostridium, które najszybciej osiąga się za pomocą barwienia metodą Grama. E. coli może wywoływać zapalenie płuc de novo i często jest wydalana z plwociny podczas nadkażenia. zmiany w płucach.
infekcja noworodkowa. Noworodki, zwłaszcza wcześniaki, często rozwijają bakteriemię E. coli związaną z zapaleniem opon mózgowych i odmiedniczkowym zapaleniem nerek. Zanieczyszczenie kałem i brak matczynych przeciwciał gamma-globuliny (IgM) to dwa główne czynniki, które czynią tę kohortę szczególnie podatną na zakażenie coli.
Nieżyt żołądka i jelit. Dzieci poniżej 2 roku życia rozwijają zapalenie żołądka i jelit, typowe objawy którymi są nudności, wymioty i biegunka. Większość ognisk ma miejsce w żłobkach i jest spowodowana przez specyficzne enteropatogenne szczepy E. coli (EPEC). Szczepy te są zdolne do wytwarzania toksyn, z których jedna jest termolabilna (LT) i podobna do toksyny wytwarzanej przez Vibrio cholerae, podczas gdy druga toksyna (ST) jest termostabilna (także rozdz. 89 i 115). W celu szybkiej identyfikacji drobnoustrojów należących do serotypów często wykrywanych w tym zespole stosuje się metody wykrywania przeciwciał fluorescencyjnych. Chociaż teoretycznie każdy szczep E. coli może zostać wyizolowany przez hodowlę, liczba różnych serotypów biorących udział w tym procesie pozostaje ograniczona. Wynika to z faktu, że informacja genetyczna kodująca produkcję toksyny znajduje się na plazmidach i może być przenoszona między szczepami. Chociaż biegunka jest zwykle wywoływana przez enterotoksyny, czasami E. coli może mieć działanie enteroinwazyjne, obejmujące błonę śluzową i powodujące chorobę podobną do czerwonki Shigella. Szybkie odwodnienie i wysoka śmiertelność wymagają natychmiastowego rozpoznania tego stanu, izolacji dzieci i leczenia zarówno chorych, jak i tych, którzy mieli z nimi kontakt. Wiadomo również, że powoduje E. coli ostra biegunka u dorosłych, zwłaszcza wyjeżdżających za granicę.
Badania laboratoryjne. Nie ma specyficznych parametrów laboratoryjnych dla infekcji E. coli. Liczba leukocytów jest zwykle zwiększona z przewagą granulocytów. Czasami jednak liczba białych krwinek jest normalna lub niska. W przypadkach, gdy infekcja coli rozwija się u wcześniej zdrowej osoby, niedokrwistość nie jest wykrywana, ale często obserwuje się niedokrwistość związaną ze współistniejącą chorobą. E. coli rośnie szybko na podłożach bakteriologicznych i musi być izolowana z odpowiednich wydzielin i krwi. W obecności bakteriemii mogą rozwinąć się zaburzenia metaboliczne, w tym azotemia, kwasica metaboliczna, hipokaliemia, hiperkaliemia i różne wady układu krzepnięcia krwi.
Diagnostyka. W barwieniu metodą Grama E. coli nie można odróżnić od większości innych bakterii Gram-ujemnych. Do dokładnej identyfikacji niezbędne jest uzyskanie odpowiedniej charakterystyki biochemicznej mikroorganizmu wyizolowanego podczas inokulacji. U wybranych pacjentów z nawracającymi zakażeniami dróg moczowych serotypowanie E. coli może być pomocne w różnicowaniu między nawrotem a ponowną infekcją.
Leczenie. Jak z innymi choroba zakaźna istotnym punktem w leczeniu zakażeń wywołanych przez Escherichia coli jest drenaż treści ropnej i usunięcie ciała obce. Jeśli jako czynnik etiologiczny konkretnej infekcji sugeruje się E. coli, wybór odpowiedniego środka przeciwdrobnoustrojowego zależy od lokalizacji i rodzaju infekcji, a także od jej ciężkości. Wynik często zależy od choroby podstawowej. Na przykład w ostrych, niepowikłanych zakażeniach dróg moczowych u kobiet choroba często ustępuje samoistnie, nawet bez leczenia przeciwbakteryjnego, i nie ma dowodów na to, że antybiotyki są skuteczniejsze niż sulfonamidy. Natomiast u pacjenta z białaczką bakteriemia E. coli może nie reagować na antybiotykoterapię, jeśli nie można jednocześnie osiągnąć remisji hematologicznej.
W większości sytuacji antybiotyki należy dobierać na podstawie testów lekowrażliwości in vitro. Chociaż nie istnieje leki, które są równie aktywne przeciwko wszystkim szczepom Escherichia coli, wiele leków jest dość skutecznych przeciwko większości izolowanych klinicznie szczepów. Chociaż niektóre szczepy E. coli, zwłaszcza te szpitalne, mogą być stosunkowo oporne, ampicylina w dawce 2 do 4 g dziennie dożylnie, domięśniowo lub doustnie pozostaje skuteczna. W ciężkich zakażeniach dawkę ampicyliny można zwiększyć do 12 g na dobę przy podawaniu dożylnym. Cefalosporyny są również skuteczne przeciwko E. coli; korzystne działanie zapewniają związki takie jak cefazolina i cefapiryna. Nowsze leki, tzw. cefalosporyny trzeciej generacji, mają niższe minimalne stężenia hamujące czynnik zakaźny. Ten zwiększona aktywność w połączeniu z nieznacznie zwiększoną przepuszczalnością w ośrodkowym układzie nerwowym pozwala na ich zastosowanie w leczeniu zapalenia opon mózgowo-rdzeniowych wywołanego przez E. coli (rozdz. 346). Gentamycyna i tobramycyna były z powodzeniem stosowane w podstawowa opieka ciężkich zakażeń coli w dawce 5 mg/kg mc. na dobę, podzielonej na trzy dawki co 8 godzin. wysoka aktywność przeciwko szczepom opornym na inne aminoglikozydy. Stosuje się go w dawce 15 mg/kg na dobę, podzielonej na kilka dawek co 8-12 h. Tetracykliny i lewomycetynę nadal stosuje się w leczeniu zakażeń wywołanych przez Escherichia coli, ale obecnie dostępne są bardziej skuteczne leki. Chociaż w leczeniu zalecane są schematy wielolekowe, w większości przypadków nie jest konieczne stosowanie więcej niż jednego leku. W leczeniu pacjentów z bakteriomoczem wywołanym przez E. coli skuteczne są nitrofurantoina (400 mg) i kwas nalidyksowy (2-4 g); jednak tych leków nie należy stosować w przypadku infekcji, które nie obejmują dróg moczowych. Na choroby zakaźne dróg moczowych stosuje się również trimetoprim - sulfametoksazol (biseptol).
Zapobieganie. Aby zakończyć epidemię biegunki u małych dzieci, potrzebna jest izolacja i terapia przeciwdrobnoustrojowa. U dorosłych wiele zakażeń E. coli jest wynikiem narażenia szpitalnego. Częstość ich występowania można zmniejszyć, ograniczając stosowanie stałych cewników moczowych i moczowych cewniki dożylne, starannego przestrzegania zasad aseptyki chirurgicznej, właściwej izolacji zakażonych pacjentów oraz w wyniku rozważnego i rozsądnego stosowania antybiotyków, glikokortykosteroidów i leków cytotoksycznych.
Infekcje Klebsiella-Enterobacter-Serratia
Obok E. coli najważniejszymi bakteriami jelitowymi zakażającymi człowieka są Klebsiella, Enterobacter i Serratia, również należące do rodziny enterobakterii. Według licznych danych Klebsiella jest bardziej oporna na antybiotyki niż E. coli, a ich izolacja z krwi, wysięków ropnych i moczu ma znacznie poważniejszą wartość epidemiologiczną i prognostyczną.
Pałeczki Friedlandera (K. pneumoniae) to kapsułkowane bakterie Gram-ujemne występujące wśród normalna mikroflora jamy ustnej lub jelit. Klebsiella są spokrewnione z bakteriami z rodzaju Serratia iz rodzaju Enterobacter i można je rozróżnić tylko za pomocą specjalnych testów na dekarboksylazę aminokwasową. oprócz określone metody różnicowanie przedstawicieli rodzajów Klebsiella, Enterobacter i Serratia wg aktywność biochemiczna Należy zauważyć, że przedstawiciele szczepu Klebsiella są zwykle nieruchomi i tworzą duże śluzowe kolonie na powierzchni gęstych pożywek, podczas gdy ruchliwość jest charakterystyczna dla innych gatunków. Ponadto szczepy Klebsiella mogą różnić się w zależności od typu antygenów otoczkowych. Zidentyfikowano już ponad 75 typów kapsułek. Istnieje niewiele dowodów na to, że niektóre typy są bardziej zjadliwe niż inne, a głównym celem typowania otoczkowego Klebsiella jest wyjaśnienie ich roli epidemiologicznej w ogniskach szpitalnych.
Klebsiella rhinoscleromatis najprawdopodobniej jest czynnikiem etiologicznym rhinoscleroma, a K. ozenae jest czasami izolowana z jamy nosowej pacjentów z ostrym, ciężkim przewlekły nieżyt nosa, w połączeniu z zanikiem małżowiny nosowej i postępującą utratą węchu. Klebsiella oxytoca to nowe oznaczenie indolo-dodatnich szczepów K. pneumoniae.
Patogeneza. Klebsiella, Enterobacter i Serratia mogą powodować choroby w różnych obszarach anatomicznych. Jednak wyniki badań klinicznych i epidemiologicznych sugerują, że wśród przedstawicieli tych rodzajów mikroorganizmów mogą występować różnice w stopniu patogeniczności, a ich dokładna identyfikacja taksonomiczna ma pewne znaczenie. Pomimo tego, że w przeszłości K. pneumoniae izolowano głównie z infekcji układu oddechowego, obecnie większość szczepów izolowanych z materiału klinicznego stwierdza się również w zakażeniach układu moczowego. Objawy kliniczne i patogeneza tych zakażeń są podobne do wywoływanych przez bakterie E. coli, jednak Klebsiella częściej występuje u pacjentów z powikłanymi i obturacyjnymi zmianami w drogach moczowych. Nierzadkie są również zmiany infekcyjne dróg żółciowych, jamy brzusznej, ucha środkowego, wyrostka sutkowatego, zatok przynosowych i opony twardej. W tych lokalizacjach Klebsiella jest bardziej powszechna niż Enterobacter lub Serratia i prawdopodobnie powoduje cięższą chorobę. Niewątpliwie zwiększona częstość chorób powodowanych przez Serratia wynika przede wszystkim z rozprzestrzeniania się tej infekcji w szpitalach. Escherichia często odgrywają rolę głównego czynnika etiologicznego w rozwoju ognisk bakteriemii szpitalnej spowodowanej zanieczyszczonym płynem dożylnym.
Manifestacje. Objawy przedmiotowe i podmiotowe infekcji powszechnie wywoływanych przez Klebsiella, w szczególności infekcji dróg moczowych, dróg żółciowych i jamy brzusznej, nie różnią się od objawów infekcji wywołanych przez Escherichia coli. Zwykle rozwijają się u pacjentów z cukrzycą, a także w postaci nadkażeń obserwuje się u pacjentów otrzymujących środki przeciwdrobnoustrojowe na które patogen jest odporny. Klebsiella jest również ważnym czynnikiem etiologicznym wstrząs septyczny. Serratia i Enterobacter są prawie wyłącznie patogenami szpitalnymi. Drobnoustroje te biorą udział jako czynniki chorobotwórcze w wielu infekcjach, a najczęściej w rozwoju zapalenia płuc, infekcji dróg moczowych i bakteriemii.
Zapalenie płuc. Klebsiella jest dobrze znana jako czynnik chorobotwórczy w choroby płuc, jednak prawdopodobnie stanowi mniej niż 1% wszystkich przypadków bakteryjnego zapalenia płuc. Choroba ta jest najbardziej typowa dla mężczyzn w wieku powyżej 40 lat i jest najczęściej wykrywana u pacjentów z alkoholizmem. Innymi czynnikami powodującymi zwiększoną wrażliwość na tę infekcję są cukrzyca i przewlekłe choroby oskrzelowo-płucne. U pacjentów z alkoholizmem czynnikiem inicjującym rozwój zakażenia jest najprawdopodobniej zachłyśnięcie się wydzieliną ustno-gardłową zawierającą klebsiellę. W tym przypadku objawy kliniczne są podobne do obserwowanych w pneumokokowym zapaleniu płuc (rozdział 93) i charakteryzują się nagłym pojawieniem się dreszczy, gorączką, produktywnym kaszlem i silnym bólem opłucnej. Pacjenci często leżą na ziemi i majaczą, ale można to również zaobserwować infekcja pneumokokowa. W płucach zmiana jest najczęściej zlokalizowana w prawym górnym płacie, ale zwykle postępuje szybko i nieleczona może rozprzestrzeniać się z jednego płata do drugiego. Szybko rozwija się sinica i duszność, może wystąpić żółtaczka, wymioty i biegunka. Badanie fizykalne ujawnia guzek tkanka płucna z powodu powstania wysięku opłucnowego lub martwiczego zapalenia płuc z szybkim tworzeniem się jam. Liczba leukocytów na obwodzie może być podwyższona, ale często jest niska, co prawdopodobnie odzwierciedla ciężką infekcję u alkoholików z niewystarczającymi rezerwami szpik kostny i niedobór kwasu foliowego. Znacznie częściej niż w przypadku pneumokokowego zapalenia płuc obserwuje się ropnie i ropniak płuc. Wynika to ze zdolności Klebsiella do powodowania niszczenia tkanek. Tylko czasami ujawniają się tzw. charakterystyczne objawy radiologiczne, na przykład zmniejszenie objętości płuc w wyniku ich zagęszczenia i regionalne zmiany rozedmowe; można je również znaleźć w infekcjach pneumokokowych, a także w martwiczym zapaleniu płuc wywołanym przez inne bakterie Gram-ujemne.
Klebsiella, Serratia i Enterobacter często występują w szpitalnym zapaleniu płuc. U starszych pacjentów bakterie Gram-ujemne kolonizują jamę ustną gardła, a następnie mogą rozprzestrzeniać się przez drogi oddechowe i powodować zapalenie płuc lub ropne zapalenie oskrzeli. Te patogeny, zwłaszcza Serratia, powodują wybuchy infekcji, które mają wspólne źródło i są związane z zakażeniem wielu leki stosowany w terapii oddechowej. Z reguły szczepy Serratia o największej lekooporności nie są zabarwione i częściej są izolowane z zakażeń szpitalnych. Jednak zarówno pigmentowane, jak i wielowrażliwe na leki szczepy Serratia są również wykrywane w infekcjach związanych ze stosowaniem zanieczyszczonych roztwory lecznicze. Czasami infekcja Klebsiella może postępować (często bardzo powoli) do przewlekłego martwiczego zapalenia płuc, które przypomina gruźlicę. Główne objawy obserwowane w tym przypadku to kaszel z odkrztuszaniem, osłabienie, niedokrwistość.
Diagnostyka. Diagnoza pozaszpitalne zapalenie płuc ustala się w obecności objawów klinicznych charakterystycznych dla zakażeń wywołanych przez Klebsiella oraz na podstawie izolacji tego mikroorganizmu. Wstępne rozpoznanie należy postawić na podstawie badania plwociny po barwieniu metodą Grama. Jednocześnie w rozmazie przeważają krótkie, grube bakterie Gram-ujemne, często otoczone jasną, niebarwioną torebką. Często te organizmy Gram-ujemne występują razem z ziarniakami Gram-dodatnimi, a ponieważ bakterie Gram-dodatnie są łatwiejsze do wykrycia, bakterie Gram-ujemne mogą zostać przeoczone, co utrudnia diagnozę i może prowadzić do opóźnienia przepisanego leczenia. Dodatkowym dowodem zmiany zakaźnej płuc wywołanej przez Klebsiella jest izolacja tego mikroorganizmu z krwi i wysięku opłucnowego. Przy pozapłucnej lokalizacji zakażenia patogen można łatwo wyizolować za pomocą bakterioskopowego lub kulturowego badania ropy lub wydzielin z narządów zaangażowanych w proces.
Rozpoznanie szpitalne infekcja drog oddechowych wywoływanej przez te mikroorganizmy, jest utrudniona głównie przez konieczność różnicowania zakażenia i bakterionośnika. Podczas stawiania diagnozy konieczna jest dokładna ocena objawów klinicznych procesu. W trudnych przypadkach wskazane jest posiew i badanie bakterioskopowe (barwienie metodą Grama) plwociny uzyskanej przez aspirację przeztchawiczą.
Leczenie. Ktebsiella, Enterobacter i Serratia mają różną wrażliwość na leki przeciwdrobnoustrojowe i hodowle tych patogenów izolowane podczas inokulacji powinny być badane in vitro. Zgodnie z ogólną zasadą, leczenie przeciwdrobnoustrojowe należy rozpocząć przed uzyskaniem wyników testów wrażliwości na antybiotyki. Ogólnie rzecz biorąc, większość szczepów Klebsiella jest wrażliwa na aminoglikozydy i cefalosporyny trzeciej generacji. Szczepy Klebsiella izolowane od pacjentów są niewrażliwe na większość analogów penicyliny, chociaż wzrost wielu z nich jest hamowany przez nowsze ureidopenicyliny, a mianowicie mezlocylinę (Mezlocillin). Szczepy Serratia izolowane od pacjentów są często oporne na wiele środków przeciwdrobnoustrojowych, przy czym stwierdza się rosnącą oporność na gentamycynę i tobramycynę; w takich przypadkach z powodzeniem stosowano amikacynę. Schematy leczenia przeciwbakteryjnego infekcji wywołanych przez Klebsiella, Enterobacter i Serratia różnią się w zależności od różne instytucje w zależności od charakteru lekooporności, a także stopnia ciężkości klinicznej zakażenia. W przypadku ciężkiej choroby wskazane jest przepisanie kombinacji aminoglikozydów, takich jak tobramycyna lub gentamycyna (3 do 5 mg/kg dziennie) lub amikacyna (15 mg/kg dziennie), z cefalotyną, cefapiryną lub cefazoliną ( 4 do 12 g dziennie). Nowsze cefalosporyny i/lub cefamycyny [w szczególności cefoksytyna
(Cefoksytyna)], jak również inne związki trzeciej generacji, mogą być aktywne przeciwko Klebsiella, Enterobacter i Serratia. Czasami leki mogą być bardziej aktywne niż starsze cefalosporyny, a do wybrania odpowiedniego leczenia wymagane jest badanie lekowrażliwości in vitro. Ze względu na stosunkowo niskie stężenia polimyksyny, które powstają we krwi i tkankach podczas stosowania tych leków, nie powinny być stosowane jako leki pierwszego rzutu w leczeniu ciężkich zakażeń wywołanych przez Klebsiella, pomimo widocznej wrażliwości na nie in vitro. Niezależnie od zastosowanego reżim lekowy, leczenie należy prowadzić przez co najmniej 10-14 dni i dłużej w przypadku stwierdzenia rozległej kawernizacji. Wysięk opłucnowy należy odsączyć. Używając tych środki przeciwdrobnoustrojowe niewystarczające do leczenia procesów otorbionych w jamie opłucnej. Czasami może być konieczna resekcja żebra z otwartym drenażem. Ta taktyka jest odpowiednia w przypadku nawracających wysięków.
Prognoza. Przed wprowadzeniem do praktyki lekarskiej środki przeciwdrobnoustrojowe częstość zgonów z powodu tych infekcji wahała się od 50 do 80%, a śmierć pacjentów często obserwowano w ciągu pierwszych 48 godzin od początku choroby. Nawet przy leczeniu przeciwbakteryjnym przebieg tych zakażeń jest bardzo zmienny, a rokowanie należy oceniać ostrożnie. W największym stopniu zależy to od wieku pacjentów, a także od występowania skłonności do alkoholizmu, wyczerpania i ciężkich współistniejące choroby.
Infekcje Proteus, Morganella i Providencia
Etiologia. Rodzaj Proteus z rodziny Enterobacteriaceae obejmuje bakterie Gram-ujemne, które nie fermentują laktozy i charakteryzują się aktywna mobilność i pełzający, rozprzestrzeniający się wzrost na powierzchni gęstej pożywki. Mikroorganizmy, które wcześniej zostały sklasyfikowane i przypisane do rodzaju Proteus, po niedawnym szczegółowe badanie DNA otrzymało nowe nazwy. P. morganii została sklasyfikowana jako Morganella morganii, podczas gdy niektóre biogrupy B. rettgeri zostały przeklasyfikowane jako Providencia stuartii i Providencia rettgeri. P. mirabilis i P. vulgaris zachowały swoje nazewnictwo. P. mirabilis powoduje 75-90% infekcji u ludzi i różni się od innych wymienionych mikroorganizmów tym, że nie ma zdolności do tworzenia indolu. Wszystkie cztery gatunki rozkładają mocznik, tworząc amon. Niektóre szczepy P. vulgaris mają wspólny antygen z niektórymi riketsjami, co wyjaśnia pojawienie się przeciwciał przeciwko białkom (reakcja Weila-Felixa) w durze brzusznym, japońskiej gorączce rzecznej (tsutsugamushi) i gorączce Gór Skalistych. Mikroorganizmy zrzeszone w grupie Providencia bardzo blisko sąsiadują z przedstawicielami rodzaju Proteus, różniąc się od nich tylko niektórymi właściwości biochemiczne.
Epidemiologia i patogeneza. Te mikroorganizmy normalnie występują w glebie, wodzie i ścieki i są częścią normalnej flory jelitowej. Czasami przypisuje się im etiologiczną rolę w biegunce małych dzieci, ale nie ma to wystarczających dowodów. Często stwierdza się je w posiewach z powierzchownych ran, osuszonych jam ucha środkowego i plwociny, zwłaszcza u pacjentów leczonych antybiotykami. W takich warunkach zastępują bardziej wrażliwą florę, która jest zabijana przez te leki.
Manifestacje. Te mikroorganizmy rzadko są przyczyną pierwotnej zmiany. Wywołują chorobę zwykle w miejscach wcześniej zakażonych innymi patogenami: na skórze, w uszach, wyrostek sutkowaty, zatok, oczu, jamy brzusznej, kości, dróg moczowych, opon mózgowych, płuc, krwioobiegu.
Infekcje skóry. Drobnoustroje te przemieszczają się w wydzielinie z ran pooperacyjnych, zwłaszcza po terapia przeciwdrobnoustrojowa, ale nigdy nie dołączaj do normalnej mikroflory rany, jeśli nastąpi normalne gojenie, tkanki są żywe i nie ma ciał obcych. Często w połączeniu z innymi bakteriami Gram-ujemnymi lub gronkowcami mogą zakażać spalić powierzchnie, żylaki, owrzodzenia tworzące się z odleżynami.
Infekcje ucha i zatoki wyrostka sutkowatego. Zapalenie ucha środkowego i zapalenie wyrostka sutkowatego, zwłaszcza wywołane przez P. mirabilis, może prowadzić do rozległego zniszczenia ucha środkowego i zatoki wyrostka sutkowatego. Cuchnąca wydzielina, perlak i ziarnina stanowią średnio chroniczne ognisko zakażenia i Ucho wewnętrzne oraz w wyrostku sutkowatym, powodując głuchotę. Jako przypadkowe powikłanie możliwy jest rozwój porażenia nerwu twarzowego. Główne niebezpieczeństwo tych infekcji polega na możliwości ich rozprzestrzenienia się do jamy czaszki, prowadząc do zakrzepicy zatok bocznych, zapalenia opon mózgowo-rdzeniowych, ropnia mózgu i bakteriemii.
Infekcje oka. Drobnoustroje te mogą powodować owrzodzenia rogówki, zwykle będące konsekwencją urazu oka, kończące się zapaleniem gałki ocznej i zniszczeniem. gałka oczna.
Zapalenie otrzewnej. Istnienie część integralna normalnej mikroflory jelitowej, przedstawicieli tych rodzajów można wyizolować z jamy brzusznej po perforacji narządy wewnętrzne lub zawał jelit.
Infekcje dróg moczowych. Drobnoustroje te są główną przyczyną infekcyjnych zmian w drogach moczowych, zwłaszcza u pacjentów z przewlekłym bakteriomoczem, z których wielu cierpi na uropatię zaporową, po ingerencjach instrumentalnych w pęcherz moczowy i powtarzane kursy chemoterapia. Często są izolowane od pacjentów z licznymi uszkodzeniami nerek lub Pęcherz moczowy towarzyszy bakteriuria. Można to wytłumaczyć aktywnością ureazy tych mikroorganizmów, która warunkuje zasadowy odczyn moczu i stwarza dogodne środowisko do powstawania kamieni amonowo-magnezowo-fosforanowych.
bakteriemia. Wprowadzenie do krwioobiegu jest najpoważniejszym przejawem zakażenia wywołanego przez przedstawicieli rodzajów Proteus, Morganella i Providencia. W 75% przypadków drogi moczowe służą jako brama wejściowa do zakażenia; w innych przypadkach główny nacisk kładziony jest na drogi żółciowe, przewód pokarmowy, uszy, zatoki, skórę. Rozwój bakteriemii jest często poprzedzony zabiegami takimi jak cystoskopia, cewnikowanie moczowodu, resekcja przezcewkowa prostata lub inne interwencje chirurgiczne. Objawy kliniczne Objawy i wyniki badań laboratoryjnych posocznicy – gorączka, dreszcze, wstrząs, ropnie z przerzutami, leukocytoza, a czasem małopłytkowość – są podobne do objawów bakteriemii wywołanej przez E. coli, Klebsiella lub inne bakterie Gram-ujemne.
Diagnostyka. Rozpoznanie zakażenia Proteus, Morganella lub Providencia opiera się na wynikach izolacji kulturowej tych organizmów z krwi, moczu lub wysięku oraz ich identyfikacji za pomocą odpowiednich testów biochemicznych. Szczególnie ważne jest oddzielenie P. mirabilis, gatunku indolo-ujemnego, od organizmów indolo-dodatnich, ponieważ P. mirabilis jest wrażliwy na penicylinę i wiele innych antybiotyków. Przedstawiciele rodzaju Proteus często spotykani są w połączeniu z innymi patogenami. Specjalna uwaga zwrócono się w stronę izolacji mikroorganizmów nie spokrewnionych z P. mirabilis czy P. vulgaris, ale rosnących na tych samych pożywkach, tak aby nie były one maskowane przez pełzający wzrost Proteus. Powszechny pełzający charakter wzrostu tych bakterii utrudnia również interpretację wyników oznaczania ich lekowrażliwości.
Leczenie. Większość szczepów P. mirabilis jest wrażliwa na penicylinę wysokie stężenia(10 j. w 1 ml lub więcej), na ampicylinę, sól disodową karbenicyliny, gentamycynę, tobramycynę lub amikacynę, a także na antybiotyki cefalosporynowe. Bakteriuria wywołana przez P. mirabilis może być szybko wyeliminowana za pomocą dowolnego z wymienionych antybiotyków. Najskuteczniejsza w tej postaci zakażenia jest ampicylina w dawce 0,5 g co 4-6 h. W ciężkich zakażeniach leczenie należy prowadzić pozajelitowo: od 6 do 12 g ampicyliny lub 20 000 000 j.m. penicyliny G w skojarzeniu z tobramycyną lub gentamycyna w dawkach ułamkowych 5 mg/kg dziennie, jeśli czynność nerek nie jest uszkodzona. Istnieją dowody na to, że w zakażeniach wywołanych przez
P. mirabilis aminoglikozydy działają synergistycznie z ampicyliną i penicyliną G. Ze względu na obecność dużej liczby bardziej skuteczne leki w infekcjach wywołanych przez P. mirabilis nie ma potrzeby stosowania chloramfenikolu. Wszystkie szczepy P. mirabilis są oporne na tetracyklinę. Większość szczepów innych niż P. mirabilis jest wrażliwa tylko na aminoglikozydy i cefalosporyny trzeciej generacji. Karbenicylina, tikarcylina i nowe ureidopenicyliny są skuteczne wobec szczepów wyizolowanych z materiału klinicznego. W idealnej sytuacji terapia powinna opierać się na badaniu lekowrażliwości in vitro, aw przypadku jego braku na znajomości reprezentatywnych próbek. Podobnie jak w przypadku innych zakażeń bakteriami Gram-ujemnymi, należy zwrócić szczególną uwagę na odprowadzanie ropy, utrzymanie równowagi wodno-elektrolitowej oraz, w przypadku wstrząsu endotoksycznego, leczenie zapaści krążeniowej.
Zakażenia Pseudomonas
Etiologia. P. aeruginosa to ruchliwa, Gram-ujemna bakteria w kształcie pałeczki, która zwykle nie jest otoczona i nie tworzy przetrwalników. Rosną szybko na wszystkich typowych podłożach, a na agarze tworzą miękkie, opalizujące kolonie, zwykle o żółto-zielonym kolorze fluorescencyjnym, który powstaje w wyniku dyfuzji do pożywki dwóch pigmentów, piocyjaniny i fluoresceiny. Pseudomonas tworzy kwas z glukozy (bez gazu) i ma aktywność proteolityczną, jest oksydazo-dodatnia i tworzy amon z argininy. Identyfikacja poszczególnych szczepów odbywa się za pomocą immunofluorescencji lub typowania bakteriofagowego. Nie ma jednak dowodów na to, że szczepy te różnią się zjadliwością u ludzi. Inne rodzaje Pseudomonas - P. maltophilia, P. cepacia, P. fluorescens, P. testosteroni i P. putida są zdolne do wywoływania infekcji u ludzi. Organizmy te wykrywano głównie w ogniskach zakażeń szpitalnych. Ponadto przypisuje się im rolę czynników sprawczych bakteriemii, zapalenia wsierdzia i zapalenia kości i szpiku, które rozwijają się u narkomanów.
Epidemiologia. Mikroorganizmy z rodzaju Pseudomonas przemieszczają się po skórze zdrowi ludzie zwłaszcza w okolicy pachowej i odbytowo-płciowej. W kale dorosłych, którzy nie otrzymują antybiotyków, są rzadko spotykane. W większości przypadków Pseudomonas jest izolowany przez hodowlę jako wtórna azjadliwa mikroflora z powierzchownych ran lub z plwociny pacjentów otrzymujących antybiotyki. Zwykle ich droga nie ma wyraźnych konsekwencji, ponieważ mikroorganizmy te po prostu wypełniają próżnię bakteriologiczną powstałą w wyniku eliminacji bardziej wrażliwych bakterii. Czasami jednak infekcje Pseudomonas wpływają na ucho, płuca, skórę lub drogi moczowe chorych osób, często po stłumieniu pierwotnego patogenu przez antybiotyki. Ciężkie infekcje prawie zawsze wiążą się z miejscowym uszkodzeniem tkanek. reakcja obronna lub ze spadkiem odporności makroorganizmu. Chociaż Pseudomonas zawiera wiele potencjalnych czynników wirulencji, mikroorganizm ten rzadko powoduje chorobę u zdrowych osób. Pacjenci osłabieni mukowiscydozą, a także chorzy na neutropenię są szczególnie narażeni na rozwój ciężkich infekcji wywołanych przez P. aeruginosa. Wydaje się, że zakażenia Pseudomonas występują najczęściej u wcześniaków, u niemowląt z wady wrodzone oraz u pacjentów z białaczką (którzy zwykle otrzymują antybiotyki, glikokortykosteroidy lub leki przeciwnowotworowe), u pacjentów z oparzeniami, u pacjentów w podeszłym wieku z wyniszczającymi chorobami. Większość tych zakażeń obserwuje się w szpitalach i tak jest zakażenia egzogenne, zakażenie, z którym występuje ze środowiska, a nie ze składu normalnej mikroflory pacjentów. W szpitalach mikroorganizmy te są wykrywane na różnych przedmiotach gospodarstwa domowego, urządzeniach sanitarnych, w tym zlewozmywakach, na pisuarach, cewnikach, na rękach personelu medycznego, a także w roztwory antyseptyczne I roztwory wodne leki. Z wieloma błyskami zakażenie szpitalne układu moczowego wywołanego przez Pseudomonas stwierdzono, że patogen jest przenoszony przez nosicieli bakterii. Podobne epidemie opisano u dzieci instytucje medyczne wśród wcześniaków, a także na oddziałach oparzeń. Chociaż w normalne warunki P. aeruginosa stwierdza się w przewodzie pokarmowym tylko u około 5% zdrowych osób dorosłych, a u pacjentów hospitalizowanych częstość nosicielstwa wzrasta.
Patogeneza. Brama wejściowa zakażenia różni się w zależności od wieku pacjenta i choroby podstawowej. W niemowlęctwie i dzieciństwo częściej dotyczy to skóry, pępowiny i przewodu pokarmowego; w starszym wieku główny nacisk jest z reguły zlokalizowany w drogach moczowych. Infekcja często pozostaje zlokalizowana w obrębie skóry lub tkanki podskórnej. Podczas oparzeń obszar tkanki znajdujący się bezpośrednio pod strupem może być masowo naciekany przez bakterie i komórki biorące udział w zapaleniu i zwykle służy jako źródło bakteriemii, jedynego śmiertelnego powikłania. Hematogenne rozsiewanie zakażenia charakteryzuje się pojawieniem się licznych ognisk krwotocznych w skórze, mięśniu sercowym, płucach, nerkach i oponach mózgowych. Histologicznie zmiany te wykazują martwicę i krwotok. W typowych przypadkach ściany tętniczek są masowo naciekane bakteriami, a naczynia są częściowo lub całkowicie zakrzepnięte.
Większość szczepów P. aeruginosa wytwarza śluz, bogate w węglowodany i wraz z Ściana komórkowa drobnoustroju, który określił jego termostabilną antygenowość somatyczną. Przeciwciała przeciwko określonemu serotypowi antygenu śluzu Pseudomonas aeruginosa zapewniają ochronę przed ekspozycją eksperymentalną. Większość szczepów wyizolowanych z materiału klinicznego wytwarza szereg egzotoksyn. Egzotoksyna A, która ma wiele takich samych właściwości jak toksyna błonicza, jest najsilniejszą toksyną P. aeruginosa. Na zagrażający życiu zakażeń wywołanych przez P. aeruginosa, wysokie miano przeciwciał przeciwko egzotoksynie A koreluje ze zwiększoną przeżywalnością.
Manifestacje. Infekcje Pseudomonas wpływają na skórę, tkanki podskórne, kości i stawów, oczu, uszu, wyrostka sutkowatego i zatok przynosowych, opony mózgowe i zastawek serca. Może również wystąpić bakteriemia bez ustalonego pierwotnego miejsca zakażenia, co rodzi pytanie o skażone leki, płyny dożylne lub środki antyseptyczne, zwłaszcza jeśli izolowane są gatunki Pseudomonas inne niż P. aeruginosa .
Zakażenia skóry i tkanki podskórnej. Drobnoustroje z rodzaju Pseudomonas są często izolowane podczas badań hodowlanych wydzieliny z ran chirurgicznych i oparzeniowych, owrzodzeń żylakowatych i owrzodzeń występujących przy odleżynach, zwłaszcza po zastosowaniu antybiotykoterapii. Mogą wtórnie infekować osuszone zmiany gruźlicze lub szpikowe. Proste pasażowanie Pseudomonas w tych ogniskach świadczy jedynie o tym, że namnażanie się bakterii w głębi tkanki podskórnej nie zachodzi i nie rozwija się bakteriemia. Skórne ogniska infekcji zwykle goją się po usunięciu lub złuszczaniu martwej tkanki. Pseudomonas może powodować przebarwienia paznokci u osób, których dłonie są nadmiernie narażone na działanie wody, mydła i detergentów; osoby z grzybicą paznokci lub mające odsłonięte dłonie uraz mechaniczny(paznokcie dostają zielonkawy kolor). Patogeny z reguły są izolowane podczas wysiewania zeskrobania z płytki paznokcia. Pseudomonas przypisuje się udział w rozwoju zapalenia skóry związanego z działalność zawodowa. Ta choroba jest łagodna i leczy się samoistnie.
Zapalenie szpiku. Zapalenie kości i szpiku o tej etiologii zwykle nie obserwuje się, z wyjątkiem sytuacji, gdy rozwija się jako powikłanie bakteriemii, podanie dożylne narkotyki lub rany powstałe w wyniku nakłucia. Jeśli takie rany, zwłaszcza u dzieci w okolicy paliczków paznokciowych stopy, nie reagują na leczenie w ciągu 3-4 dni, należy podejrzewać powikłanie zapalenia kości i szpiku wywołane przez Pseudomonas.
Infekcje ucha, wyrostka sutkowatego i zatok przynosowych. Najbardziej znaną postacią infekcji ucha wywołanej przez pseudomonady jest zapalenie ucha zewnętrznego. Ta choroba jest szczególnie niepokojąca w klimacie tropikalnym. Charakteryzuje się przewlekłą surowiczo-krwawą i ropną wydzieliną z zewnątrz przewód słuchowy. Szybko postępująca ciężka infekcja jest określana jako złośliwe zapalenie ucha zewnętrznego. Pacjenci z cukrzycą są szczególnie podatni na tę chorobę. W przeciwieństwie do zwykłego zapalenia ucha zewnętrznego, zakażenie to wymaga aktywnej interwencji, obejmującej eksplorację chirurgiczną z usunięciem martwych obszarów i pozajelitową antybiotykoterapię. Zapalenie ucha środkowego lub zapalenie wyrostka sutkowatego zwykle rozwija się jako nadkażenie, które pojawia się po wyeliminowaniu drobnoustrojów Gram-dodatnich pod wpływem środków przeciwdrobnoustrojowych.
Infekcje oka. Owrzodzenie rogówki jest najcięższą postacią zakażenia oka Pseudomonas. Zwykle rozwija się w tle traumatyczny uraz oczy i może prowadzić do panophthalmitis i zniszczenia gałki ocznej. U wcześniaków objawem tej infekcji jest ropne zapalenie spojówek.
Zanieczyszczenie szkła kontaktowe lub płynne środki do soczewek mogą być ważnym mechanizmem zakażenia oka Pseudomonas.
Infekcje dróg moczowych. Drobnoustroje z rodzaju Pseudomonas są powszechnymi czynnikami sprawczymi zmian infekcyjnych dróg moczowych. Z reguły występują u pacjentów z uropatią zaporową, którzy przeszli wielokrotne manipulacje cewka moczowa lub urologiczne interwencje chirurgiczne. Bakteriomocz wywołany przez Pseudomonas nie różni się od bakteriomoczu podobna patologia różna etiologia i podłoże objawy kliniczne nie do odróżnienia od zakażenia wywołanego przez inne mikroorganizmy.
Przewód pokarmowy. W odniesieniu do mikroorganizmów z rodzaju Pseudomonas istnieją sugestie, że powodują one epidemiczną biegunkę u małych dzieci. Ponadto pewna liczba niemowląt, które zmarły z powodu posocznicy noworodków, ma klasyczne martwicze, jałowe owrzodzenia charakterystyczne dla bakteriemii Pseudomonas podczas sekcji zwłok w jelicie. „Dur brzuszny” charakteryzuje się gorączką, bólami mięśni i biegunką i występuje głównie w krajach tropikalnych. Choroba ta, zwana także gorączką 13-dniową lub gorączką szanghajską, zwykle ustępuje samoistnie. Prognozy są korzystne.
Drogi oddechowe. Pseudomonas zapalenie płuc jest rzadkie. Izolacja kulturowa tego mikroorganizmu z plwociny jest zwykle wskaźnikiem aspiracji treści jamy ustnej i gardła z obecnością wtórnego zakażenia, które rozwija się w wyniku eliminacji bardziej wrażliwej mikroflory pod wpływem antybiotyków. Normalna flora jamy ustnej i gardła hospitalizowanych pacjentów jest często zastępowana przez Gram-ujemne bakterie w kształcie pałeczek, w tym Pseudomonas, już w wieku wczesne daty od hospitalizacji. Cała linia manipulacje przeprowadzane w szpitalu mogą odgrywać rolę czynników predysponujących do rozwoju infekcji dróg oddechowych. Należą do nich stosowanie leków uspokajających, intubacja dotchawicza, stosowanie sztuczna wentylacja pod okresowym dodatnim ciśnieniem. Zakażenie w płucach często wiąże się z rozwojem mikroropni. Czynnik sprawczy jest zwykle izolowany z plwociny pacjentów z rozstrzeniami oskrzeli, przewlekłe zapalenie oskrzeli lub mukowiscydoza, a także uporczywe infekcje, w których stosowano wiele cykli chemioterapii. Często patogen jest izolowany ze stomii u pacjentów z tracheostomią. Zapalenie oskrzeli i zapalenie oskrzelików wywołane przez Pseudomonas może być końcowym powikłaniem mukowiscydozy. Szczepy patogenu wyizolowane z plwociny na gęstym podłożu agarowym mają charakterystyczny kształt kolonie tworzące śluz.
Zapalenie opon mózgowych. Samoistny rozwój zapalenia opon mózgowo-rdzeniowych wywołanego przez Pseudomonas jest niezwykły, ale patogen może dostać się do przestrzeni podpajęczynówkowej przy nakłuciu lędźwiowym, znieczulenie rdzeniowe, dokanałowo manipulacje medyczne lub uraz głowy. Przetoki z powodu wodogłowia mogą również ulec zakażeniu, a rewizja lub usunięcie przetoki jest najbardziej lecznicze.
bakteriemia. Wprowadzenie patogenu do krwiobiegu obserwuje się zwykle u pacjentów osłabionych, wcześniaków lub dzieci z wadami wrodzonymi, u pacjentów z chłoniakami, białaczkami lub innymi nowotwory złośliwe u pacjentów w podeszłym wieku, którzy przeszli interwencje chirurgiczne lub instrumentalne drogi żółciowe lub dróg moczowych. bakteriemia Pseudomonas jest ważny powód zgonów wśród pacjentów z ciężkimi oparzeniami. U dorosłych pacjentów z Pseudomonas bakteriemia jest nie do odróżnienia od bakteriemii wywołanej przez inne rodzaje patogenów. Wyjątkiem pod tym względem są dwa stany, które wskazują na zakażenie Pseudomonas: ecthyma gangrenosum, klasyczna zmiana skórna często zlokalizowana na odcinku odbytowo-płciowym lub Pacha i objawia się jako zaokrąglony, zwarty obszar o fioletowo-czarnym kolorze o średnicy około 1 cm z owrzodzonym środkiem i otaczającą strefą rumieniową; rzadko obserwowane wydzielanie zielonego moczu, prawdopodobnie z powodu jego zabarwienia werdohemoglobiną. Drobnoustroje są zwykle izolowane kulturowo ze zmian skórnych i służą jako swego rodzaju wskazówka do rozpoznania.
Bakteryjne zapalenie wsierdzia. Szereg przypadków podostrego bakteryjnego zapalenia wsierdzia wywołanego przez Pseudomonas rozwija się później operacje chirurgiczne NA otwarte serce. Zazwyczaj patogen jest wszczepiany na jedwabne lub syntetyczne nici służące do zakładania szwów lub zamykania ubytków w przegrodzie serca. Ponowne operacje w celu usunięcia przerostów i ciał obcych stanowią najbardziej obiecującą nadzieję na wyleczenie. Zapalenie wsierdzia stwierdza się na zdrowych zastawkach serca u pacjentów z oparzeniami i u osób uzależnionych od narkotyków. Konsekwencją zapalenia wsierdzia o tej etiologii są często przerzutowe ropnie w kościach, stawach, mózgu, nadnerczach i płucach.
Leczenie. W przypadku miejscowego zakażenia Pseudomonas należy przeprowadzić irygację 1% roztworem. kwas octowy lub miejscowo zastosować kolistynę lub polimyksynę B. Gdy zajęte są głębsze tkanki, ważne jest usunięcie. chirurgicznie martwe obszary i drenaż ognisk ropnych. W podobne przypadki aw przypadku zagrażających życiu infekcji, takich jak zapalenie płuc i bakteriemia, należy zastosować terapię pozajelitową. Antybiotyki aminoglikozydowe, tobramycyna i gentamycyna, hamują rozwój większości szczepów Pseudomonas.
U pacjentów z normalna funkcja użycie nerek wspomniane fundusze w ilości 5 mg/kg dziennie w dawkach podzielonych zapewni ich hamujący poziom. Amikacyna jest również aktywna przeciwko Pseudomonas i jest szczególnie skuteczna w izolowaniu szczepów patogenów z uformowaną, za pośrednictwem enzymów, lekoopornością na tobramycynę i gentamycynę. Należy go stosować w dawce 15 mg/kg dziennie w dawkach podzielonych. Ticarcillin (Ticarcillin) i mezlocillin (Mezlocillin) są aktywne przeciwko większości szczepów Pseudomonas w dawkach od 16 do 20 g dziennie. Piperacylina (Piperacylina) i azlocylina (Aziocylina) wykazują aktywność in vitro przeciwko niektórym szczepom, których nie hamuje tikarcylina. Szczepy te wyizolowane z materiału klinicznego są z reguły pochodzenia szpitalnego. Aby zmniejszyć lekooporność patogenu podczas terapii i zapewnić więcej szeroki zasięg Szczególnie u pacjentów z granulocytopenią i zakażeniem Pseudomonas często stosuje się połączenie aminoglikozydów o działaniu przeciw patogenowi z penicyliną, która wykazuje specyficzne działanie przeciw Pseudomonas aeruginosa. Bezobjawowy bakteriomocz, zwłaszcza z powodu ograniczonego zajęcia pęcherza moczowego, powinien być leczony lekami o mniejszej toksyczności, takimi jak sulfonamidy lub tetracykliny. Wrażliwość przeciwbakteryjna Pseudomonas, z wyjątkiem P. aeruginosa, jest różna, a niektóre szczepy wyizolowane z materiału klinicznego mogą być oporne na antybiotyki aminoglikozydowe. Niektóre nowsze cefalosporyny, w szczególności cefoperazon (cefoperazon) i ceftazydym (ceftazydym), również wykazują aktywność przeciwko wielu szczepom in vitro.
Zapobieganie. Częstość występowania zakażeń krzyżowych Pseudomonas Pseudomonas w szpitalach można zmniejszyć poprzez staranną aseptykę i praktyki kontroli zakażeń (rozdz. 85).
Ogólnoustrojowa profilaktyka przeciwbakteryjna mająca na celu zapobieganie kolonizacji i rozprzestrzenianiu się infekcji jest oczywiście nieskuteczna i powinna być zabroniona. Opracowano poliwalentną szczepionkę przeciwko Pseudomonas, a także specyficzną hiperimmunizowaną gamma globulinę, ale nie są one powszechnie stosowane.
Prognoza.Śmiertelność w bakteriemii Pseudomonas wynosi 75% i jest najwyższa u pacjentów we wstrząsie lub z ciężkimi chorobami współistniejącymi, takimi jak rozległe oparzenia. III stopień, białaczka, u wcześniaków. Gdy bakteriemia występuje w drogach moczowych i nie towarzyszy jej wstrząs, rokowanie jest znacznie lepsze. Zlokalizowane zakażenia Pseudomonas nie stanowią zagrożenia dla życia, dopóki nie rozwinie się rozsiew hematogenny.
Infekcje Acinetobacter
Definicja. Mikroorganizmy z rodzaju Acinetobacter to pleomorficzne pałeczki Gram-ujemne, które łatwo pomylić z mikroorganizmami z rodzaju Neisseria. Ciężkie zakażenia tymi organizmami, w tym zapalenie opon mózgowych, bakteryjne zapalenie wsierdzia, zapalenie płuc i bakteriemia, są opisywane coraz częściej.
Etiologia. Wariant A. calcoaceticus Iwoffi został opisany przez DeBorda jako Mima polymorpha w 1939 roku. Jest to jeden z dwóch dobrze znanych wariantów Acinetobacter. Innym jest A. calcoaceticus, odmiana anitratus, pierwotnie nazywana Herella vaginicola. Organizmy opisane jako Bacterium anitratum i B5W mogą być określane synonimem Acinetobacter. Mikroorganizmy te są pleomorficzne, otoczkowe, nieruchome, Gram-ujemne. Dobrze rosną na prostych pożywkach, tworząc białe, wypukłe, gładkie kolonie. Wśród drobnoustrojów hodowanych na gęstych podłożach dominują formy diplokokowe; pałeczkowate i nitkowate warianty patogenu są częściej wykrywane w płynnym podłożu. Identyfikacja gatunkowa enterobakterii opiera się na ich negatywnej reakcji z azotanami, a u przedstawicieli rodzaju Neisseria, których mogą przypominać morfologicznie, na ich bezpretensjonalności w stosunku do pożywek, na pałeczkowatej formie na płynnych pożywkach i na ich charakterystycznej ujemnej oksydazie reakcja.
Epidemiologia i patogeneza. Mikroorganizmy z rodzaju Acinetobacter są wszechobecne. Są normalnymi mieszkańcami skóry u 25% zdrowych osób. W przypadkach możliwego zaangażowania Acinetobacter w bakteriemię rozwijającą się podczas stosowania cewników dożylnych u pacjenta, uwzględnia się główne wrota zakażenia skóra. Zwiększona częstość występowania zapalenia płuc wywołanego przez Acinetobacter, zarówno pierwotnego, jak i wtórnego do nadkażenia, sugeruje również, że drogi oddechowe mogą służyć jako ważna brama do infekcji. Najprawdopodobniej mikroorganizm ten jest pospolitym komensalem o stosunkowo niskiej zjadliwości, który znacznie częściej powoduje bakterionośnik niż powoduje infekcję. Wydaje się, że choroba Acinetobacter rozwija się u osób, które nieoczekiwanie napotkają szpitalne zakażenie Gram-ujemne. Ciężkie zakażenia rozwijają się w warunkach obniżonej oporności makroorganizmów, przy interwencjach instrumentalnych lub po długotrwałym leczeniu przeciwdrobnoustrojowym lekami o szerokim spektrum działania. Odnotowano niewyjaśniony wzrost częstości powodowany przez Acinetobacter infekcje płuc późne lato. Udział tego mikroorganizmu w etiologii zapalenia spojówek, pochwy i cewki moczowej wymaga dalszego potwierdzenia.
Manifestacje. Ciężkie zakażenia Acinetobacter obejmują zapalenie opon mózgowych, podostre i ostre bakteryjne zapalenie wsierdzia, zapalenie płuc, infekcje dróg moczowych i bakteriemię. Zwykle objawy kliniczne i objawy tej infekcji nie różnią się od tych w podobnych chorobach wywołanych przez inne patogeny. Czasami Acinetobacter może powodować piorunującą bakteriemię z ciężką gorączką, zapaść naczyniowa, wybroczyny, masywne krwotoki podskórne, które są nie do odróżnienia od meningokokcemii. Częściej jednak bakteriemia wiąże się z pozornym wprowadzeniem zakażenia przez układ żylny, w szczególności przez cewniki żylne, rany chirurgiczne lub spalić powierzchnie. Może również rozwinąć się po zabiegach instrumentalnych na cewce moczowej lub w innych obszarach. W objawy kliniczne w takich chorobach dominuje endotoksemia, a ich rokowanie jest niekorzystne.
Diagnostyka. Rozpoznanie zakażenia Acinetobacter może być trudne, ponieważ personel laboratoriów bakteriologii klinicznej ma niewielką wiedzę na temat tych organizmów, co prowadzi do błędnej interpretacji wyników badań. Zamieszanie obserwowane w klasyfikacji taksonomicznej tych mikroorganizmów również nie ułatwia zadania. Ze względów praktycznych izolację Acinetobacter z krwi, płynu mózgowo-rdzeniowego, plwociny, moczu lub ropy należy uznać za istotną klinicznie, chyba że istnieją dowody na współistnienie jakiegokolwiek innego patogenu. W praktyce rozróżnienie Acinetobacter i Neisseria jest obowiązkowe, ponieważ te pierwsze są oporne na penicylinę, a te drugie są wrażliwe.
Leczenie. Wrażliwość poszczególnych szczepów Acinetobacter na antybiotyki jest różna, ale większość z nich jest hamowana przez gentamycynę, tobramycynę, amikacynę i ureidopenicyliny, takie jak piperacylina. Wrażliwość na tetracykliny jest nieprzewidywalna, a większość szczepów jest oporna na penicylinę, ampicylinę, cefalosporyny, erytromycynę i chloramfenikol. W ciężkich zakażeniach ogólnoustrojowych należy zastosować odpowiedni antybiotyk, zwykle aminoglikozyd. W przypadku miejscowych ropni wywołanych przez te mikroorganizmy konieczne jest zastosowanie drenaż chirurgiczny.
Zakażenia Eikenellą
Etiologia. E. corrodens to fakultatywne beztlenowce lub kapnofilne, gram-ujemne, pałeczkowate, oksydazo-dodatnie mikroorganizmy. Kiedy kolonie rosną na agarze z krwią, wykrywane są małe „wgniecenia” lub „korozje”. Pojawienie się widocznego wzrostu zajmuje od 48 do 72 godzin.
Epidemiologia. E. corrodens - mieszkańcy Jama ustna, wyższe dywizje dróg oddechowych i przewodu pokarmowego człowieka. Infekcje często rozwijają się w jelitach lub w jamie ustnej. Zaobserwowano związek między infekcjami Eikenella a nadużywaniem metylofenidatu, prawdopodobnie ze względu na niski potencjał redoks i wydalanie tego czynnika przez skórę, a także zanieczyszczenie igieł używanych przez narkomanów wydzieliną ustną podczas ich lizania.
Manifestacje. Najczęstsze infekcje wywołane przez Eikenellę dotyczą skóry i tkanek miękkich. Zapalenie wsierdzia, zapalenie płuc, zapalenie kości i szpiku oraz zapalenie opon mózgowych są znacznie rzadsze. Infekcje Eikenella często przypominają infekcje wywołane przez bezwzględne beztlenowce, takie jak Bacteroides fragilis lub Peptostreptococcus. Choroby często mają charakter powolnych procesów o mieszanej etiologii, w rozwoju których biorą udział tlenowe ziarniaki Gram-dodatnie; podczas drenażu jest często określana cuchnący zapach; możliwe powstawanie ropni.
Leczenie. E. corrodens jest wrażliwa na penicylinę, ampicylinę, karbenicylinę i tetracyklinę. W leczeniu tych zakażeń bardzo ważne jest zapewnienie odpowiedniego drenażu treści ropnej. Ampicylina lub penicylina w połączeniu z drenażem chirurgicznym zwykle skutkuje dobry wynik. Należy pamiętać o wyraźnej oporności Eikenelli na klindamycynę. Okoliczność ta jeszcze bardziej zwiększa znaczenie różnicowania infekcji wywołanych przez Eikenella i mieszane populacje beztlenowców.
